
Лекции / Лекция_40-41(а)
.DOC
Лекции №40-41
Производные карбоновых кислот
План.
Классификация. Номенклатура.
Галогенангидриды карбоновых кислот. Методы синтеза. Физические и химические свойства.
Ангидриды карбоновых кислот. Методы синтеза и химические свойства.
Сложные эфиры. Методы получения. Химические свойства.
Синтезы на основе эфиров 1,3-кетокислот.
Амиды карбоновых кислот. Методы получения и химические свойства. Нитрилы карбоновых кислот.
Производные угольной кислоты.
Ф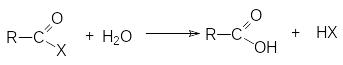 ункциональные
производные карбоновых кислот можно
рассматривать как результат замещения
гидроксильной группы кислоты на
какую-либо другую группу Х. Эти вещества
могут быть гидролизованы в кислоту в
соответствии с уравнением.
ункциональные
производные карбоновых кислот можно
рассматривать как результат замещения
гидроксильной группы кислоты на
какую-либо другую группу Х. Эти вещества
могут быть гидролизованы в кислоту в
соответствии с уравнением.
К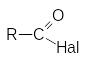 таким соединениям относят
таким соединениям относят
галогенангидриды |
|
|
|
ангидриды |
|
|
|
имиды |
|
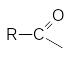
Общим элементам структуры этих соединений
является ацильная группа
Однако нитрилы R-CN также часто рассматриваются как производные карбоновых кислот, поскольку их гидролиз приводит к карбоновым кислотам.
Г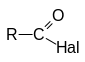 алогенангидриды
карбоновых кислот
алогенангидриды
карбоновых кислот
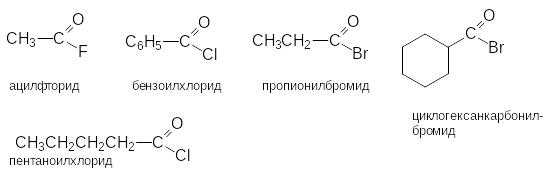
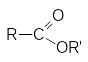
Соединения этого ряда выражаются формулой:
Названия соединений этого ряда складывается из названия ацильного радикала и галогена с окончанием "ид".
Методы получения
В
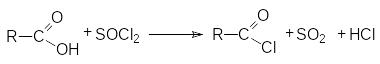 заимодействие
карбоновых кислот с галогенангидридами
неорганических кислот (SOCl2,
SO2Cl2,
PCl3,
POCl3,
PCl5,
PBr5,
COCl2)
заимодействие
карбоновых кислот с галогенангидридами
неорганических кислот (SOCl2,
SO2Cl2,
PCl3,
POCl3,
PCl5,
PBr5,
COCl2)
Так получают бромиды и хлориды.
Реакции диспропорционирования с галогенангидридами органических кислот (оксалилхлорид, бензоилхлорид).

Эти реакции лежат в основе синтеза ацилхлоридов.
Физические свойства и строение
А цилгалогениды
представляют собой бесцветные жидкости
или кристаллические вещества с острым
запахом, легколетучие, на воздухе
"дымят". Низшие ацилфториды
газообразны. В воде растворяются плохо,
но быстро с ней реагируют. В ацильной
группе заряд на карбонильном углероде
существенно завышен по сравнению с
карбонильным углеродом карбоновых
кислот из-за сильных электроакцепторных
свойств атомов галогенов
цилгалогениды
представляют собой бесцветные жидкости
или кристаллические вещества с острым
запахом, легколетучие, на воздухе
"дымят". Низшие ацилфториды
газообразны. В воде растворяются плохо,
но быстро с ней реагируют. В ацильной
группе заряд на карбонильном углероде
существенно завышен по сравнению с
карбонильным углеродом карбоновых
кислот из-за сильных электроакцепторных
свойств атомов галогенов
Это обусловливает высокую склонность галогенангидридов к взаимодействию с нуклеофильными реагентами.
Химические свойства
Реакции нуклеофильного замещения
А цилгалогениды
легко реагируют с различными нуклеофильными
реагентами, причем эти реакции не требуют
катализа. Общая схема этих реакций может
быть представлена уравнениями
цилгалогениды
легко реагируют с различными нуклеофильными
реагентами, причем эти реакции не требуют
катализа. Общая схема этих реакций может
быть представлена уравнениями
Важными реакциями нуклеофильного замещения по ацильному углероду являются:
Г
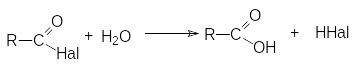 идролиз
идролиз
В
 заимодействие
со спиртами (этерификация)
заимодействие
со спиртами (этерификация)
В
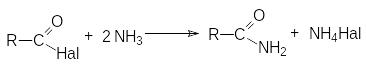 заимодействие
с аммиаком и аминами (аммонолиз)
заимодействие
с аммиаком и аминами (аммонолиз)
В
 заимодействие
с гидразином и его производными
заимодействие
с гидразином и его производными
В
 заимодействие
с металлоорганическими соединениями
заимодействие
с металлоорганическими соединениями
П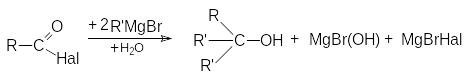 о
этому суммарно реакцию можно представить
следующей схемой
о
этому суммарно реакцию можно представить
следующей схемой
Реакции восстановления
В
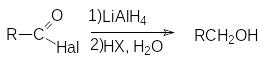 осстановление
натрийборгидридом или литийалюминий
гидридом.
осстановление
натрийборгидридом или литийалюминий
гидридом.
В
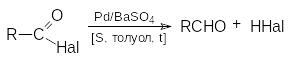 осстановление
по Розенмунду
осстановление
по Розенмунду
Р еакция
с диазометаном (реакция Арндта-Эйстерта)
еакция
с диазометаном (реакция Арндта-Эйстерта)
Эта реакция является синтетическим средством увеличения длины углеводородных цепей органических соединений на один атом углерода.
А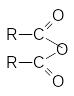 нгидриды
карбоновых кислот
нгидриды
карбоновых кислот
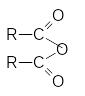
Строение ангидридов выражается следующей общей формулой
Методы получения
Т
 ермическая
дегидратация карбоновых кислот.
ермическая
дегидратация карбоновых кислот.
В
 заимодействие
карбоновых кислот с водоотнимающими
агентами.
заимодействие
карбоновых кислот с водоотнимающими
агентами.
Взаимодействие ацилгалогенидов с карбоновыми кислотами.
![]()
Таким способом получают несимметричные ангидриды.
В
 заимодействие
ацилгалогенидов с солями карбоновых
кислот.
заимодействие
ацилгалогенидов с солями карбоновых
кислот.
В
 заимодействие
кетена и карбоновых кислот.
заимодействие
кетена и карбоновых кислот.
Химические свойства ангидридов карбоновых кислот
Одна ацильная группа действует на другую как сильный акцептор, поэтому на карбонильном атоме углерода концентрируется достаточно высокий положительный заряд. Это обусловливает высокую реакционную способность ангидридов в реакциях нуклеофильного замещения
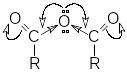
Реакция нуклеофильного замещения
Ангидриды карбоновых кислот легко реагируют с различными нуклеофильными реагентами, хотя скорость реакции меньше, чем в случае ацилгалогенидов.
О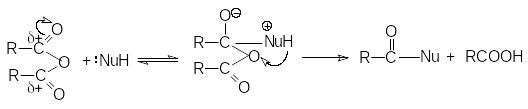 бщий
механизм реакции ангидридов карбоновых
кислот с нуклеофилом может быть
представлен схемой:
бщий
механизм реакции ангидридов карбоновых
кислот с нуклеофилом может быть
представлен схемой:
М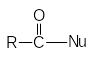 ожно
видеть, что в результате реакции кроме
продукта нуклеофильного
ожно
видеть, что в результате реакции кроме
продукта нуклеофильного
замещения образуется карбоновая кислота.
Важнейшими реакциями нуклеофильного замещения с участием ангидридов карбоновых кислот является:
Гидратация.
(RCO)2O + H2O 2RCOOH
Этерификация.
(RCO)2O + R'OH RCOOR' + RCOOH
Взаимодействие с аммиаком и аминами (аммонолиз).
(RCO)2O + 2NH3 RCONH2 + RCOONH4
К е т е н
Кетен формально может рассматриваться как ангидрид уксусной кислоты.
CH2=C=O + H2O CH3CHO
Кетен получают следующими методами:
Пиролизом кетонов или карбоновых кислот на фосфатных катализаторах.

Отщепление галогеноводорода от ацилхлоридов в присутствии сильного органического основания, например, третичного амина.

Дегалогенирование - галогенацилгалогенида
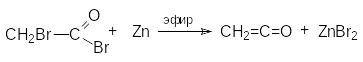
Химические свойства
Химическое поведение кетена определяют два фактора: напряженность
![]()
молекулы и высокий положительный заряд на карбонильном углероде
Н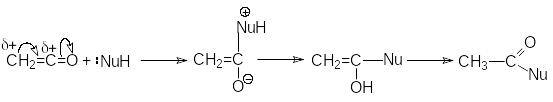 аиболее
типичными реакциями кетенов являются
реакции нуклеофильного присоединения.
аиболее
типичными реакциями кетенов являются
реакции нуклеофильного присоединения.
Н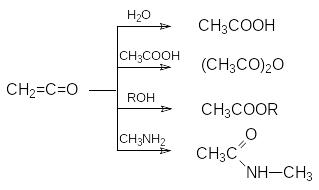 аиболее
важными среди этих являются реакции
гидратации, образования ангидридов
сложных эфиров и амидов карбоновых
кислот:
аиболее
важными среди этих являются реакции
гидратации, образования ангидридов
сложных эфиров и амидов карбоновых
кислот:
Поскольку в результате этих реакций не образуется каких-либо других продуктов, то кетен является идеальным ацилирующим агентом.
Сложные эфиры
С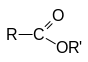 ложные
эфиры – производные карбоновых кислот,
которые можно рассматривать как результат
замещения гидроксильной группы карбоновой
кислоты на алкоксирадикал
ложные
эфиры – производные карбоновых кислот,
которые можно рассматривать как результат
замещения гидроксильной группы карбоновой
кислоты на алкоксирадикал
Методы получения сложных эфиров:
Этерификация карбоновых кислот (см. химические свойства карбоновых кислот).

А
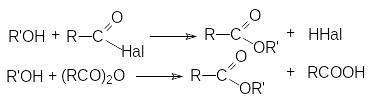 цилирование
спиртов галогенангидридами и ангидридами
карбоновых кислот.
цилирование
спиртов галогенангидридами и ангидридами
карбоновых кислот.
Ацилирование алкоголятов галогенангидридами и ангидридами карбоновых кислот.
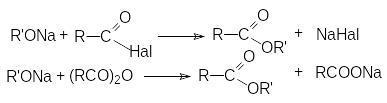
А
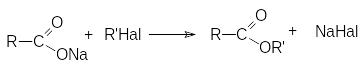 лкилирование
солей карбоновых кислот.
лкилирование
солей карбоновых кислот.
Этерификация амидов и нитрилов карбоновых кислот.
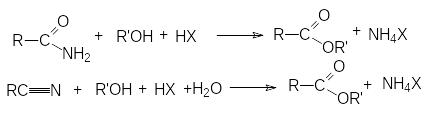
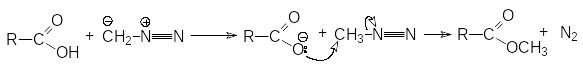
С
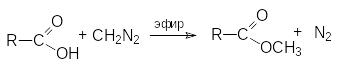 интез
метиловых эфиров взаимодействием
карбоновых кислот с диазометаном.
интез
метиловых эфиров взаимодействием
карбоновых кислот с диазометаном.
Механизм реакции:
Реакция Байера-Виллигера
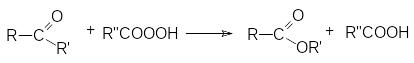
Методы синтеза лактонов (циклических сложных эфиров)
В
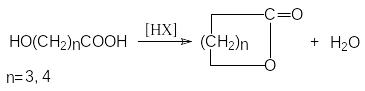 нутренняя
этерификация -
и -оксикарбоновых
кислот.
нутренняя
этерификация -
и -оксикарбоновых
кислот.
Реакция Байера-Виллигера

Физические свойства и строение сложных эфиров
Сложные эфиры являются бесцветными жидкостями или кристаллическими веществами с приятным запахом. Температура кипения сложных эфиров обычно ниже чем температура близких по молекулярной массе карбоновых кислот. Это свидетельствует об уменьшении межмолекулярных взаимодействий, что объясняется отсутствием межмолекулярных водородных связей.
П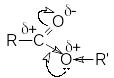 олярность
связей в молекуле сложного эфира подобна
полярности связи в карбоновых кислотах.
олярность
связей в молекуле сложного эфира подобна
полярности связи в карбоновых кислотах.
Основное отличие от карбоновых кислот – отсутствие подвижного протона, вместо него находится углеводородный остаток. Электрофильный центр находится на карбонильном и алкильном углеродном атоме. В то же время карбонильный кислород обладает основностью.
Химические свойства
Объектами нуклеофильной атаки могут быть ацильный или алкильный углерод. В то же время кислотность водородных атомов при -углеродном атоме радикала кислоты обусловливает склонность сложность эфиров к реакции конденсации.
Реакции нуклеофильного замещения
Гидролиз.
Р![]() азличают
кислотнокаталитический гидролиз и
основной гидролиз (омыление). Кислотный
гидролиз представляет собой обратимую
реакцию.
азличают
кислотнокаталитический гидролиз и
основной гидролиз (омыление). Кислотный
гидролиз представляет собой обратимую
реакцию.
Механизм этой реакции – см в разделе Кислотно-каталитическая этерификация – Химические свойства карбоновых кислот.
Реакция омыления необратима. Основание не только ускоряет реакцию гидролиза, но выступает в качестве реагента. Эффективность реакции обусловлена высокой нуклеофильной активностью гидроксил-анионов.
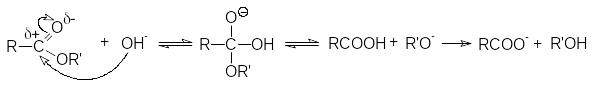
RCOOR' + NaOH RCOONa + R'OH
Аммонолиз.

П
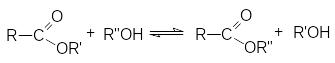 ереэтерификация.
ереэтерификация.
Реакция катализируется кислотами или основаниями.
Взаимодействие с магний- и литий-органическими соединениями.
а) Реакция с магнийорганическими соединениями подобна реакции с галогенангидридами.
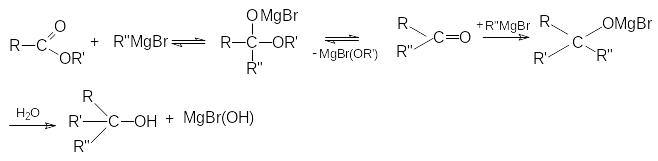
б) Взаимодействие с Li-органическими соединениями.

Р еакции
восстановления.
еакции
восстановления.
Реакции конденсации.
К
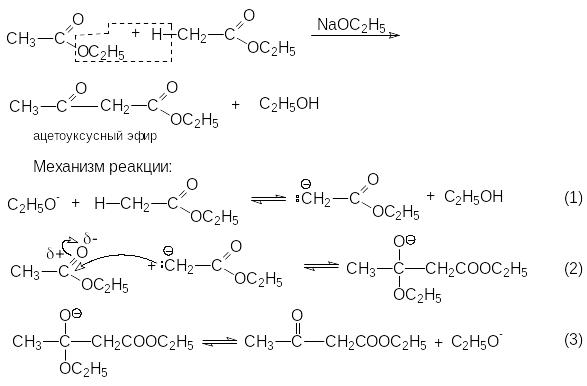 онденсация
Кляйзена – наиболее важная в синтетическом
отношении реакция. Ее стехиометрический
результат заключается в автоконденсации
этилацетата, катализируемая этилатом
натрия,
онденсация
Кляйзена – наиболее важная в синтетическом
отношении реакция. Ее стехиометрический
результат заключается в автоконденсации
этилацетата, катализируемая этилатом
натрия,
Условия равновесия неблагоприятны для всех трех стадий. Поэтому равновесие брутто-реакций существенно смещено в левую сторону.
Ф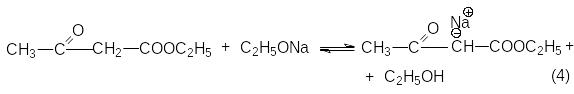 акторами
смещения равновесия могут быть: отгонка
этилового спирта, применение избытка
этилата натрия. Последний метод
оказывается эффективным, так как этанол
более слабая кислота, чем енол сложного
эфира, и избыток этилата смещает
равновесие нацело вправо вследствие
превращения -кетоэфира
в соль енола.
акторами
смещения равновесия могут быть: отгонка
этилового спирта, применение избытка
этилата натрия. Последний метод
оказывается эффективным, так как этанол
более слабая кислота, чем енол сложного
эфира, и избыток этилата смещает
равновесие нацело вправо вследствие
превращения -кетоэфира
в соль енола.
Очевидно, что продукт конденсации необходимо получить из соли енола и выделять в условиях, предотвращающих обратную реакцию распада на исходные реагенты. Наилучшим методом оказывается "замораживание" реакционной смеси для чего ее вливают в избыток холодной кислоты.
Для протекания конденсации Кляйзена необходимы следующие структурные предпосылки: исходный эфир должен иметь водородный атом при -углеродном атоме, чтобы могли осуществиться реакции, представленные в механизме (реакции (1)-(3)) и два водородных атома при -углероде, для того чтобы оказалось возможным смещение равновесия реакции в сторону продукта за счет образования енолят-аниона ацетоуксусного эфира.
О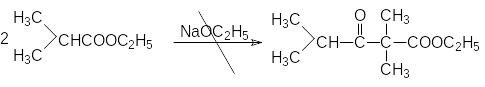 чевидно,
что этилизобутират не вступает в
присутствии этилата натрия в реакцию
автоконденсации, поскольку в продукте
конденсация отсутствует -водородные
атомы.
чевидно,
что этилизобутират не вступает в
присутствии этилата натрия в реакцию
автоконденсации, поскольку в продукте
конденсация отсутствует -водородные
атомы.
Конденсация Кляйзена может быть проведена между двумя сложными эфирами, но поскольку при этом возможно образование четырех различных продуктов, в результате реакции часто получают сложные смеси. Этого удается избежать, если один из сложных эфиров не содержит -водородных атомов и легко реагируется с карбанионом. Реакции в этом случае напоминают перекрестную альдольную конденсацию. К числу применимых для этой цели сложных эфиров, не содержащих -водородные атомы и обладающих высокой реакционной способностью относятся эфиры бензойной, муравьиной, щавелевой и угольной кислот.
Примеры:


 сложные
эфиры
сложные
эфиры
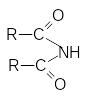 амиды
амиды