
Лекции / Лекция_40-41(б)
.DOC
Кето-енольная таутомерия эфиров 1,3-кетокислот
и реакции таутомерных форм.
Э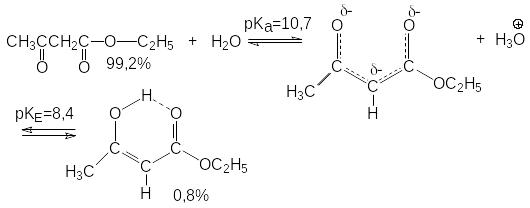 фиры
1,3-кетокислот по своему химическому
поведению близки к 1,3-дикетонам. Однако
их кислотность ниже. Для них характерна
кетоенольная таутомерия.
фиры
1,3-кетокислот по своему химическому
поведению близки к 1,3-дикетонам. Однако
их кислотность ниже. Для них характерна
кетоенольная таутомерия.
Как и в случае 1,3-дикетонов таутомерное равновесие чувствительно к сольватирующей способности реакционной среды. Так, в растворе метанола образуется 8,7% енола.
А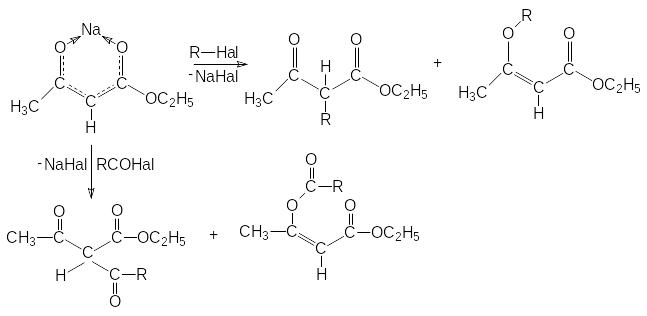 нионы
эфиров 1,3-кетокислот представляют собой
сопряженную систему с выровненными
связями и делокализованным отрицательным
зарядом. Они содержат несколько
реакционных центров. Их соли в растворах
существуют в виде ионных пар. С ионами
тяжелых металлов они образуют внутренние
комплексы (хелаты). Соли 1,3-кетокислот
подобны солям 1,3-дикетонов. Они легко
алкилируются и ацилируются
нионы
эфиров 1,3-кетокислот представляют собой
сопряженную систему с выровненными
связями и делокализованным отрицательным
зарядом. Они содержат несколько
реакционных центров. Их соли в растворах
существуют в виде ионных пар. С ионами
тяжелых металлов они образуют внутренние
комплексы (хелаты). Соли 1,3-кетокислот
подобны солям 1,3-дикетонов. Они легко
алкилируются и ацилируются
Алкилирование и ацилирование происходит главным образом у углеродного атома, т.к. атомы кислорода в значительной степени блокированы ионом металла.
Е сли
в полученных продуктах алкилирования
или ацилирования при атоме углерода в
положении 2 содержится еще один кислый
атом водорода открывается дополнительная
возможность введения в это положение
алкильных или ацильных групп, например
сли
в полученных продуктах алкилирования
или ацилирования при атоме углерода в
положении 2 содержится еще один кислый
атом водорода открывается дополнительная
возможность введения в это положение
алкильных или ацильных групп, например
П оследующий
гидролиз и нагревание приводит к синтезу
1,3-кетокарбоновой кислоты и соответствующего
кетона
оследующий
гидролиз и нагревание приводит к синтезу
1,3-кетокарбоновой кислоты и соответствующего
кетона
Эти реакции представляют собой важных синтетический метод получения кетонов различных структур.
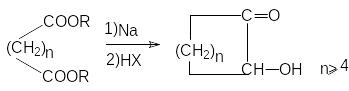
Ацилоиновая конденсация.
В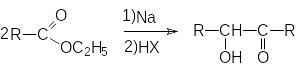 отличие от конденсации Кляйзена в
ацилоиновой конденсации ключевую роль
играют сложноэфирные группы. Суммарно
ацилоиновая конденсация может быть
представлена схемой:
отличие от конденсации Кляйзена в
ацилоиновой конденсации ключевую роль
играют сложноэфирные группы. Суммарно
ацилоиновая конденсация может быть
представлена схемой:
М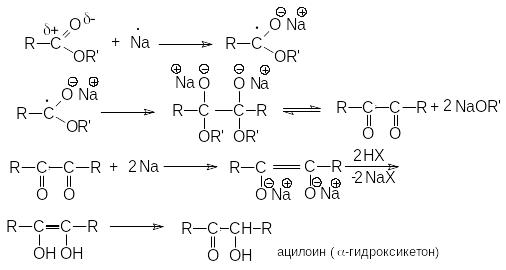 еханизм
ацилоиновой конденсации может быть
представлен последовательностью стадий:
еханизм
ацилоиновой конденсации может быть
представлен последовательностью стадий:
Реакция представляет собой важнейший метод образования углерод-углеродной связи. Она имеет большое значение для синтеза соединений с большими циклами.
Амиды карбоновых кислот
Э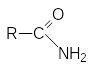 ти
соединения следует рассматривать как
результат замещения гидрокси-группы в
карбоновой кислоте на амино-группу
ти
соединения следует рассматривать как
результат замещения гидрокси-группы в
карбоновой кислоте на амино-группу
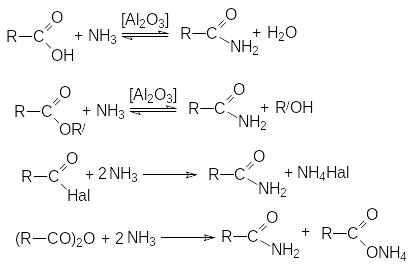
Методы получения амидов:
ацилирование аммиака и аминов.
Д
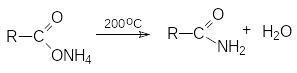 егидратация
аммониевых солей карбоновых кислот
егидратация
аммониевых солей карбоновых кислот
Гидролиз нитрилов карбоновых кислот
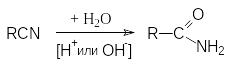
П
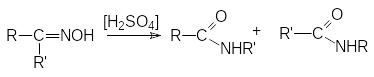 ерегруппировка
оксимов кетонов по Бекману
ерегруппировка
оксимов кетонов по Бекману
Обычно к атому азота мигрирует та группа, которая находится в транс-положении к ОН-группе.
Механизм перегруппировки Бекмана.
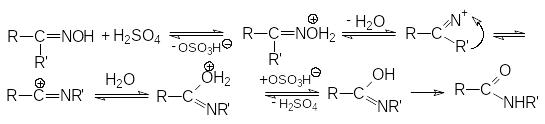
Синтез лактамов - циклических амидов.
П
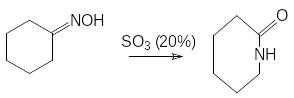 ерегруппировка
циклических амидов – лактамов
ерегруппировка
циклических амидов – лактамов
Реакция Байера-Виллигера

Циклизация аминокислот (n3)

Физические свойства амидов. Строение амидной группы.
Амиды представляют собой бесцветные кристаллические вещества или жидкости, растворяющиеся в органических растворителях. Амиды, в молекулах которых имеются связи N-H, ассоциированы вследствие образования межмолекулярных водородных связей и имеют более высокие температуры кипения.
В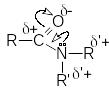 молекулах амидов имеет место значительное
сопряжение неподеленной парой электронов
азота и -электронной
системой двойной связи С=О. Это приводит
к образованию дополнительной поляризации
связей в амидной группе и наличие
электрофильных реакционных центров на
ацильном и алкильных углеродных атомах
и отрицательного - на карбонильном
кислороде.
молекулах амидов имеет место значительное
сопряжение неподеленной парой электронов
азота и -электронной
системой двойной связи С=О. Это приводит
к образованию дополнительной поляризации
связей в амидной группе и наличие
электрофильных реакционных центров на
ацильном и алкильных углеродных атомах
и отрицательного - на карбонильном
кислороде.
Химические свойства амидов.
Реакции нуклеофильного замещения.
Примером может служить гидролиз. В нейтральной среде гидролиз протекает медленно. Поэтому реакцию ведут в присутствии минеральной кислоты либо основания, которые не только ускоряют ее, но и участвуют как реагенты.
А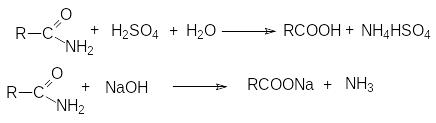
 ктивация
молекулы амида кислотой связана с ее
протонированием и увеличением
положительного заряда на карбонильном
углероде, который становится более
восприимчивым к последующей нуклеофильной
атаке:
ктивация
молекулы амида кислотой связана с ее
протонированием и увеличением
положительного заряда на карбонильном
углероде, который становится более
восприимчивым к последующей нуклеофильной
атаке:
В случае щелочного гидролиза в качестве нуклеофила вместо воды выступает более реакционно способный гидроксил-анион, который эффективно осуществляет нуклеофильную атаку на кaрбонильный углерод:
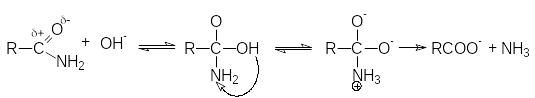
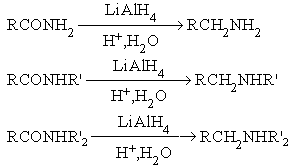
Реакция восстановления.
Р
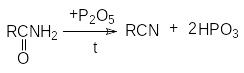 еакция
дегидратации.
еакция
дегидратации.
Расщепление по Гофману.
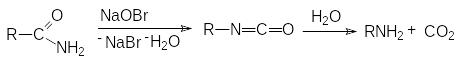
М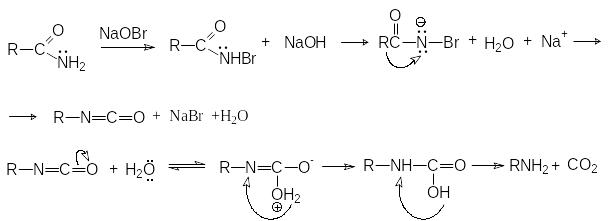 еханизм
реакции
еханизм
реакции
Перегруппировка Курциуса характерна для азидов карбоновых кислот, которые ведут себя подобно амидам в расщеплении по Гофману.
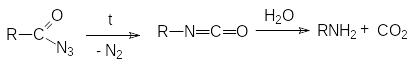
Взаимодействие формамидов с реактивом Гриньяра (реакция Буво)
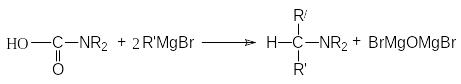
Продуктами этой реакции являются альдeгид и третичный амин.
Нитрилы карбоновых кислот.
Общая формула нитрилов R-CN или CnH2n+1CN.
Методы получения нитрилов.
Д
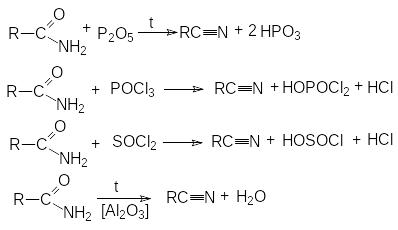 егидратация
амидов карбоновых кислот с помощью
водоотнимающих агентов.
егидратация
амидов карбоновых кислот с помощью
водоотнимающих агентов.
Н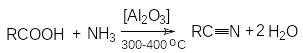 а
практике в последнем случае пропускают
над катализатором смесь карбоновой
кислоты с аммиаком. В этом процессе
совмещается образование амида и его
дегидратация.
а
практике в последнем случае пропускают
над катализатором смесь карбоновой
кислоты с аммиаком. В этом процессе
совмещается образование амида и его
дегидратация.
Н
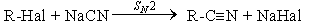 уклеофильное
замещение галогена в галогеналканах
на циaнид-анион.
уклеофильное
замещение галогена в галогеналканах
на циaнид-анион.
Д
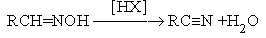 егидратация
альдоксимов.
егидратация
альдоксимов.
М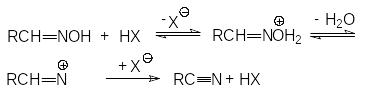 еханизм
реакции:
еханизм
реакции:
Химические свойства нитрилов.
Ц![]() иано-группа
характеризуется высокой степенью
поляризации, следствием которой является
образование частичного положительного
заряда на углероде и отрицательного
заряда – на азоте
иано-группа
характеризуется высокой степенью
поляризации, следствием которой является
образование частичного положительного
заряда на углероде и отрицательного
заряда – на азоте
Это обусловливает, с одной стороны, восприимчивость углеродного центра к нуклеофильной атаке, с другой – основность атома азота.
Реакции нуклеофильного присоединения.
Н итрилы
легко реагируют с сильными анионными
нуклеофильными реагентами (карбанионами,
амидами металлов, щелочами, алкоголятами,
тиоалкоголятами)
итрилы
легко реагируют с сильными анионными
нуклеофильными реагентами (карбанионами,
амидами металлов, щелочами, алкоголятами,
тиоалкоголятами)
П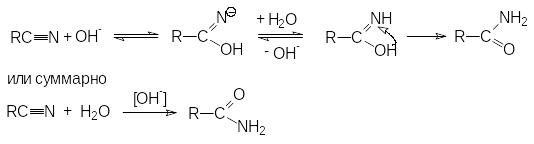 римером
может служить щелочной гидролиз нитрилов:
римером
может служить щелочной гидролиз нитрилов:
Дальнейший гидролиз амида приводит к образованию солей карбоновых кислот.

Таким образом суммарное уравнение щелочного гидролиза нитрилов можно представить как
R-CN + H2O + NaOH RCOONa + NH3
Р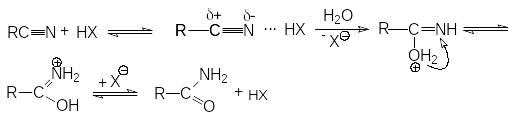 еакции
нитрилов со слабыми нуклеофилами (водой,
спиртами) протекает крайне медленно.
Для эффективного проведения этих реакций
используют кислотный катализ. Активация
молекулы нитрила в этом случае
осуществляется за счет образования
водородной связи между кислотой –
катализатором и атомом азота и, как
следствие, увеличение положительного
заряда на нитрильном углеродном атоме.
еакции
нитрилов со слабыми нуклеофилами (водой,
спиртами) протекает крайне медленно.
Для эффективного проведения этих реакций
используют кислотный катализ. Активация
молекулы нитрила в этом случае
осуществляется за счет образования
водородной связи между кислотой –
катализатором и атомом азота и, как
следствие, увеличение положительного
заряда на нитрильном углеродном атоме.
Н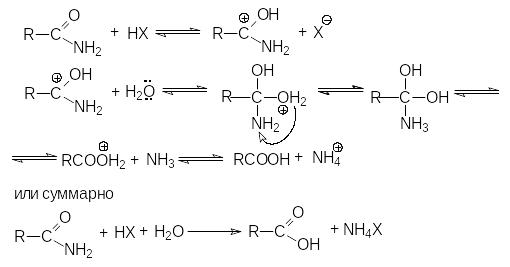 а
последующей стадии гидролиза кислота
НХ выступает одновременно как ускоритель
реакции и реагент.
а
последующей стадии гидролиза кислота
НХ выступает одновременно как ускоритель
реакции и реагент.
Таким образом, полный кислотный гидролиз нитрилов описывается уравнением:
R-CN + 2H2O + HX RCOOH + NH4X
Если в качестве реагента использовать водно-спиртовые среды, то можно осуществлять синтез сложных эфиров
R-CN + R'OH + H2O + HX RCOOR' + NH4X
Гидрирование.
Реакции гидрирования нитрилов можно подразделить на две группы:
а![]() )
каталитическое гидрирование
)
каталитическое гидрирование
В качестве катализаторов этих реакций используют металлические Pt, Pd, Ni.
б![]() )
реагентное гидрирование
)
реагентное гидрирование
В качестве реагентов этих реакциях используют LiAlH4, NaBH4.
Механизм реакции:
RCN + LiAlH4 RCH=N-Li + AlH3
RCH=N-Li + HX RCH=NH + LiX
Механизм второй стадии:

В
 заимодействие
с металлоорганическими соединениями.
заимодействие
с металлоорганическими соединениями.
Реакция Риттера.
Э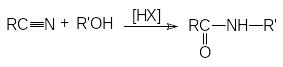 та
реакция является примером присоединения
атома углерода к гетероатому (азоту).
та
реакция является примером присоединения
атома углерода к гетероатому (азоту).
Р еакция
протекает по карбкатионному механизму:
еакция
протекает по карбкатионному механизму:
В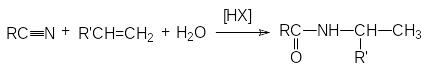 реакцию вступают только спирты, дающие
достаточно стабильные карбкатионы
(вторичные, третичные, бензильные и
т.п.). Первичные спирты не реагируют.
Карбкатионы не обязательно следует
генерировать из спирта, его можно
получать протонированием алкенов.
реакцию вступают только спирты, дающие
достаточно стабильные карбкатионы
(вторичные, третичные, бензильные и
т.п.). Первичные спирты не реагируют.
Карбкатионы не обязательно следует
генерировать из спирта, его можно
получать протонированием алкенов.
