
- •Химическая связь и взаимное влияние атомов
- •1. Электронная теория связи. Формулы Льюиса
- •2. Электронное строение и типы гибридизации атома углерода
- •Атомные орбитали
- •sp3-Гибридизация
- •Атом Сsp3 :
- •sp2-Гибридизация
- •sp-Гибридизация
- •Ацетилен
- •Основные характеристики химической связи
- •3. Делокализованная связь. Сопряжение
- •p Сопряжение
- •Резонансные структуры
- •Свойства соединений с делокализованными связями
- •2.Повышенная термодинамическая устойчивость, которая определяется энергией сопряжения (ЭС)
- •4. Циклические сопряженные системы Ароматичность
- •Электронное строение бензола
- •Ароматические гетероциклические соединения
- •Избыточные гетероциклы
- •Электронное строение пиридина
- •Ароматические гетероциклы с несколькими гетероатомами
- •4. Электронные эффекты
- •• Индуктивный эффект (I-эффект ) – это передача влияния заместителя по цепи связей
- •Мезомерный эффект (М-эффект) – это передача влияния заметителя по системе сопряженных связей
- •Направление влияния замеcтителей в сопряженной системе
- •5. Водородная связь
- •Влияние на физические свойства
- •Учебник, 2005г:

Основные характеристики химической связи
Связь |
|
Энергия, |
Длина, |
Дипольный |
Поляризуемость |
|
|
кДж/моль |
нм |
момент, |
(R – |
|
|
|
|
D |
молекулярная |
|
|
|
|
|
рефракция)* |
|
|
|
|
|
|
С-С |
|
348 |
0,154 |
0 |
1,29 |
|
|
|
|
|
|
С=С |
|
620 |
0,133 |
0 |
4,17 |
|
|
|
|
|
|
C≡C |
|
814 |
0,120 |
0 |
5,96 |
|
|
|
|
|
|
CSP3-H |
|
414 |
0,11 |
0,30 |
|
|
|
|
|
|
|
C-O |
|
344 |
0,143 |
0,86 |
1,5 |
|
|
|
|
|
|
C=O |
|
708 |
0,121 |
2,4 |
3,5 |
|
|
|
|
|
|
= +− |
∙ |
|
|
|
|
|
|
|
|
|
|
где n – показатель преломления- плотность
3. Делокализованная связь. Сопряжение
Сопряжение
CH2=CH-CH=CH2 CH2=CH-CH=O CH2=CH-C CH
CH
H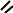







 H
H

 C C
C C






 H
H
H 





 C C
C C
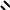
H 



 H
H
бутадиен-1,3
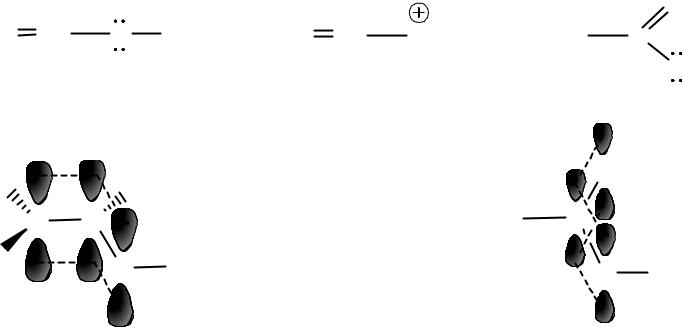
p Сопряжение
O
CH2 |
CH O CH |
CH2 |
CH CH |
CH |
3 |
C |
|
3 |
|
2 |
|
|
OH
H |
H |
O |
C |
C |
CH3 C |
H |
O CH3 |
O H |
метивиниловый эфир |
уксусная кислота |

Резонансные структуры
CH2=CH-CH2 
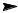 CH2-CH=CH2
CH2-CH=CH2
+1/2 |
+1/2 |
|||
CH2 |
|
CH |
|
CH2 |
|
|
|||
|
||||

Свойства соединений с делокализованными связями
1.Плоское строение, укорочение простых и удлиннение кратных связей по сравнению с их обычными величинами, так что порядок связи становится дробным.
2.Повышенная термодинамическая устойчивость, которая определяется энергией сопряжения (ЭС)
ЭС = Е CH2=CH-CH=CH2 |
Е CH2 |
|
CH |
|
CH |
|
CH2 = 15 кДж/моль |
|
|
|
3.Сдвиг полос поглощения в электронных спектрах в сторону больших длин волн. Вещества, содержащие длинную систему сопряженных связей, окрашены
Êàðî òèí (î ðàí æåâû é)
4. Циклические сопряженные системы Ароматичность
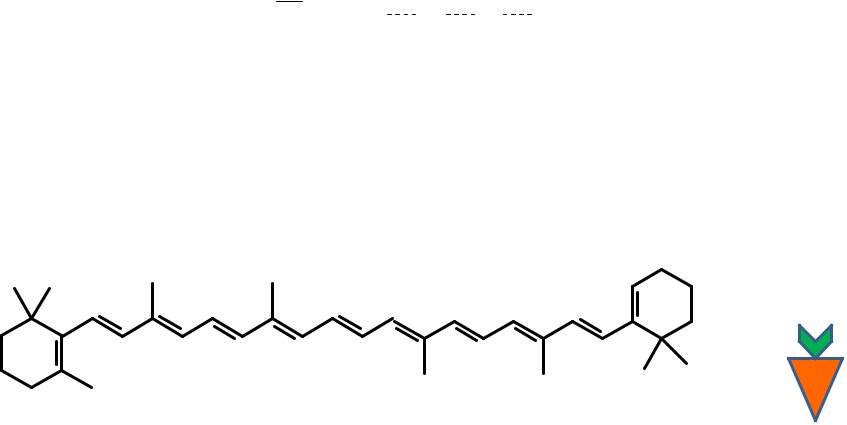
Правило Хюккеля
Ароматической является плоская циклическая замкнутая сопряженная система, число электронов в которой удовлетворяет формуле 4n + 2, где n = 0,1,2 ,3 …
Число |
4 |
6 |
8 |
электро н о в
í åàðî ì . |
аром. |
í åàðî ì . |
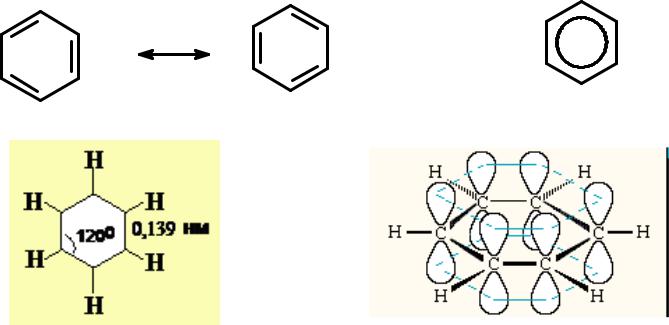
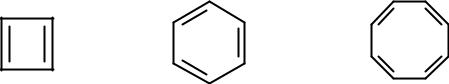
Электронное строение бензола
или
Энергия сопряжения –150 кДж/моль
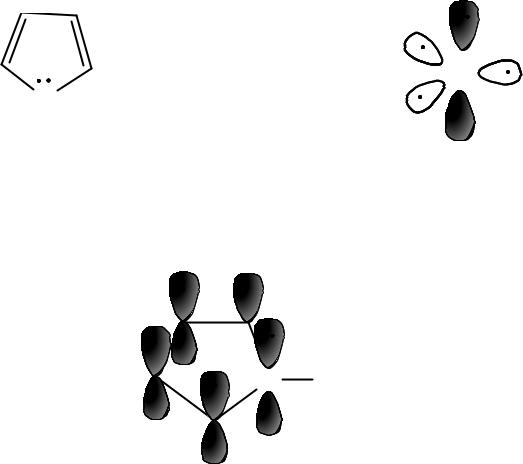
Ароматические гетероциклические соединения
|
pz |
|
|
sp2 |
|
N |
N |
sp2 |
sp2 |
|
|
H |
|
пиррол |
пиррольный атом N |
|
N H |
6 электронов |
-система пиррола
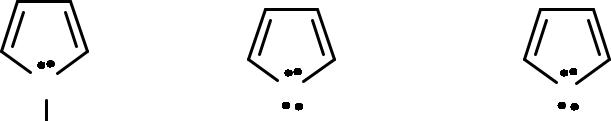
Избыточные гетероциклы
N |
O |
S |
H
Пиррол |
Фуран |
Тиофен |
