
- •1. Ферменты: определение понятия, химическая природа, физико-химические свойства и биологическая роль ферментов.
- •2. Изоферменты. Строение, биологическая роль, диагностическое значение определения, изменение в онтогенезе и при патологии органа, диагностическое значение.
- •5. Ингибирование активности ферментов, виды ингибирования: обратимое, необратимое, конкурентное, неконкурентное
- •6. Регуляция активности ферментов: неспецифическая, специфическая (понятия). Механизмы специфической регуляции активности ферментов
- •9. Энзимопатии: понятие, классификация, молекулярные причины возникновения и механизмы развития, последствия, биохимическая диагностика.
- •10. Энзимодиагностика: классификация ферментов клетки, крови в энзимодиагностике, диагностическое значение, применение в педиатрии
- •11. Биохимические основы энзимотерапии, применение ферментов в энзимотеравии (примеры)
- •12. Цикл Кребса - схема реакций, ферменты, коферменты, энергетический баланс одного оборота. Тканевые особенности в детском возрасте, Регуляция.
- •14. Механизмы сопряжения и разобщения дыхания и фосфорилирования, эндогенные и экзогенные разобщители.
- •15. Микросомальное биологическое окисление (система транспорта электронов, цитохромы р-450, в-5). Биологическое значение, регуляция, особенности активности ферментов в детском возрасте
- •21. Нормогликемия, пути превращения углеводов в клетках организма и ключевая роль глюкозо-б-фосфата.
- •23. Аэробный путь окисления глюкозы, тканевые особенности, энергетический баланс. Эффект Пастера, регуляция.
- •24. Катаболизм глюкозы по пентозофосфатному пути, биологическая роль. Регуляция значение пентозофосфатного пути в обеспечении метаболических процессов в организме человека
- •25. Гипогликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •26. Гипергликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •27. Контринсулярные гормоны (глюкагон, адреналин, кортизол): химическая природа, молекулярные механизмы участия в углеводном обмене.
- •29. Сахарный диабет инсулинзависимый (ИЗСД, I тип): биохимическая диагностика, механизмы развития метаболических нарушений (гипергликемия, холестеринемия, кетонемия, ацидоз, гликозилирование белков), биохимические особенности детского возраста
- •36. Липолиз триглицеридов в белой и бурой жировой ткани
- •37. Механизмы β - окисления жирных кислот. Регуляция
- •38. Пути обмена АцКоА. Кетоновые тела: биологическая роль, кетонемия, кетонурия, причины и механизмы развития, последствия, биохимические особенности детского возраста.
- •39. Обмен холестерина в организме человека. Регуляция синтеза холестерина
- •40. Атеросклероз: биохимические причины, факторы риска, лабораторная диагностика риска развития атеросклероза: обмена и развития его нарушений, гендерные особенности.
- •41. Роль белка в питании: состав и классификация пищевых белков, заменимые и незаменимые аминокислоты. Принципы нормирования белка в питании детей и взрослых. Азотистый баланс организма человека.
- •45. Причины токсичности аммиака и пути обезвреживания аммиака (образование глн, цикл мочевины, регуляция).
- •47. Регуляторные системы организма. Определение понятия – гормоны, принципы классификации гормонов.
- •48. Уровни и принципы организации нейро – эндокринной системы. Концепции обратной связи.
- •49. Рецепция и механизмы действия стероидных гормонов.
- •50. Рецепция и механизмы действия пептидных гормонов
- •55. Белки плазмы крови: классификация, диагностическое значение электрофореграмм.
- •57. Альбумины сыворотки крови: физико-химических свойства, функции, обмен
- •60. Гемоглобин: виды, строение, функции, обмен в норме. Метгемоглобинредуктазная система.
- •61. Биохимические функции почек, особенности метаболических процессов в почках.
- •63. Состав первичной и конечной мочи, физико – химические показатели в норме.
- •64. Химический состав мочи в норме и при патологии. Клиренс: понятие, виды.
- •65. Ренин-ангиотензин-альдостероновая система (РААС) в поддержании гомеостаза натрия. Механизм действия альдостерона на молекулярном уровне в почке и слюнных железах
- •66. Антидиуретический гормон и регуляция водного баланса организма.
- •67. Биохимические гомеостатические функции печени, биохимические особенности в детском возрасте.
- •68. Функциональные пробы и нагрузки характеризующие состояние углеводного, липидного, белкового обмена и детоксицирующей функции печени у детей. И взрослых.
- •70. Белки соединительной ткани коллаген и эластин: особенности аминокислотного состава и структурной организации молекул. Витамин С в синтезе коллагена.
- •74.Витамин Д – этапы образования активных форм, их метаболические функции, механизм действия. Роль печени, почек в обмене витамина Д, патохимические причины развития рахита, показатели кальций-фосфорного обмена при рахите на разных стадиях болезни.
- •75.Паратиреоидный гормон (ПГ) и кальцитонин (КГ) – химическая природа, стимулы секреции, механизмы действия в регуляции обмена кальция и ремоделирования костной ткани, проявления гипо- и гипертиреоза
- •76.Биохимические процессы в остеобластах и остеокластах в ремоделировании костной ткани.
- •77.Белковые и минеральные компоненты костной ткани
- •78.Биохимия нервной ткани: особенности химического состава, метаболических процессов, синтез нейромедиаторов.
- •80.Миокард: особенности метаболических процессов, метаболические нарушения при гипоксии, клиническая биохимическая энзимодиагностика при инфаркте миокарда
- •81.Биохимия лактации: физико – химические свойства, химический состав грудного молока, характеристика ферментов молока. Изменение химического состава в процессе лактации: виды женского молока
- •82.Биохимия лактации: биохимические механизмы образования органических компонентов молока в лактирующей железе, белок лактальбумин, роль гормонов (пролактин, окситоцин, плацентарного лактоген, эстрогены, СТГ, Т3, Т4, кортизол, инсулин)
- •83.Витамины: химическая природа, классификация по растворимости в воде и биохимическим механизмам действия. Провитамины и механизмы их активации (на примере провитаминов Д и А). Эндогенные и экзогенные причины гипо- , гипер- и авитаминозов
- •84.Витамины-коферменты РР, В2 участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •Симптомы гиповитаминоза
- •Симптомы гиповитаминоза
- •86.Витамины-коферменты В12, фолиевая кислота участие в метаболических процессах, биохимические проявления гиповитаминозов
- •87.Витамин С: участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •89.Буферные системы плазмы крови: гидрокарбонатная, фосфатная, белковая Гемоглобиновая буферная система эритроцитов, связь с гидрокарбонатной системой плазмы и эритроцита. Механизмы участия карбоангидразы в регуляции КОС.
- •90.Кислотно-основный гомеостаз: биологическое значение постоянства внутренней среды организма., механизмы поддержания КОС, особенности в детском возрасте.
- •91.Нарушения КОС - классификация по механизмам? Биохимические пути компенсации.
Образованная глюкозо-1-ф может включаться в: 1) синтез гликогена; 2) превращение в свободную глюкозу; 3) катаболизм, сопряжённый с синтезом АТФ, и т.д.
Нарушения метаболизма галактозы:
Галактоземия обусловлена наследственным дефектом одного из ферентов.
Недостаточность галактозо-1-фосфатуридилтрансферазы (ГАЛТ) особенно опасна для детей, так как материнское молоко, содержит лактозу. Ранние симптомы дефекта ГАЛТ: рвота, диарея, дегидратация, уменьшение массы тела, желтуха. В крови, моче и тканях повышается концентрация галактозы и галактозо-1-ф. В хрусталике глаза галактоза восстанавливается до образования галактитола. Он накапливается в стекловидном теле и связывает большое количество воды, что приводит к развитию катаракты, которая наблюдается уже через несколько дней после рождения.
Некоторые дефекты в строении ГАЛТ приводят лишь к частичной потере активности фермента. Поскольку в норме ГАЛТ присутствует в организме в избытке, то снижение его активности до 50%, а иногда и ниже может клинически не проявляться.
Лечение заключается в удалении галактозы из рациона.
21. Нормогликемия, пути превращения углеводов в клетках организма и ключевая роль глюкозо-б-фосфата.
Нормальное количество глюкозы в крови: 3,3-5,5.
Метаболизм моносахаридов в клетке:
После всасывания в кишечнике глюкоза и другие моносахариды поступают в воротную вену и далее в печень. Моносахариды в печени превращаются в глюкозу или продукты её метаболизма. Часть глюкозы в печени депонируется в виде гликогена, часть идет на синтез новых веществ, а часть через кровоток, направляется в другие органы и ткани. При этом печень поддерживает концентрацию глюкозы в крови на уровне 3,3-5,5 ммоль/л.
Роль глюкозо-6-фосфата:
Глюкозо-6-ф может использоваться клетке в различных превращениях, основными из которых являются: катаболизм с образованием АТФ, синтез гликогена, липидов, пентоз, полисахаридов и аминокислот.
32

22. Анаэробный гликолиз: понятие, этапы, общая схема, последовательность реакций, регуляция, энергетический
баланс. Регуляция гликолиза
Анаэробный гликолиз – это процесс окисления глюкозы до лактата, протекающий в отсутствии О2.
Анаэробный гликолиз отличается от аэробного только наличием последней 11 реакции, первые 10 реакций у них общие.
Этапы:
1)Подготовительный, в нем затрачивается 2 АТФ. Глюкоза фосфорилируется и расщепляется на 2 фосфотриозы;
2)2 этап сопряжён с синтезом АТФ. На этом этапе фосфотриозы превращаются в ПВК. Энергия этого этапа используется для синтеза 4 АТФ и восстановления 2НАДН2, которые в анаэробных условиях восстанавливают ПВК до лактата.
Энергетический баланс: 2АТФ = -2АТФ + 4АТФ
Общая схема:
Происходит окисление 1 глюкозы до 2 молекул молочной кислоты с образованием 2 АТФ (сначала 2 АТФ затрачиваются, затем 4 образуются). В анаэробных условиях гликолиз является единственным источником энергии. Суммарное уравнение: С6Н12О6 + 2Н3РО4 + 2АДФ → 2С3Н6О3 + 2АТФ + 2Н2О.
Реакции:
Общие реакции аэробного и анаэробного гликолиза
1)Гексокиназа в мышцах фосфорилирует в основном глюкозу, меньше – фруктозу и галактозу. Ингибитор глюкозо-6-ф, АТФ. Активатор адреналин. Индуктор инсулин.
Глюкокиназа фосфорилирует глюкозу. Активна в печени, почках. Не ингибируется глюкозо-6-ф. Индуктор инсулин.
|
|
|
H |
|
O |
|
|
|
Mg2+ |
H |
|
|
O |
|
||||||
|
|
|
|
C |
|
|
|
|
|
|
|
C |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
ÀÒÔ |
ÀÄÔ |
|
|
|
|
|
|
|
|
|
||
H |
C |
OH |
H |
C |
|
OH |
|
|||||||||||||
|
|
|
|
|
|
|||||||||||||||
HO |
|
C |
|
|
H |
|
|
|
|
HO |
|
C |
|
|
H |
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
H |
|
C |
|
|
OH |
ãåê ñî ê è í àçà |
|
H |
|
|
C |
|
|
OH |
|
|||||
|
|
|
|
|
|
|
|
|||||||||||||
H |
|
C |
|
|
OH |
ãë þ ê î ê è í àçà |
H |
|
C |
|
|
OH |
2- |
|||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
CH OH |
|
|
|
|
|
|
|
|
CH OPO |
|||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
2 |
3 |
||||
|
|
|
ãëþ êî çà |
|
|
|
|
|
ãëþ êî çî -6ô |
|
||||||||||
33
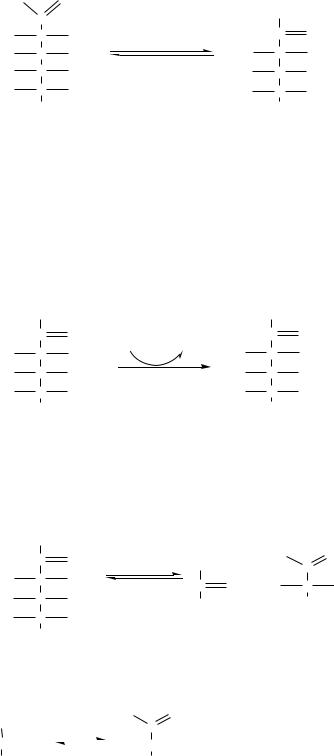
2)Фосфогексозоизомераза осуществляет альдо-кетоизомеризацию открытых форм гексоз.
|
H |
O |
|
|
|
|
|
|
|
|
|
|
CH OH |
|
|
|
C |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
H |
C |
OH |
|
|
C |
O |
|
|
|
|
|
|
|||
HO |
C |
H |
|
HO |
C |
H |
|
H |
C |
OH |
ф о сф о гек со зо и зо м ераза |
H |
C |
OH |
|
H |
C |
OH |
|
H |
C |
OH |
|
|
|
|
|
|
|||
|
CH OPO |
2- |
|
CH OPO |
2- |
||
|
|
|
|
||||
|
2 |
3 |
|
|
2 |
3 |
|
ãëþ êî çî -6ô |
|
|
ф рукто зо -6ф |
||||
3)Фосфофруктокиназа 1 осуществляет фосфорилирование фруктозы-6ф. Реакция необратима и самая медленная из всех реакций гликолиза, определяет скорость всего гликолиза. Активируется: АМФ, фруктозо- 2,6-дф, фруктозо-6-ф, Фн. Ингибируется: глюкагоном, АТФ, НАДН2, цитратом, жирными кислотами, кетоновыми телами. Индуктор реакции инсулин.
|
CH OH |
|
|
|
|
|
CH OPO |
2- |
||
|
|
|
|
|
|
|
||||
|
2 |
|
|
|
|
|
|
2 |
3 |
|
|
C |
O |
|
ÀÒÔ |
ÀÄÔ |
|
|
C |
O |
|
HO |
C |
H |
|
HO |
C |
H |
|
|||
|
|
2+ |
|
|||||||
|
|
|
|
|
Mg |
|
|
|
|
|
H |
C |
OH |
|
ô î ñô î фруктокиназа 1 |
H |
C |
OH |
|
||
|
|
|
|
|
|
|
|
|||
H |
C |
OH |
|
|
|
|
H |
C |
OH |
|
|
CH OPO |
2- |
|
|
|
|
CH OPO |
2- |
||
|
|
|
|
|
|
|
||||
|
2 |
3 |
|
|
|
|
2 |
3 |
||
|
ф рукто зо -6ф |
|
|
|
|
ф рукто зо -1,6-ф |
||||
4)Альдолаза А действует на открытые формы гексоз, образует несколько изоформ. В большинстве тканей содержится Альдолаза А. В печени и почках – Альдолаза В.
|
CH OPO |
2- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
2 |
3 |
|
|
|
|
|
|
|
|
|
C |
O |
|
|
|
2- |
H |
|
O |
|
|
|
CH OPO |
|
C |
|
|
||||
|
|
|
|
3 |
|
|
|
|||
|
|
|
|
|
2 |
|
|
|
||
HO |
C |
H |
|
C |
O |
+ |
H |
C |
OH |
|
|
|
|
|
|
||||||
H |
C |
OH |
Àë üäî ë àçà À |
CH OH |
|
|
CH OPO |
2- |
||
|
|
|
|
|
|
2 |
3 |
|||
|
|
|
|
|
2 |
|
|
|
|
|
H |
C |
OH |
|
ÄÀÔ |
|
|
3-ÔÃÀ |
|
||
|
CH OPO |
2- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
2 |
3 |
|
|
|
|
|
|
|
|
ôрукто зо -1,6-ô
5)Фосфотриозоизомераза.
CH OPO 2- |
|
|
|
|
H |
|
O |
|||||
|
|
|
|
|
|
C |
||||||
2 |
|
3 |
|
|
|
|
|
|
||||
C |
|
O |
|
|
|
|
|
H |
|
C |
|
OH |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|||||
CH2OH |
Òðè î çî ô î ñô àò- |
CH2OPO32- |
||||||||||
|
|
|
|
и зо м ераза |
|
|
|
|
||||
ÄÀÔ |
3-ÔÃÀ |
|
6)3-ФГА дегидрогеназа катализирует образование макроэргической связи в 1,3-ФГК и восстановление НАДН2.
34
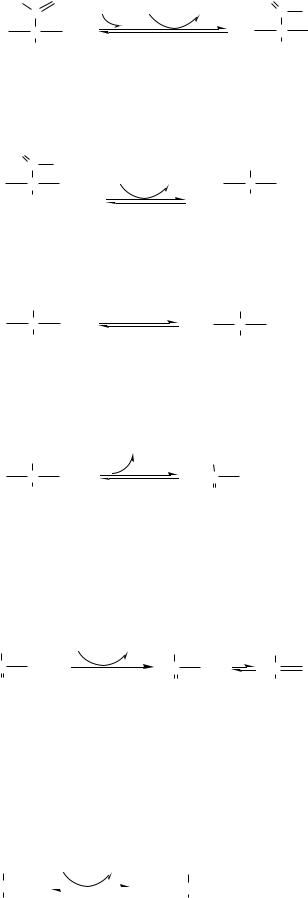
|
H |
O |
2Í |
ÐÎ |
|
+ |
2Í ÀÄÍ |
|
|
O |
|
|
|
|
|
|
4 |
2Í ÀÄ |
2 |
|
|
|
|
2- |
|||
|
C |
|
|
3 |
|
|
|
C |
OPO |
||||
|
|
|
|
|
|
|
|
|
3 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
||
2 H |
C |
OH |
|
|
|
|
|
|
2 H |
C |
OH |
|
|
|
CH OPO |
2- |
ÔÃÀ äåãè äðî ãåí àçà |
|
|
CH OPO |
2- |
||||||
|
|
|
|
3 |
|
||||||||
|
2 |
3 |
|
|
|
2 |
|
|
|||||
|
3-ÔÃÀ |
|
|
|
|
|
|
|
1,3-ÔÃÊ |
|
|
||
7) Фосфоглицераткиназа осуществляет субстратное фосфорилирование АДФ с образованием АТФ.
|
O |
|
|
2- |
|
|
|
|
|
|
|
C |
OPO |
|
|
COOH |
|
|
|||
|
3 |
2ÀÄÔ |
2ÀÒÔ |
|
|
|
||||
|
|
|
|
|
|
|
|
|||
2 H |
C |
OH |
|
|
2 H |
C |
OH |
|||
|
|
|
|
|||||||
|
CH OPO |
2- |
|
|
|
CH OPO |
2- |
|||
|
|
|
|
|
|
3 |
||||
|
2 |
3 |
|
|
|
|
|
2 |
|
|
|
1,3-ÔÃÊ |
|
|
ф о сф о гл и цератк и н аза |
3-ÔÃÊ |
|
|
|||
|
|
|
|
|
|
|
|
|||
8) Фосфоглицератмутаза осуществляет перенос фосфатного остатка в ФГК из положения 3 положение 2.
|
COOH |
|
|
|
COOH |
|
2 H |
C |
OH |
|
2 H |
C |
OPO 2- |
|
|
|
|
|
|
3 |
|
CH OPO |
2- |
ф о сф о гл и цератм утаза |
CH OH |
||
|
|
|||||
|
2 |
3 |
|
|
2 |
|
|
3-ÔÃÊ |
|
|
|
2-ÔÃÊ |
|
9) Енолаза отщепляет от 2-ФГК молекулу воды и образует высокоэнергетическую связь у фосфора. Ингибируется ионами F-.
|
|
|
|
2H O |
|
|
|
|
|
COOH |
|
|
2 |
|
|
|
|
|
|
|
2+ |
COOH |
|
|
||
|
|
|
2- |
Mg |
|
|
|
2- |
2 H |
C |
OPO |
2 |
C |
|
OPO |
||
3 |
|
3 |
||||||
|
|
|
|
|
|
|
||
|
CH OH |
|
Åí î ë àçà |
CH |
2 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
2-ÔÃÊ |
|
|
ÔÅÏ |
|
|
||
10) Пируваткиназа осуществляет субстратное фосфорилирование АДФ с образованием АТФ. Активируется фруктозо-1,6-дф, глюкозой. Ингибируется АТФ, НАДН2, глюкагоном, адреналином, аланином, жирными кислотами, Ацетил-КоА. Индуктор: инсулин, фруктоза.
COOH |
|
2ÀÄÔ |
2ÀÒÔ |
COOH |
|
COOH |
|||||
|
|
2+ |
|
||||||||
2 C |
OPO |
2- |
Mg |
|
2 C |
|
OH |
2 |
|
|
|
|
|
|
C |
|
O |
||||||
3 |
|
|
|
|
|||||||
CH2 |
|
|
П и руватк и н аза |
CH |
2 |
|
CH |
3 |
|||
ÔÅÏ |
|
|
|
|
|
|
|
||||
|
|
|
|
Ï |
ÂÊ (åí î ë) |
|
Ï |
ÂÊ (êåòî ) |
|||
Образующаяся енольная форма ПВК затем неферментативно переходит в более термодинамически стабильную кетоформу.
Реакция анаэробного гликолиза
11) Лактатдегидрогеназа. Стоит из 4 субъединиц, имеет 5 изоформ.
COOH |
2Í ÀÄÍ 2 2Í ÀÄ+ |
|
COOH |
||||||||
2 C |
|
O |
|
|
|
|
2 H |
|
C |
|
OH |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
||||||||
CH3 |
ËÄÃ |
|
|
|
CH3 |
||||||
Ï ÂÊ |
|
|
|
|
|
|
Лактат |
||||
35
