
- •1. Ферменты: определение понятия, химическая природа, физико-химические свойства и биологическая роль ферментов.
- •2. Изоферменты. Строение, биологическая роль, диагностическое значение определения, изменение в онтогенезе и при патологии органа, диагностическое значение.
- •5. Ингибирование активности ферментов, виды ингибирования: обратимое, необратимое, конкурентное, неконкурентное
- •6. Регуляция активности ферментов: неспецифическая, специфическая (понятия). Механизмы специфической регуляции активности ферментов
- •9. Энзимопатии: понятие, классификация, молекулярные причины возникновения и механизмы развития, последствия, биохимическая диагностика.
- •10. Энзимодиагностика: классификация ферментов клетки, крови в энзимодиагностике, диагностическое значение, применение в педиатрии
- •11. Биохимические основы энзимотерапии, применение ферментов в энзимотеравии (примеры)
- •12. Цикл Кребса - схема реакций, ферменты, коферменты, энергетический баланс одного оборота. Тканевые особенности в детском возрасте, Регуляция.
- •14. Механизмы сопряжения и разобщения дыхания и фосфорилирования, эндогенные и экзогенные разобщители.
- •15. Микросомальное биологическое окисление (система транспорта электронов, цитохромы р-450, в-5). Биологическое значение, регуляция, особенности активности ферментов в детском возрасте
- •21. Нормогликемия, пути превращения углеводов в клетках организма и ключевая роль глюкозо-б-фосфата.
- •23. Аэробный путь окисления глюкозы, тканевые особенности, энергетический баланс. Эффект Пастера, регуляция.
- •24. Катаболизм глюкозы по пентозофосфатному пути, биологическая роль. Регуляция значение пентозофосфатного пути в обеспечении метаболических процессов в организме человека
- •25. Гипогликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •26. Гипергликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •27. Контринсулярные гормоны (глюкагон, адреналин, кортизол): химическая природа, молекулярные механизмы участия в углеводном обмене.
- •29. Сахарный диабет инсулинзависимый (ИЗСД, I тип): биохимическая диагностика, механизмы развития метаболических нарушений (гипергликемия, холестеринемия, кетонемия, ацидоз, гликозилирование белков), биохимические особенности детского возраста
- •36. Липолиз триглицеридов в белой и бурой жировой ткани
- •37. Механизмы β - окисления жирных кислот. Регуляция
- •38. Пути обмена АцКоА. Кетоновые тела: биологическая роль, кетонемия, кетонурия, причины и механизмы развития, последствия, биохимические особенности детского возраста.
- •39. Обмен холестерина в организме человека. Регуляция синтеза холестерина
- •40. Атеросклероз: биохимические причины, факторы риска, лабораторная диагностика риска развития атеросклероза: обмена и развития его нарушений, гендерные особенности.
- •41. Роль белка в питании: состав и классификация пищевых белков, заменимые и незаменимые аминокислоты. Принципы нормирования белка в питании детей и взрослых. Азотистый баланс организма человека.
- •45. Причины токсичности аммиака и пути обезвреживания аммиака (образование глн, цикл мочевины, регуляция).
- •47. Регуляторные системы организма. Определение понятия – гормоны, принципы классификации гормонов.
- •48. Уровни и принципы организации нейро – эндокринной системы. Концепции обратной связи.
- •49. Рецепция и механизмы действия стероидных гормонов.
- •50. Рецепция и механизмы действия пептидных гормонов
- •55. Белки плазмы крови: классификация, диагностическое значение электрофореграмм.
- •57. Альбумины сыворотки крови: физико-химических свойства, функции, обмен
- •60. Гемоглобин: виды, строение, функции, обмен в норме. Метгемоглобинредуктазная система.
- •61. Биохимические функции почек, особенности метаболических процессов в почках.
- •63. Состав первичной и конечной мочи, физико – химические показатели в норме.
- •64. Химический состав мочи в норме и при патологии. Клиренс: понятие, виды.
- •65. Ренин-ангиотензин-альдостероновая система (РААС) в поддержании гомеостаза натрия. Механизм действия альдостерона на молекулярном уровне в почке и слюнных железах
- •66. Антидиуретический гормон и регуляция водного баланса организма.
- •67. Биохимические гомеостатические функции печени, биохимические особенности в детском возрасте.
- •68. Функциональные пробы и нагрузки характеризующие состояние углеводного, липидного, белкового обмена и детоксицирующей функции печени у детей. И взрослых.
- •70. Белки соединительной ткани коллаген и эластин: особенности аминокислотного состава и структурной организации молекул. Витамин С в синтезе коллагена.
- •74.Витамин Д – этапы образования активных форм, их метаболические функции, механизм действия. Роль печени, почек в обмене витамина Д, патохимические причины развития рахита, показатели кальций-фосфорного обмена при рахите на разных стадиях болезни.
- •75.Паратиреоидный гормон (ПГ) и кальцитонин (КГ) – химическая природа, стимулы секреции, механизмы действия в регуляции обмена кальция и ремоделирования костной ткани, проявления гипо- и гипертиреоза
- •76.Биохимические процессы в остеобластах и остеокластах в ремоделировании костной ткани.
- •77.Белковые и минеральные компоненты костной ткани
- •78.Биохимия нервной ткани: особенности химического состава, метаболических процессов, синтез нейромедиаторов.
- •80.Миокард: особенности метаболических процессов, метаболические нарушения при гипоксии, клиническая биохимическая энзимодиагностика при инфаркте миокарда
- •81.Биохимия лактации: физико – химические свойства, химический состав грудного молока, характеристика ферментов молока. Изменение химического состава в процессе лактации: виды женского молока
- •82.Биохимия лактации: биохимические механизмы образования органических компонентов молока в лактирующей железе, белок лактальбумин, роль гормонов (пролактин, окситоцин, плацентарного лактоген, эстрогены, СТГ, Т3, Т4, кортизол, инсулин)
- •83.Витамины: химическая природа, классификация по растворимости в воде и биохимическим механизмам действия. Провитамины и механизмы их активации (на примере провитаминов Д и А). Эндогенные и экзогенные причины гипо- , гипер- и авитаминозов
- •84.Витамины-коферменты РР, В2 участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •Симптомы гиповитаминоза
- •Симптомы гиповитаминоза
- •86.Витамины-коферменты В12, фолиевая кислота участие в метаболических процессах, биохимические проявления гиповитаминозов
- •87.Витамин С: участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •89.Буферные системы плазмы крови: гидрокарбонатная, фосфатная, белковая Гемоглобиновая буферная система эритроцитов, связь с гидрокарбонатной системой плазмы и эритроцита. Механизмы участия карбоангидразы в регуляции КОС.
- •90.Кислотно-основный гомеостаз: биологическое значение постоянства внутренней среды организма., механизмы поддержания КОС, особенности в детском возрасте.
- •91.Нарушения КОС - классификация по механизмам? Биохимические пути компенсации.
и все 3 активных центра, образованных парам α- и β-субъединиц, катализируют очередную фазу цикла: 1) связывание АДФ и Н3РО4; 2) образование фосфоангидридной связи АТФ; 3) освобождение конечного продукта АТФ.
14. Механизмы сопряжения и разобщения дыхания и фосфорилирования, эндогенные и экзогенные разобщители.
Сопряжения и разобщения окислительного фосфорилирования
Процесс окисления создает электрохимический потенциал, а процесс фосфорилирования его использует. Таким образом, электрохимический потенциал обеспечивает сопряжение процессов окисления и фосфорилирования.
Так как необходимый для сопряжения электрохимический потенциал создают I, III и IV комплексы дыхательной цепи, их называют пунктами сопряжения окисления и фосфорилирования.
Разобщение дыхания и фосфорилирования называют явление исчезновения на мембране электрохимического потенциала под действием разобщителей и прекращение синтеза АТФ.
Разобщителями являются вещества, которые могут переносить протоны или другие ионы через мембрану минуя каналы АТФ-синтетазы. В результате разобщения количество АТФ снижается, АДФ увеличивается, возрастает скорость потребления О2, окисления НАДН2, ФАДН2, а образовавшаяся свободная энергия выделяется в виде теплоты.
15. Микросомальное биологическое окисление (система транспорта электронов, цитохромы р-450, в-5). Биологическое значение, регуляция, особенности активности ферментов в детском возрасте
Микросомальное окисление - Катализируют низкоспецифичные реакции.
1) Цитохром Р450
Донор: НАДФН2.
Субстраты - гидрофобные вещества экзогенного (лекарства, ксенобиотики) и эндогенного (стероиды, жирные кислоты и т.д.) происхождения.
Регуляция активности: индукция синтеза ферментов.
22

Í ÀÄÔÍ |
|
Í |
ÀÄÔ |
+ |
Í |
2 |
Î |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
2 |
|
|
|
|
|
|
ROH |
RH |
||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
2Í |
+ |
+ Î |
2- |
|
Î |
|
||
ÔÀÄ |
|
|
|
|
2 |
|||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
e |
- |
|
|
|
|
|
|
ÔÌ |
Í |
|
|
|
|
|
|
|
öè òî ï ë àçì à |
|||
|
|
|
|
|
|
|
Fe |
2+/3+ |
||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ãë àäê è é ÝÏ Ð |
Í ÀÄÔ Í |
2 |
-редукт аза |
|
|
|
öè ò î õðî ì |
Ð |
|||||
|
|
|
|
|
|
|
|
|
|
|
450 |
|
НАДФН2-Р450 редуктаза. Содержит 2 домена: цитозольный (содержит 2 кофермента ФАД и ФМН), гидрофобный (фиксирует фермент в мембране). Переносит электроны с НАДФН2 на цитохром Р450.
Цитохром Р450 – передает 2 электрона на 1 атом молекулы кислорода, который превращается в О2-, при взаимодействии с 2 протонами О2- дает воду. Второй атом молекулы кислорода включается в субстрат RH, образуя
ROH.
2) Цитохром b5
Донор: НАДН2.
öè òî ï |
ë àçì à |
|
|
|
|
|
R--CH=CH--CO-SKoA |
|
||||||
|
|
|
|
|
|
|
|
|
Í |
Î |
|
Àëåí î èë-Êî À |
|
|
|
|
|
|
Í |
Î |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
2 |
|
|
|
|
||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R--CHOH-CH --CO-SKoA |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
Í ÀÄÍ |
2 Í |
+ |
2Í |
+ |
+ Î |
2- |
|
|
Î |
|
2- |
Î 2 |
|
|
ÀÄ |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
R--CH -CH --CO-SKoA |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
ÔÀÄ |
|
|
e |
- |
|
Fe |
2+/3+ |
|
e |
- |
|
стеаро ил-Ко А |
||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
FeS |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ãë àäê è é ÝÏ Ð |
|
Í ÀÄÍ |
-редукт аза |
|
öè ò |
î õðî ì |
b |
|
|
|
Десат ураза |
|
||||
2 |
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
НАДН2-цитохром b5 редуктаза. Содержит 2 домена: цитозольный (содержит ФАД), гидрофобный (фиксирует фермент в мембране). Переносит электроны с НАДН2 на цитохром b5.
Цитохром b5. Содержит 2 домена: цитозольный (содержит гем), гидрофобный (фиксирует фермент в мембране). Может передавать электроны на различные ферменты. Участвует в синтезе холестерина, плазминогенов и церамида.
Стеароил-КоА-десатураза – переносит электроны с цитохрома b5 на 1 атом кислород, при участии протонов этот кислород образует воду. Второй атом
23
кислорода включается стеариновую кислоту с образованием её оксиацила, который дегидрируется до олеиновой кислоты.
Регуляция активности: такая же как и в цитохроме Р450?
Биологическое значение: микросомальное окисление – первая фаза обезвреживания ксенобиотиков. В соединительной ткани монооксигеназы участвуют в гидроксилировании пролина в оксипролин в молекуле коллагена.
16. Реакции образования активных форм О2, значение в физиологии и патологии клетки, ферментативная и
неферментативная антиоксидантная защиты, особенности детского возраста
Реакции образования активных форм кислорода:
a.О2 + 1е- → О∙2
b.О∙2 +1е- → О2-2 он быстро протонируется с образованием перекиси водорода О2-2 + 2Н+ → Н2О2
c.Н2О2 + 1е- → НО∙ + ОН- ОН- протонируется с образованием воды ОН- + Н+ → Н2О
d.ОН∙ + 1е- → Н2О
1)Ферментативные:
Электроны, необходимые для образования АФК могут давать цепи переноса электронов. Утечка е- из ЦПЭ на кислород является основным путем образования АФК в большинстве клеток:
a.В цепи окислительного фосфорилирования Q принимая 1 е- превращается в свободный радикал семихинон НQ∙, который может непосредственно взаимодействовать с кислородом, образуя супероксидный анион-радикал: HQ· + O2 → Q+ О∙2 + H+;
b.В монооксигеназных реакциях е- с цитохрома Р450 переходит на кислород с образованием супероксидного анион-радикала, который иногда теряется с активного центра.
c.Аэробные дегидрогеназы (ФАД-зависимые оксидазы) переносят е- и Н+ с субстрата на кислород с образованием перекиси водорода. Примеры таких оксидаз — оксидазы аминокислот, супероксид дисмутаза, оксидазы, локализованные в пероксисомах.
2)Неферментативные:
24
Электроны, необходимые для образования АФК могут давать:
a.Металлы переменной валентности. Наличие в клетках Fe2+ или ионов других переходных металлов катализирует образования АФК. Например, в эритроцитах окисление иона железа гемоглобина способствует образованию супероксидного анион-радикала.
Hb(Fe2+) + O2 → MetHb(Fe3+) + О∙2
b.Радикалы. АФК, обмениваясь электроном, легко переходят друг в друга: О∙2 + Н2О2 → О2 + НО∙ + ОН-
Так же при гомолитическом разрыве связей под действием ионизирующего излучения. Этот процесс обычно происходит на поверхности тела - в коже.
Значение активных форм кислорода в физиологии клеток:
1)Иммунная система. АФК используются фагоцитарными клетками - тканевыми макрофагами, моноцитами и гранулоцитами крови для разрушения бактерий, вирусов и онкоклеток.
2)Поддержание гомеостаза.
3)Внутриклеточное пищеварение.
Значение активных форм кислорода в патологии клеток:
Вызывают повреждение белков, нуклеиновых кислот и липидов мембран клеток. Инактивируют многие ферменты. Могут повреждать ДНК. Нарушают физико-химические свойства мембран - проницаемость, рецепторная функция и работа мембранных белков. Повреждение барьера приводит к нарушению регуляции внутриклеточных процессов и тяжелым расстройствам клеточных функций. Часто вызывают гибель клеток, следовательно, ускоряют процесс старения организма.
Антиоксидантная защита:
Прооксиданты усиливают процессы свободно-радикального окисления. Это высокие концентрации кислорода, ферментные системы, ионы двухвалентного железа.
Антиоксиданты тормозят свободно-радикальное окисление. Они образуют ферментативную и неферментативную антиоксидантную систему.
1) Ферментативная антиоксидантная система
Ферменты, защищающие клетки от действия активных форм кислорода: супероксиддисмутаза, каталаза и глутатионпероксидаза.
25
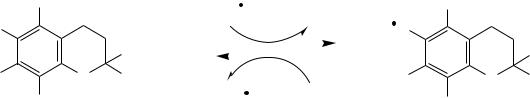
Органы, где их активность наивысшая: печень, надпочечники и почки (там особенно велико содержание митохондрий, цитохрома Р450 и пероксисом).
Супероксиддисмутаза: 2О∙2 + 2H+ → H2O2+ O2
Его (это же фермент. Он) изоферменты находятся и в цитозоле и в митохондриях и являются первой линией защиты.
Синтез этого фермента увеличивается, если в клетках активируется свободнорадикальное окисление.
Каталаза: 2Н2О2 → H2O+ O2
Находится в пероксисомах, в лейкоцитах и в эритроцитах.
Глутатионпероксидаза: Н2О2 + 2 GSH → 2 Н2О + G-S-S-G. (участвует глутатион. Видимо GSH – глутатион, а G-S-S-G – окисленный глутатион)
Кофермент: селен.
Глутатионредуктаза: GS-SG + НАДФН2 → 2 GSH + НАДФ+.
2) Неферментативная антиоксидантная система
"Липидные антиоксиданты" - производные фенола, способны инактивировать свободные радикалы в гидрофобном слое мембран и предотвращать развитие перекисного окисления липидов.
К ним относится витамин Е, коэнзим Q, тироксин и синтетические соединения.
Витамин Е самый распространённый, обеспечивает защиту мембран от свободно-радикального окисления. Отдаёт атом водорода радикалу липида ROO∙, восстанавливает его до гидропероксида (ROOH), а сам превращается в малоактивный свободный радикал, что прерывает перекисное окисление липидов:
|
CH3 |
ROO |
ROOH |
CH3 |
|
||||
HO |
|
|
|
||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
O |
CH3 |
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|||||
Фитил |
|
|
|
|
H3C |
O |
Фитил |
||
|
CH3 |
Í Î -àñêî ðáàò-Î |
Í Î -àñêî ðáàò-Î Í |
CH3 |
|
||||
|
Òî êî ô åðî ë |
|
|
|
|
|
|
То ко ф ерилрадикал |
|
(витамин Е = токоферол)
Регенерацию витамина Е осуществляет витамин С.
26
Витамин С ингибирует свободно-радикальное окисление с помощью двух механизмов:
a.Восстанавливает в мембранах витамин Е:
b.Взаимодействует с активными формами кислорода — О∙2, Н2О2, НО∙ и инактивирует их.
Соединения, связывающие железо. Большинство из них не просто связывают железо, но и не дают ему возможности приникнуть в липидную фазу мембран, поскольку образующиеся комплексы, в силу своей полярности, не проникают в гидрофобную зону.
17. Углеводы пищи и организма человека: классификация, биологические функции, принципы нормирования суточной
пищевой потребности для ребенка и взрослого
Углеводы – это многоатомные спирты содержащие оксогруппу.
Классификация:
1)По количеству мономеров:
a)Моносахариды
b)Дисахариды
c)Олигосахариды
d)Полисахариды
2)Моносахариды по положению оксогруппы:
a)Альдозы
b)Кетозы
3)Моносахариды по количеству атомов углерода:
a)Триозы
b)Тетрозы
c)Пентозы
d)Гексозы и т.д.
Биологические функции:
Моносахариды:
27
Энергетическая (образование АТФ;
Пластическая (образование ди-, олиго-, полисахаридов, аминокислот, липидов, нуклеотидов);
Детоксикационная (обезвреживание токсичных метаболитов и ксенобиотиков);
Фрагменты гликолипидов.
Дисахариды – у человека только лактоза. Она:
Источник глюкозы и галактозы для новорожденных;
Формирование нормальной микрофлоры у новорожденных.
Олигосахариды:
Фрагменты гликопротеинов, гликолипидов;
Образуют на поверхности клетки гликокаликс.
Полисахариды:
Гомополисахариды:
a)Запасающая (гликоген – форма хранения глюкозы).
Гетерополисахариды (ГАГ)
a)Структурный компонент межклеточного вещества;
b)Пролиферация и дифференцировка клеток;
c)Препятствуют свертыванию крови (гепарин).
Принципы нормирования суточной потребности для ребенка и взрослого:
75% массы пищевого рациона. 50% необходимых калорий.
У взрослого человека суточная потребность в углеводах 400г/сут, в целлюлозе и пектине до 10-15 г/сут.
Рекомендуется употреблять в пищу больше сложных полисахаридов и меньше моносахаров.
18. Механизмы переваривания в полости рта и желудочнокишечном тракте, характеристика и действие ферментов, участвующих в полостном и пристеночном пищеварении.
Переваривание углеводов в ротовой полости (полостное):
28
В ротовой полости пища измельчается при пережёвывании и смачивается слюной.
Слюна состоит на 99% из воды и обычно имеет рН 6,8.
Ферменты слюны: α-амилаза (расщепляет в крахмале внутренние α-1,4- гликозидные связи с образованием декстринов.
Переваривание углеводов в желудке (полостное):
В желудке рН <4. В нем прекращает действовать α-амилаза слюны. Однако, она сохраняется внутри пищевого комка.
Желудочный сок не содержит ферментов, в нем возможен лишь незначительный кислотный гидролиз гликозидных связей.
Переваривание углеводов в тонком кишечнике (полостное и пристеночное):
Двенадцатиперстная кишка: рН 7,5-8,0.
Ферменты: панкреатическая α-амилаза. Она гидролизует внутренние α-1,4- гликозидные связи в крахмале и декстринах с образованием мальтозы, изомальтозы и олигосахаридов.
Переваривание мальтозы, изомальтозы и олигосахаридов происходит под действием специфических ферментов - экзогликозидаз, образующих ферментативные комплексы.
Сахаразо-изомальтазный комплекс состоит из 2 пептидов: первый имеет изомальтазную субъединицу; второй - сахаразную. Сахаразная субъединица гидролизует α-1,2-гликозидные связи в сахарозе, изомальтазная - α-1,6- гликозидные связи в изомальтозе, α-1,4-гликозидные связи в мальтозе. Комплекса много в тощей кишке.
Гликоамилазный комплекс, содержит две субъединицы. Гидролизует α-1,4- гликозидные связи в олигосахаридах (с восстанавливающего конца) и в мальтозе. Наибольшая активность в нижних отделах тонкого кишечника.
β-Гликозидазный комплекс (лактаза) гидролизует β-1,4-гликозидные связи в лактозе. Активность лактазы зависит от возраста. У плода она особенно повышена в поздние сроки беременности и сохраняется на высоком уровне до 5-7-летнего возраста. Затем активность лактазы снижается.
Трегалаза гидролизует α-1,1-гликозидные связи между глюкозами в трегалозе.
29
Переваривание углеводов заканчивается образованием моносахаридов – в основном глюкозы, меньше образуется фруктозы и галактозы.
Всасывание углеводов
Моносахариды всасываются эпителиальными клетками тощей и подвздошной кишок. Транспорт моносахаридов в клетки слизистой оболочки кишечника может осуществляться путём диффузии (рибоза, ксилоза, арабиноза), облегчённой диффузии с помощью белков переносчиков (фруктоза, галактоза, глюкоза), и путем вторично-активного транспорта (галактоза, глюкоза). Вторично-активный транспорт галактозы и глюкозы из просвета кишечника в энтероцит осуществляется симпортом с Na+. Через белок-переносчик Na+ двигается по градиенту своей концентрации и переносит с собой углеводы против их градиента концентраций. Градиент концентрации Na+ создаётся Nа+/К+-АТФ-азой.
Скорость всасывания: галактоза > глюкоза > фруктоза > другие моносахариды.
Нарушение переваривания и всасывания углеводов:
Недостаточное переваривание и всасывание переваренных продуктов называют мальабсорбцией. В основе мальабсорбции углеводов могут быть причины двух типов:
1). Наследственные и приобретенные дефекты ферментов, участвующих в переваривании. Наследственные – дефекты ферментов. Приобретенные - при кишечных заболеваниях, после операций на ЖКТ.
2). Нарушение всасывания моносахаридов в кишечнике. Дефект компонента, участвующего в транспорте моносахаридов через мембраны.
19. Виды транспорта при всасывании моносахаридов, клеточные транспортеры глюкозы (ГЛЮТ 1-5), тканевая
локализация, регуляция активности.
Виды транспорта при всасывании моносахаридов:
Диффузия - рибоза, ксилоза
Облегчённая диффузия с помощью белков переносчиков - фруктоза, галактоза, глюкоза
Вторично-активный транспорт - галактоза, глюкоза. Симпорт с Na+.
Транспорт глюкозы из крови в клетки:
30
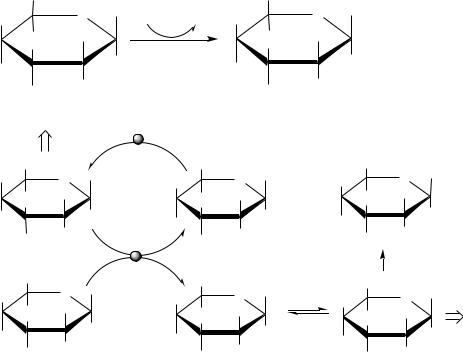
ГЛЮТЫ:
•ГЛЮТ-1 - преимущественно в мозге, плаценте, почках, толстом кишечнике;
•ГЛЮТ-2 - преимущественно в печени, почках, β-клетках поджелудочной железы, энтероцитах, есть в эритроцитах.
•ГЛЮТ-3 - во многих тканях, включая мозг, плаценту, почки. Обладает большим, чем ГЛЮТ-1, сродством к глюкозе;
•ГЛЮТ-4 - инсулинзависимый, в мышцах (скелетной, сердечной), жировой ткани;
•ГЛЮТ-5 - много в клетках тонкого кишечника, является переносчиком фруктозы.
20.Пути обмена галактозы в организме в норме, механизм развития галактоземии метаболические нарушения, биохимические и клинические ранние проявления в
период новорожденности.
Пути обмена галактозы в норме.
Галактоза образуется в кишечнике в результате гидролиза лактозы. Превращение галактозы в глюкозу происходит в печени.
|
CH2OH |
|
|
|
|
CH2OH |
|
|
|
OH |
|
O |
ÀÒÔ |
ÀÄÔ |
OH |
O |
|
|
|
|
|
|
Mg2+ |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
OH |
|
Галактокиназа |
OH |
|
|
|
||
|
|
OH |
|
OPO3H2 |
|
|
|||
|
|
OH |
|
|
|
|
OH |
|
|
|
галакто за |
|
|
|
галакто зо -1ф |
|
|
||
|
гликоген |
эпимераза |
|
|
|
|
|
||
|
CH OH |
|
|
|
CH OH |
CH2OH |
|
|
|
|
2 |
|
|
|
2 |
|
|
|
|
|
O |
|
|
OH |
|
O |
OH |
O |
|
|
OH |
|
|
|
OH |
|
OH |
|
|
OH |
|
O-ÓÄÔ |
|
|
|
O-ÓÄÔ |
|
|
OH |
|
OH |
|
|
|
|
OH |
|
OH |
|
ÓÄÔ-ãëþ êî çà |
|
УДФ-галакто за |
глюкоза |
|
|||||
|
|
|
|
галактозо-1ф-уридилтрансфераза |
|
|
|||
|
CH2OH |
|
|
|
CH2OH |
CH OPO H |
2 |
||
|
O |
|
|
|
|
|
2 |
3 |
|
OH |
|
|
OH |
|
O |
OH |
O |
|
|
|
|
|
|
|
|||||
|
OH |
OPO3H2 |
|
|
OH |
|
OH |
|
гликолиз |
|
|
|
|
|
OPO3H2 |
|
|
OH |
|
|
OH |
|
|
|
|
OH |
|
OH |
|
галакто зо -1ф |
|
|
|
|
|
||||
|
|
ãëþ êî çî -1ô |
ãëþ êî çî -6ô |
|
|||||
|
|
|
|
|
|
|
|
||
31
