
- •1. Ферменты: определение понятия, химическая природа, физико-химические свойства и биологическая роль ферментов.
- •2. Изоферменты. Строение, биологическая роль, диагностическое значение определения, изменение в онтогенезе и при патологии органа, диагностическое значение.
- •5. Ингибирование активности ферментов, виды ингибирования: обратимое, необратимое, конкурентное, неконкурентное
- •6. Регуляция активности ферментов: неспецифическая, специфическая (понятия). Механизмы специфической регуляции активности ферментов
- •9. Энзимопатии: понятие, классификация, молекулярные причины возникновения и механизмы развития, последствия, биохимическая диагностика.
- •10. Энзимодиагностика: классификация ферментов клетки, крови в энзимодиагностике, диагностическое значение, применение в педиатрии
- •11. Биохимические основы энзимотерапии, применение ферментов в энзимотеравии (примеры)
- •12. Цикл Кребса - схема реакций, ферменты, коферменты, энергетический баланс одного оборота. Тканевые особенности в детском возрасте, Регуляция.
- •14. Механизмы сопряжения и разобщения дыхания и фосфорилирования, эндогенные и экзогенные разобщители.
- •15. Микросомальное биологическое окисление (система транспорта электронов, цитохромы р-450, в-5). Биологическое значение, регуляция, особенности активности ферментов в детском возрасте
- •21. Нормогликемия, пути превращения углеводов в клетках организма и ключевая роль глюкозо-б-фосфата.
- •23. Аэробный путь окисления глюкозы, тканевые особенности, энергетический баланс. Эффект Пастера, регуляция.
- •24. Катаболизм глюкозы по пентозофосфатному пути, биологическая роль. Регуляция значение пентозофосфатного пути в обеспечении метаболических процессов в организме человека
- •25. Гипогликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •26. Гипергликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •27. Контринсулярные гормоны (глюкагон, адреналин, кортизол): химическая природа, молекулярные механизмы участия в углеводном обмене.
- •29. Сахарный диабет инсулинзависимый (ИЗСД, I тип): биохимическая диагностика, механизмы развития метаболических нарушений (гипергликемия, холестеринемия, кетонемия, ацидоз, гликозилирование белков), биохимические особенности детского возраста
- •36. Липолиз триглицеридов в белой и бурой жировой ткани
- •37. Механизмы β - окисления жирных кислот. Регуляция
- •38. Пути обмена АцКоА. Кетоновые тела: биологическая роль, кетонемия, кетонурия, причины и механизмы развития, последствия, биохимические особенности детского возраста.
- •39. Обмен холестерина в организме человека. Регуляция синтеза холестерина
- •40. Атеросклероз: биохимические причины, факторы риска, лабораторная диагностика риска развития атеросклероза: обмена и развития его нарушений, гендерные особенности.
- •41. Роль белка в питании: состав и классификация пищевых белков, заменимые и незаменимые аминокислоты. Принципы нормирования белка в питании детей и взрослых. Азотистый баланс организма человека.
- •45. Причины токсичности аммиака и пути обезвреживания аммиака (образование глн, цикл мочевины, регуляция).
- •47. Регуляторные системы организма. Определение понятия – гормоны, принципы классификации гормонов.
- •48. Уровни и принципы организации нейро – эндокринной системы. Концепции обратной связи.
- •49. Рецепция и механизмы действия стероидных гормонов.
- •50. Рецепция и механизмы действия пептидных гормонов
- •55. Белки плазмы крови: классификация, диагностическое значение электрофореграмм.
- •57. Альбумины сыворотки крови: физико-химических свойства, функции, обмен
- •60. Гемоглобин: виды, строение, функции, обмен в норме. Метгемоглобинредуктазная система.
- •61. Биохимические функции почек, особенности метаболических процессов в почках.
- •63. Состав первичной и конечной мочи, физико – химические показатели в норме.
- •64. Химический состав мочи в норме и при патологии. Клиренс: понятие, виды.
- •65. Ренин-ангиотензин-альдостероновая система (РААС) в поддержании гомеостаза натрия. Механизм действия альдостерона на молекулярном уровне в почке и слюнных железах
- •66. Антидиуретический гормон и регуляция водного баланса организма.
- •67. Биохимические гомеостатические функции печени, биохимические особенности в детском возрасте.
- •68. Функциональные пробы и нагрузки характеризующие состояние углеводного, липидного, белкового обмена и детоксицирующей функции печени у детей. И взрослых.
- •70. Белки соединительной ткани коллаген и эластин: особенности аминокислотного состава и структурной организации молекул. Витамин С в синтезе коллагена.
- •74.Витамин Д – этапы образования активных форм, их метаболические функции, механизм действия. Роль печени, почек в обмене витамина Д, патохимические причины развития рахита, показатели кальций-фосфорного обмена при рахите на разных стадиях болезни.
- •75.Паратиреоидный гормон (ПГ) и кальцитонин (КГ) – химическая природа, стимулы секреции, механизмы действия в регуляции обмена кальция и ремоделирования костной ткани, проявления гипо- и гипертиреоза
- •76.Биохимические процессы в остеобластах и остеокластах в ремоделировании костной ткани.
- •77.Белковые и минеральные компоненты костной ткани
- •78.Биохимия нервной ткани: особенности химического состава, метаболических процессов, синтез нейромедиаторов.
- •80.Миокард: особенности метаболических процессов, метаболические нарушения при гипоксии, клиническая биохимическая энзимодиагностика при инфаркте миокарда
- •81.Биохимия лактации: физико – химические свойства, химический состав грудного молока, характеристика ферментов молока. Изменение химического состава в процессе лактации: виды женского молока
- •82.Биохимия лактации: биохимические механизмы образования органических компонентов молока в лактирующей железе, белок лактальбумин, роль гормонов (пролактин, окситоцин, плацентарного лактоген, эстрогены, СТГ, Т3, Т4, кортизол, инсулин)
- •83.Витамины: химическая природа, классификация по растворимости в воде и биохимическим механизмам действия. Провитамины и механизмы их активации (на примере провитаминов Д и А). Эндогенные и экзогенные причины гипо- , гипер- и авитаминозов
- •84.Витамины-коферменты РР, В2 участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •Симптомы гиповитаминоза
- •Симптомы гиповитаминоза
- •86.Витамины-коферменты В12, фолиевая кислота участие в метаболических процессах, биохимические проявления гиповитаминозов
- •87.Витамин С: участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •89.Буферные системы плазмы крови: гидрокарбонатная, фосфатная, белковая Гемоглобиновая буферная система эритроцитов, связь с гидрокарбонатной системой плазмы и эритроцита. Механизмы участия карбоангидразы в регуляции КОС.
- •90.Кислотно-основный гомеостаз: биологическое значение постоянства внутренней среды организма., механизмы поддержания КОС, особенности в детском возрасте.
- •91.Нарушения КОС - классификация по механизмам? Биохимические пути компенсации.
84.Витамины-коферменты РР, В2 участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
ВИТАМИН В2 (РИБОФЛАВИН).
Структура. В основе лежит изоаллоксазин, соединённый со спиртом рибитолом.
|
|
|
|
O |
|
|
|
H C |
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
изо алло ксазин |
H C |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
3 |
N |
|
|
N |
|
|
|
|
|
|
|
|
|
||
H C |
H |
H |
H |
CH |
OH |
рибито л |
|
C |
C |
C |
|||||
|
2 |
|
|
|
2 |
|
|
|
|
OH OH OH |
|
|
|
||
Âè òàì è í |
 |
(ðè áî ô ë àâè í ) |
|
||||
|
2 |
|
|
|
|
|
|
Физико-химические свойства. Кристаллы желтого цвета, слаборастворимые в воде.
Главные источники витамина В2 — печень, почки, яйца, молоко, дрожжи. Витамин содержится также в шпинате, пшенице, ржи. Частично человек получает витамин В2 как продукт жизнедеятельности кишечной микрофлоры.
СуточнаяпотребностьввитаминеВ2 взрослого человека составляет 1,8—2,6 мг.
Активация. В слизистой оболочке кишечника после всасывания витамина происходит образование коферментов ФМН и ФАД по схеме:
ÀÒÔ |
ÀÄÔ |
|
ÀÒÔ |
ÔÔí |
Рибо ф лавин |
ÔÌ Í |
|
ÔÀÄ |
|
Рибо ф лавин кин аза |
Ф М Н -аден или лт ран сф ераза |
|||
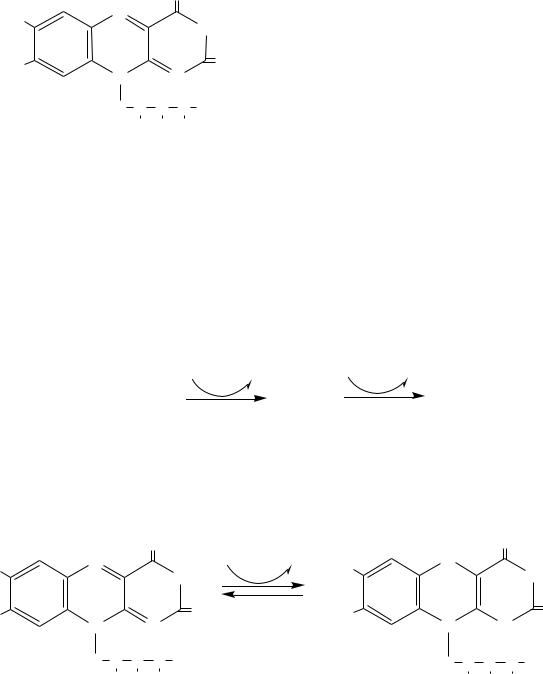
Биологические функции. Коферменты ФАД и ФМН входят в состав аэробных и анаэробных дегидрогеназ, принимающих участие в окислительно-восстановительных реакциях (реакции окислительного фосфорилирования, СДГ, оксидазы АК, ксантионоксидаза, альдегидоксидаза и т.д.).
|
|
|
|
O |
Сукцин ат Фум арат |
H |
|
|
O |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||||
H C |
N |
|
|
|
|
|
|
H C |
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
3 |
|
|
|
|
NH |
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H C |
|
|
|
|
O |
|
ÑÄÃ |
H C |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
3 |
N |
|
|
N |
|
|
3 |
N |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H C |
H |
H |
H |
CH OPO H |
|
|
|
H |
H |
H |
|
|
||
C |
C |
C |
|
|
H C |
CH OPO H |
||||||||
2 |
|
C |
C |
C |
||||||||||
2 |
|
|
|
2 |
3 |
|
||||||||
|
|
|
|
|
|
|
|
|
2 |
|
|
|
2 |
3 |
|
|
OH OH OH |
|
|
|
|
|
OH OH OH |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
ÔÌ |
Í |
|
|
|
|
|
|
|
ÔÌ |
Í Í |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
Симптомы гиповитаминоза
При пониженном содержании или отсутствии в пище рибофлавина развивается гипорибофлавиноз, а затем ариболфавиноз.
При гиповитаминозе В2 отмечается:
255
снижение аппетита, падение массы тела
слабость
головная боль, чувство жжения кожи
резь в глазах, нарушение сумеречного зрения
болезненность в углах рта и на нижней губе При развитии заболевания:
трещины и корочки в углах рта (угловой стоматит)
воспаления слизистой ротовой и языка
себорейный дерматит носа, губных складок
поражения кожи, дерматиты, выпадение волос
расстройства пищеварения
изменение роговицы, повышение чувствительности к свету, конъюктивит, блефарит
головокружения, бессонница, замедленная умственная реакция
задержка роста
Дефицит рибофлавина, прежде всего, отражается на тканях, богатых капиллярами и мелкими сосудами (ткань мозга). При дефиците частым проявлением может быть церебральная недостаточность разной степени выраженности, проявляющаяся ощущением общей слабости, головокружением, снижением тактильной и болевой чувствительности, повышением сухожильных рефлексов и др.
Недостаток рибофлавина может также приводить к нарушению усвоения железа и ослаблять щитовидную железу.
ВИТАМИН РР (НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
Структура
COOH |
CONH |
|
2 |
N |
N |
Н ико тин о вая кисло та |
Í èêî òèí àì èä |
Âè òàì è í |
ÐÐ |
Физико-химические свойства. Плохо растворим в воде, хорошо - в щелочах.
Источники. Витамина РР много в растительных продуктах, в рисовых и пшеничных отрубях, дрожжах, в печени и почках крупного рогатого скота и свиней. Витамин РР может образовываться из триптофана (из 60 молекул триптофана может образоваться 1 молекула НАД), что снижает потребность в витамине РР при увеличении количества триптофана в пище.
Суточная потребность в этом витамине составляет для взрослых 15-25мг, для детей — 15 мг.
Активация
ФРПФ |
ФФн |
АТФ |
ФФн АТФ |
АДФ |
|
Никотинамид |
никотинамидмононуклеотид |
НАД |
+ |
+ |
|
|
НАДФ |
||||
никотинамидмононуклеотид |
НАД-пирофосфорилаза НАД-киназа |
||||
пирофосфорилаза |
|
|
|
|
|
Биологические функции. Никотиновая кислота в организме в составе НАД и НАДФ выполняет функции коферментов различных анаэробных дегидрогеназ.
Нарушение обмена. Авитаминоз витамина РР приводит к заболеванию «пеллагра» (шершавая кожа), для которого характерны 3 основных признака: дерматит, диарея и деменция («три Д»). Пеллагра проявляется в виде симметричного дерматита на участках кожи, доступных действию солнечных лучей, расстройств ЖКТ (диарея) и воспалительных поражений слизистых оболочек рта и языка (стоматиты, гингивиты). Расстройства ЦНС проявляются в виде головной
256
боли, головокружений, повышенной раздражимости, в тяжелых случаях в виде деменции (потеря памяти, галлюцинации и бред).
85.Витамины-коферменты В1, В6 участие в метаболических процессах, биохимические механизмы проявления
|
|
|
|
|
гиповитаминозов |
||
ВИТАМИН B1 (ТИАМИН) |
|
|
|
|
|
||
Структура тиамина включает пиримидиновое и тиазоловое кольца, соединённые |
|||||||
метановым мостиком. |
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
- |
|
|
|
|
|
|
Cl |
|
|
H |
+ |
|
|
|
||
N |
C |
2 |
N |
CH |
|
|
|
|
|
|
|||||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
C |
2 |
CH OH |
|
|
|
|
|
|
||
H C |
|
|
|
|
|
|
2 |
3 |
N |
|
|
|
S |
|
|
|
|
|
|
|
|
||
|
Витамин В |
1 |
(тиамин) |
|
|
||
|
|
|
|
|
|
|
|
Физико-химические свойства. Водорастворим, разрушается при термической обработке.
Источники. Тиамин широко распространён в продуктах растительного происхождения (оболочка семян хлебных злаков и риса, горох, фасоль, соя и др.). В организмах животных содержится преимущественно в виде тиаминпирофосфата.
Суточная потребность взрослого человека в среднем составляет 2-3 мг витамина В1. Преобладание углеводов в пище повышает потребность организма в витамине; жиры, наоборот, резко уменьшают эту потребность.
Активация. При участии тиаминкиназы и АТФ в печени, почках, мозге и сердечной мышце витамин В1 превращается в кофермент тиаминпирофосфат (ТПФ).
|
NH |
2 |
|
|
|
|
|
|
NH |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
H |
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
H |
2 |
+ |
|
|
ÀÒÔ |
ÀÌ Ô |
|
|
2 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
N |
|
C |
N |
CH |
|
|
|
|
|
|
|
|
||||||
N |
|
C |
N |
CH |
3 |
|
|
|
|
3 |
|
|
|
O |
|
O |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
H |
|
|
|
|||||
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
2 |
C |
2 |
O |
P |
O |
P |
OH |
||
|
|
|
|
|
C |
2 |
CH OH |
H C |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H C |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
N |
|
|
|
|
S |
|
|
|
|
O |
|
O |
|
|
3 |
N |
|
|
|
S |
|
Òè àì èí êèí àçà |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Âè òàì è í |
 (òè àì è í ) |
|
Òè àì è í |
äè ô î ñô àò (ÒÏ Ô) |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Биологическая роль витамина В1 нетоксичен, в виде ТПФ входит в состав:
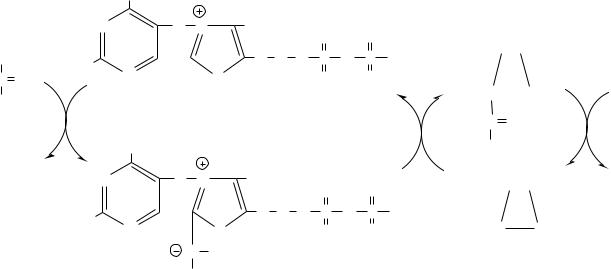
1.пируватдегидрогеназного комплекса (ПВК→ Ацетил-КоА);
2.α-кетоглутаратдегидрогеного комплекса (α-КГ→ Сукцинил-КоА);
3.транскетолаз ПФШ (перенос альдегида с кетосахара на альдосахар)
ТПФ забирает у субстрата группу и передает ее на липоевую кислоту:
257
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
C |
2 |
N |
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
O |
|
O |
|
|
||
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|
|
|
Лип о евая кисло та |
||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
||||||
COOH |
|
|
|
|
|
|
|
|
C |
C |
2 |
O |
P |
O |
P |
OH |
|
||||
H C |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
O |
3 |
N |
|
|
|
|
|
|
S |
|
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH |
|
|
|
|
Òè àì è í ï |
è ðî ô î ñô àò (ÒÏ Ô) |
|
|
S |
SH |
|||||||||||
3 |
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
O |
|
|
|
NH |
|
П И РУВАТДЕГИ ДРО ГЕН АЗА |
|
|||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
3 |
|
CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
N |
|
C |
2 |
N |
CH |
|
|
|
|
|
|
|
|
|
Лип о евая кисло та |
|||
|
|
|
|
|
3 |
|
|
|
|
O |
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
H |
H |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
C |
2 |
C |
2 |
O |
P |
O |
P |
OH |
|
||
|
|
H C |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
N |
|
|
|
|
|
|
S |
|
|
|
|
|
|
O |
|
O |
S |
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
C |
OH |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
CH |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ãè äðî ê ñè ýòè ë-ÒÏ Ô |
|
|
|
|
|
|
|
|
||||||||
Симптомы гиповитаминоза
При полном авитаминозе B1 развивается болезнь бери-бери: в организме нарушается углеводный обмен, и накапливаются молочная и пировиноградная кислоты. При этом наблюдаются поражения нервной системы (полиневриты, которые могут оканчиваться параличами), сердечной мышцы (она теряет способность эффективно сокращаться, сердце больного увеличивается, учащается пульс), пищеварительного тракта (снижается аппетит, появляются запоры). У больных наблюдается резкое общее истощение, распространенный или частичный отек.
Первичными признаками развивающегося гиповитаминоза B1 являются:
Со стороны нервной системы:
повышенная раздражительность, ощущение внутреннего беспокойства, плаксивость,
депрессия,
бессонница (временами стойкая),
снижение памяти,
онемение рук и ног,
боли,
зуд,
ухудшение координации,
зябкость при комнатной температуре,
нарушение функций мозга,
повышенная умственная и физическая утомляемость;
синдром Вернике-Корсакова (присущий больным, страдающим алкоголизмом).
Со стороны пищеварительной системы:
снижение аппетита,
ощущение тяжести или жжения в подложечной области,
тошнота,
запоры,
диарея,
потеря веса,
увеличение печени.
Со стороны сердечно-сосудистой системы:
одышка даже при небольшой физической нагрузке,
тахикардия,
артериальная гипотония,
острая сердечно-сосудистая недостаточность (может развиться в некоторых случаях при отсутствии своевременной диагностики и назначения лечения).
258
Дефицит витамина В1 в сыворотке крови встречается у 25% больных СПИДом. Хронический дефицит тиамина у больных СПИДом ведет к появлению различных неврологических симптомов, приводит к анорексии и снижению массы тела.
ВИТАМИН В6 (ПИРИДОКСИН, ПИРИДОКСАЛЬ, ПИРИДОКСАМИН)
Структура. В основе витамина В6 лежит пиридиновое кольцо. Известны 3 формы витамина В6, отличающиеся строением замещающей группы у атома углерода в п-положении к атому азота. Все они характеризуются одинаковой биологической активностью.
|
CH |
OH |
|
CHO |
|
|
CH NH |
2 |
|
2 |
|
|
|
|
|
2 |
|
HO |
|
CH OH |
HO |
CH OH |
HO |
|
CH OH |
|
|
|
2 |
|
|
2 |
|
|
2 |
H C |
N |
|
H C |
N |
|
H C |
N |
|
3 |
|
3 |
|
3 |
|
|||
П иридо ксин |
|
П иридо ксаль |
Ï |
иридо ксам ин |
||||
|
|
|
|
|
|
|||
|
|
|
|
Âè òàì è í |
 |
|
|
|
|
|
|
|
|
6 |
|
|
|
Физико-химические свойства. Все 3 формы витамина — бесцветные кристаллы, хорошо растворимые в воде.
Источники. Продукты питания: яйца, печень, молоко, зеленый перец, морковь, пшеница, дрожжи. Некоторое количество витамина синтезируется кишечной флорой.
Суточная потребность составляет 2-3мг.
Активация. Все формы витамина В6 под действием пиридоксалькиназы превращаются в коферменты пиридоксальфосфат и пиридоксаминфосфат.
|
CHO |
|
|
|
|
|
CHO |
|
|
|
|
HO |
|
ÀÒÔ |
ÀÄÔ |
HO |
H2 |
O |
|
PO3H2 |
|||
CH2OH |
C |
|
|
||||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
п и ридо ксальки н аза |
H3C |
|
|
|
|
|
|||
N |
|
|
|
|
N |
|
|
|
|||
|
П иридо ксаль |
|
|
|
|
П иридо ксальф о сф ат |
|||||
|
Âè òàì è í Â6 |
|
|
|
|
|
Êî ô åðì åí ò |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Биологические функции. Пиридоксалевые ферменты играют ключевую роль в обмене АК: катализируют реакции трансаминирования и декарбоксилирования аминокислот, участвуют в специфических реакциях метаболизма отдельных АК: серина, треонина, триптофана, серосодержащих аминокислот, а также в синтезе гема.
259
