
- •1. Ферменты: определение понятия, химическая природа, физико-химические свойства и биологическая роль ферментов.
- •2. Изоферменты. Строение, биологическая роль, диагностическое значение определения, изменение в онтогенезе и при патологии органа, диагностическое значение.
- •5. Ингибирование активности ферментов, виды ингибирования: обратимое, необратимое, конкурентное, неконкурентное
- •6. Регуляция активности ферментов: неспецифическая, специфическая (понятия). Механизмы специфической регуляции активности ферментов
- •9. Энзимопатии: понятие, классификация, молекулярные причины возникновения и механизмы развития, последствия, биохимическая диагностика.
- •10. Энзимодиагностика: классификация ферментов клетки, крови в энзимодиагностике, диагностическое значение, применение в педиатрии
- •11. Биохимические основы энзимотерапии, применение ферментов в энзимотеравии (примеры)
- •12. Цикл Кребса - схема реакций, ферменты, коферменты, энергетический баланс одного оборота. Тканевые особенности в детском возрасте, Регуляция.
- •14. Механизмы сопряжения и разобщения дыхания и фосфорилирования, эндогенные и экзогенные разобщители.
- •15. Микросомальное биологическое окисление (система транспорта электронов, цитохромы р-450, в-5). Биологическое значение, регуляция, особенности активности ферментов в детском возрасте
- •21. Нормогликемия, пути превращения углеводов в клетках организма и ключевая роль глюкозо-б-фосфата.
- •23. Аэробный путь окисления глюкозы, тканевые особенности, энергетический баланс. Эффект Пастера, регуляция.
- •24. Катаболизм глюкозы по пентозофосфатному пути, биологическая роль. Регуляция значение пентозофосфатного пути в обеспечении метаболических процессов в организме человека
- •25. Гипогликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •26. Гипергликемия: биохимические причины возникновения, механизмы восстановления нормогликемии, биохимические особенности детского возраста
- •27. Контринсулярные гормоны (глюкагон, адреналин, кортизол): химическая природа, молекулярные механизмы участия в углеводном обмене.
- •29. Сахарный диабет инсулинзависимый (ИЗСД, I тип): биохимическая диагностика, механизмы развития метаболических нарушений (гипергликемия, холестеринемия, кетонемия, ацидоз, гликозилирование белков), биохимические особенности детского возраста
- •36. Липолиз триглицеридов в белой и бурой жировой ткани
- •37. Механизмы β - окисления жирных кислот. Регуляция
- •38. Пути обмена АцКоА. Кетоновые тела: биологическая роль, кетонемия, кетонурия, причины и механизмы развития, последствия, биохимические особенности детского возраста.
- •39. Обмен холестерина в организме человека. Регуляция синтеза холестерина
- •40. Атеросклероз: биохимические причины, факторы риска, лабораторная диагностика риска развития атеросклероза: обмена и развития его нарушений, гендерные особенности.
- •41. Роль белка в питании: состав и классификация пищевых белков, заменимые и незаменимые аминокислоты. Принципы нормирования белка в питании детей и взрослых. Азотистый баланс организма человека.
- •45. Причины токсичности аммиака и пути обезвреживания аммиака (образование глн, цикл мочевины, регуляция).
- •47. Регуляторные системы организма. Определение понятия – гормоны, принципы классификации гормонов.
- •48. Уровни и принципы организации нейро – эндокринной системы. Концепции обратной связи.
- •49. Рецепция и механизмы действия стероидных гормонов.
- •50. Рецепция и механизмы действия пептидных гормонов
- •55. Белки плазмы крови: классификация, диагностическое значение электрофореграмм.
- •57. Альбумины сыворотки крови: физико-химических свойства, функции, обмен
- •60. Гемоглобин: виды, строение, функции, обмен в норме. Метгемоглобинредуктазная система.
- •61. Биохимические функции почек, особенности метаболических процессов в почках.
- •63. Состав первичной и конечной мочи, физико – химические показатели в норме.
- •64. Химический состав мочи в норме и при патологии. Клиренс: понятие, виды.
- •65. Ренин-ангиотензин-альдостероновая система (РААС) в поддержании гомеостаза натрия. Механизм действия альдостерона на молекулярном уровне в почке и слюнных железах
- •66. Антидиуретический гормон и регуляция водного баланса организма.
- •67. Биохимические гомеостатические функции печени, биохимические особенности в детском возрасте.
- •68. Функциональные пробы и нагрузки характеризующие состояние углеводного, липидного, белкового обмена и детоксицирующей функции печени у детей. И взрослых.
- •70. Белки соединительной ткани коллаген и эластин: особенности аминокислотного состава и структурной организации молекул. Витамин С в синтезе коллагена.
- •74.Витамин Д – этапы образования активных форм, их метаболические функции, механизм действия. Роль печени, почек в обмене витамина Д, патохимические причины развития рахита, показатели кальций-фосфорного обмена при рахите на разных стадиях болезни.
- •75.Паратиреоидный гормон (ПГ) и кальцитонин (КГ) – химическая природа, стимулы секреции, механизмы действия в регуляции обмена кальция и ремоделирования костной ткани, проявления гипо- и гипертиреоза
- •76.Биохимические процессы в остеобластах и остеокластах в ремоделировании костной ткани.
- •77.Белковые и минеральные компоненты костной ткани
- •78.Биохимия нервной ткани: особенности химического состава, метаболических процессов, синтез нейромедиаторов.
- •80.Миокард: особенности метаболических процессов, метаболические нарушения при гипоксии, клиническая биохимическая энзимодиагностика при инфаркте миокарда
- •81.Биохимия лактации: физико – химические свойства, химический состав грудного молока, характеристика ферментов молока. Изменение химического состава в процессе лактации: виды женского молока
- •82.Биохимия лактации: биохимические механизмы образования органических компонентов молока в лактирующей железе, белок лактальбумин, роль гормонов (пролактин, окситоцин, плацентарного лактоген, эстрогены, СТГ, Т3, Т4, кортизол, инсулин)
- •83.Витамины: химическая природа, классификация по растворимости в воде и биохимическим механизмам действия. Провитамины и механизмы их активации (на примере провитаминов Д и А). Эндогенные и экзогенные причины гипо- , гипер- и авитаминозов
- •84.Витамины-коферменты РР, В2 участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •Симптомы гиповитаминоза
- •Симптомы гиповитаминоза
- •86.Витамины-коферменты В12, фолиевая кислота участие в метаболических процессах, биохимические проявления гиповитаминозов
- •87.Витамин С: участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
- •89.Буферные системы плазмы крови: гидрокарбонатная, фосфатная, белковая Гемоглобиновая буферная система эритроцитов, связь с гидрокарбонатной системой плазмы и эритроцита. Механизмы участия карбоангидразы в регуляции КОС.
- •90.Кислотно-основный гомеостаз: биологическое значение постоянства внутренней среды организма., механизмы поддержания КОС, особенности в детском возрасте.
- •91.Нарушения КОС - классификация по механизмам? Биохимические пути компенсации.

ам ин о кисло та |
|
|
||
|
H |
|
|
|
HOOC |
C |
R |
H O |
|
|
|
1 |
2 |
|
|
NH |
|
|
|
|
|
2 |
|
|
H |
|
Î |
|
|
|
Ñ |
|
|
|
|
|
CH OPO H |
2 |
|
HO |
|
2 |
3 |
|
|
|
|
|
|
H C |
N |
|
|
|
3 |
|
|
|
|
п и ри до ксальф о сф ат |
|
|||
|
H |
|
|
|
HOOC |
C |
R |
|
|
|
N |
|
|
|
H |
Ñ |
|
|
|
|
|
CH |
OPO H |
2 |
HO |
|
2 |
3 |
|
|
|
|
|
|
H C |
N |
|
|
|
3 |
|
|
|
|
Ø è ô ô î âî |
|
|
||
î ñí î âàí è å |
|
|
||
альди м и н |
|
|
||
|
|
|
|
|
кето кисло та |
|
|
||
|
|
|
|
|
HOOC |
C |
R |
|
|
|
|
|
|
|
|
|
1 |
|
|
HOOC |
C |
R |
H O |
|
|
O |
|
|
|
2 |
|
|
|
|
|
|
|||
|
N |
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
2 |
|
|
H |
Ñ |
H |
|
|
H |
Ñ |
H |
|
|
|
|
|
|
|
|
|
|||
|
|
CH OPO H |
|
|
CH OPO H |
|
|||
HO |
|
2 |
3 |
2 |
|
|
2 |
||
|
|
|
|
HO |
|
2 |
3 |
||
|
|
|
|
|
|
|
|
|
|
H C |
N |
|
|
|
H C |
|
|
|
|
3 |
|
|
|
N |
|
|
|
||
|
|
|
|
|
3 |
|
|
|
|
Ø è ô ô î âî |
|
ï è ðè äî êñàì è í ô î ñô àò |
|
|
|||||
|
|
|
|
|
|
||||
î ñí î âàí è å |
|
|
|
|
|
|
|
||
êåò àì è í |
|
|
|
|
|
|
|
||
Нарушение обмена. Авитаминоз В6 у детей проявляется повышенной возбудимостью ЦНС, периодическими судорогами, что связано с недостаточным образованием тормозного медиатора ГАМК, специфическими дерматитами.
У взрослых признаки гиповитаминоза В6 наблюдают при длительном лечении туберкулёза изониазидом (антагонист витамина В6). При этом возникают поражения нервной системы (полиневриты), дерматиты, гомоцистинурия, цистатионурия, нарушения обмена триптафана.
86.Витамины-коферменты В12, фолиевая кислота участие в метаболических процессах, биохимические проявления гиповитаминозов
ФОЛИЕВАЯ КИСЛОТА (ВИТАМИН ВС, ВИТАМИН B9)
Структура. Фолиевая кислота состоит из трёх структурных единиц: остатка птеридина, парааминобензойной и глутаминовой кислот. Витамин, полученный из разных источников, может содержать 3—6 остатков глутаминовой кислоты.
|
OH |
|
H |
|
|
O |
COOH |
|
|
|
N |
2 |
|
||||
|
|
C |
|
C |
HN CH |
|
||
|
N |
|
|
N |
|
|||
|
|
|
|
|
||||
|
|
|
|
|
|
|
||
|
|
|
|
|
H |
|
CH |
2 |
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
|
|
CH |
2 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
2 |
N |
N |
|
|
|
|
COOH |
|
|
|
|
|
|
||||
|
п теридин |
|
|
|
Ï ÀÁÊ |
Ãëó |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
|
|
Âè òàì è í |
Âñ (ô î ë è åâàÿ ê è ñë î òà) |
|
|
|||
Фолиевая кислота была выделена в 1941г. из зелёных листьев растений, в связи, с чем и получила своё название (от лат. folium — лист).
Физико-химические свойства.
260
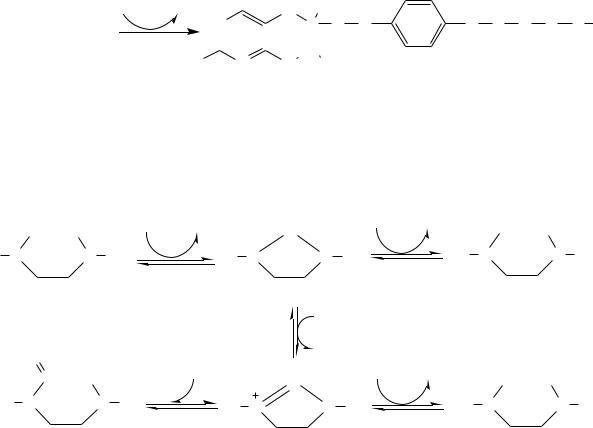
Источники. Значительное количество этого витамина содержится в дрожжах, печени, почках, мясе и других продуктах животного происхождения. Этот витамин в достаточной степени синтезируется кишечной микрофлорой.
Суточная потребность в фолиевой кислоте колеблется от 0,05-0,4мг; однако, вследствие плохой всасываемости этого витамина рекомендуемая суточная доза — 400 мкг.
Активация. Активная форма фолиевой кислоты – ТГФК. Она образуется в печени при восстановлении фолиевой кислоты с участием фолатредуктазы и дигидрофолатредуктазы, коферментом которых служит НАДФН2.
|
|
|
|
|
OH |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
2Í ÀÄÔÍ |
2 |
2Í ÀÄÔ |
+ |
|
|
|
|
H H |
|
O |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
N |
H |
|
|
|
H |
H |
H |
H |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
2 |
|
2 |
|
||||
Фо лиевая кисло та |
|
|
N |
|
|
C |
C |
|
N |
C |
N |
C |
C |
|
C |
|
COOH |
|||||||
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
|
|
CH |
H |
|
|
|
|
|
|
COOH |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
N |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Биологическая роль. ТГФК принимает от АК одноуглеродные фрагменты: серин и глицин дают метиленовый фрагмент (-СН2-), гистидин – формимино- и формильный фрагменты.
В составе ТГФК одноуглеродные фрагменты могут подвергаться взаимопревращениям: метиленовая группа превращаться в метенильную (-СН=), формильную (-НС=О), метильную (-СН3) и формиминогруппу (-CH=NH).
|
|
|
|
|
|
|
|
|
H |
|
|
Í |
ÀÄÍ |
|
|
+ |
|
|
|
|
|||
|
|
H |
H |
|
Ñåð |
Ãëè |
|
|
2 |
|
2 |
Í ÀÄ |
|
CH3 |
H |
|
|||||||
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
R |
N |
N |
R |
|
R |
N |
|
|
|
N |
R |
|
|
|
|
|
|
R |
N |
N |
R |
||
1 |
5 |
|
|
2 |
1 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
5 |
|
10 |
|
|
|
10 |
|
|
|
5 |
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
5 |
10 |
-м етилен -ТГФК |
|
|
|
|
|
5 |
|
|
|
||||||
|
|
ÒÃÔÊ |
|
|
N N |
|
|
|
|
|
N -ì åòèë-ÒÃÔÊ |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Í ÀÄÔ |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
HN |
|
|
|
|
|
|
|
|
Í ÀÄÔÍ |
2 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
||
|
|
|
|
|
NH |
|
|
|
|
|
|
Í |
|
Î |
|
Í |
|
|
|
|
|||
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|||||||
|
|
CH |
H |
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
H |
OHC |
|
|||
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
R |
1 |
N |
|
N |
R |
R |
N |
|
|
N |
R |
|
|
|
|
|
|
R |
N |
N |
R |
||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|||||||||||
|
|
5 |
|
10 |
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
|
1 |
5 |
|
2 |
|
|
|
|
|
|
5 |
|
|
10 |
|
|
|
|
|
|
|
|
10 |
|
|||||
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
-ô î ðì èì èí î -ÒÃÔÊ |
5 |
10 |
-м етелен ил-ТГФК |
|
|
|
N |
10 |
-ô î ðì èë-ÒÃÔÊ |
|||||||||||||
N |
N N |
|
|
|
|
|
|||||||||||||||||
Затем ТГФК отдает одноуглеродные фрагменты на:
синтез пуриновых оснований
синтез тимидиловой кислоты
регенерацию метионина
превращение дУМФ в дТМФ;
превращение глицина в серина и т.д.
Нарушение обмена. Гиповитаминоз фолиевой кислоты возникает редко, его вызывает использование сульфаниламидных препаратов. Сульфаниламиды — структурные аналоги парааминобензойной кислоты, они ингибируют синтез фолиевой кислоты у микроорганизмов, вызывая их гибель. Некоторые производные птеридина (аминоптерин и метотрексат) тормозят рост почти всех организмов, нуждающихся в фолиевой кислоте, их используют для подавления опухолевого роста у онкологических больных.
Гиповитаминоз фолиевой кислоты приводит к:
261
1.мегалобластической (макроцитарной) анемии. Она характеризуется уменьшением количества эритроцитов, снижением содержания в них гемоглобина, что вызывает увеличение размера эритроцитов. Причина — нарушение синтеза ДНК и РНК из-за недостатка тимидиловой кислоты и пуриновых нуклеотидов.
2.лейкопении;
3.задержке роста.
4.нарушению регенерации эпителия, особенно в ЖКТ (связано с недостатком нуклеотидов для синтеза ДНК в постоянно делящихся клетках слизистой оболочки).
ВИТАМИН В12 (КОБАЛАМИН)
Структура. Витамин В12 — единственный витамин, содержащий в своём составе металл кобальт.
Физико-химические свойства.
Источники. Витамин В12 синтезируют только микроорганизмы: бактерии, актиномицеты и сине-зелёные водоросли. Из животных тканей наиболее богаты витамином В12 печень и почки.
Суточная потребность в витамине В12 крайне мала и составляет всего 0,001-0,002мг.
Активация. Из витамина В12 образуются 2 кофермента: метилкобаламин в цитоплазме и дезоксиаденозилкобаламин в митохондриях.
Биологическая роль. Метилкобаламин участвует: в образовании метионина из гомоцистеина и в превращениях одноуглеродных фрагментов в составе ТГФК, необходимых для синтеза нуклеотидов.
Дезоксиаденозилкобаламин участвует: в метаболизме ЖК с нечётным числом углеродных атомов и АК с разветвлённой углеводородной цепью.
Нарушение обмена. Гиповитаминоз возникает при нарушении всасывании В12 из-за дефицита фактора Касла. Фактор Касла - гликопротеин с молекулярной массой 93000Да, который синтезируется обкладочными клетками желудка. В ЖКТ фактор Касла соединяется с витамином B12 при участии Ca2+, защищает его от разрушения и обеспечивает всасывание. Дефицит фактора Касла возникает при пониженной кислотности желудочного сока (может быть результатом повреждения слизистой оболочки желудка), после тотального удаления желудка при хирургических операциях.
Гиповитаминоз В12 сопровождается:
1.макроцитарной (мегалобластической) анемией: снижение числа эритроцитов, гемоглобина, увеличение размера эритроцитов. Причина — нарушение синтеза нуклеиновых кислот в быстроделящихся клетках кроветворной системы.
2.расстройствами деятельности нервной системы. При катаболизме жирных кислот с нечетным количеством атомов С и разветвленных АК из-за дефицита В12 накапливается нейротоксичная метилмалоновая кислота.
262
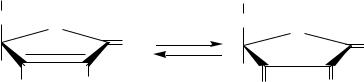
87.Витамин С: участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
Структура. Аскорбиновая кислота — лактон кислоты, близкой по структуре к глюкозе. Существует в двух формах: восстановленной (АК) и окисленной (дегидроаскорбиновой кислотой, ДАК), которые обратимо переходят друг в друга в окислительно-восстановительных реакциях.
CH OH |
|
|
CH |
OH |
|
2 |
|
|
|
||
|
|
|
2 |
|
|
CHOH |
|
- 2H |
CHOH |
|
|
O |
|
O |
|||
|
|
|
|||
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
H |
OH |
+2H |
H |
|
|
OH |
|
O |
O |
||
|
|
||||
|
|
|
|
||
Àñê î ðáè í |
î âàÿ ê -òà |
Äåãè äðî àñê î ðáè í î âàÿ ê -òà |
|||
Аскорбиновая кислота может окисляться кислородом воздуха, пероксидом и другими окислителями. ДАК легко восстанавливается цистеином, глутатионом, сероводородом.
Физико-химические свойства. Белые кристаллы, растворимые в воде. В слабощелочной среде происходят разрушение лактонового кольца и потеря биологической активности. При кулинарной обработке пищи в присутствии окислителей часть витамина С разрушается.
Источники витамина С — свежие фрукты, овощи, зелень.
Продукт |
Содержание |
Продукт |
Содержание |
|
витамина, мг/100г |
витамина, мг/100г |
|||
|
|
|||
|
|
|
|
|
Плоды шиповника |
2400 |
Яблоки |
30 |
|
|
|
|
|
|
Облепиха |
450 |
Картофель свежий |
25 |
|
|
|
|
|
|
Смородина чёрная |
300 |
Томаты |
20 |
|
|
|
|
|
|
Лимоны |
40 |
Молоко |
2,0 |
|
|
|
|
|
|
Апельсины |
30 |
Мясо |
0,9 |
|
|
|
|
|
Суточная потребность человека в витамине С составляет 50—75мг.
Биологические функции. АК вместе с ДАК образует в клетках окислительновосстановительную пару с редокс-потенциалом +0,139 В. Благодаря этой способности аскорбиновая кислота участвует:
1.в реакциях гидроксилирования Про и Лиз при синтезе коллагена;
2.в реакциях гидроксилирования дофамина в норадреналин;
3.в синтезе стероидных гормонов в коре надпочечников;
4.в восстановлении Fe3+ в Fe2+ в кишечнике, что необходимо для всасывания железа;
5.в освобождение железа из ферритина;
6.в превращении фолата в коферментные формы;
Аскорбиновая кислота является природным антиоксидантом, она подавляет реакции СРО двумя механизмами:
1.восстанавливает окисленную форму витамина Е, поддерживая в мембране концентрацию активной формы восстановленного витамина Е.
263
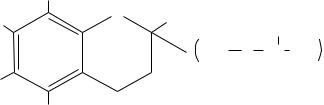
2. инактивирует активные формы кислорода О2• , Н2О2, НО• в водной фазе.
Нарушение обмена. Недостаточность аскорбиновой кислоты приводит к развитию цинги (скорбут). Цингой болеют только человек, приматы и морские свинки.
Главные проявления цинги - нарушение образования коллагена в соединительной ткани, что проявляется разрыхлением дёсен, расшатыванием зубов, нарушением целостности капилляров и подкожными кровоизлияниями. Возникают отёки, боль в суставах, анемия. Причина анемии связана с нарушением обмена железа и фолиевой кислоты.
88.Витаминыантиоксиданты: Е, А, участие в метаболических процессах, биохимические механизмы проявления гиповитаминозов
ВИТАМИН Е (ТОКОФЕРОЛЫ)
Структура. Термин ''витамин E'' включает 8 форм метильных производных токола: α, β, γ и дельта токоферолы и α, β, γ и дельта токотриенолы. Наибольшую биологическую активность проявляет α-токоферол:
CH |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C |
|
O |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
3 |
|
|
|
|
|
CH |
3 |
|
|
|
|
|
|
H |
|
|
|
||
|
|
|
|
2 |
|
|
|
||
|
|
|
H C |
C |
CH CH |
|
H |
||
|
|
|
|
2 |
|||||
|
|
|
2 |
|
|
|
|
3 |
|
HO |
|
|
|
|
|
|
|
|
|
CH |
3 |
|
à-Òî ê î ô åðî ë |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Физико-химические свойства. Токоферолы представляют собой маслянистую жидкость, хорошо растворимую в органических растворителях.
Источники витамина Е для человека — растительные масла, салат, капуста, семена злаков, сливочное масло, яичный желток.
Суточная потребность взрослого человека в витамине Е примерно 15 мг. В течение беременности необходимо увеличение потребления витамина E.
Метаболизм.
1.Все формы витамина E связываются энтероцитами и попадают в кровообращение с хиломикронами.
2.Витамин Е достигает печени, где специфический протеин (α-TTP - токоферолтранспортный протеин) селективно выделяет α-токоферол из всех поступающих токоферолов и включает его в ЛПОНП. Другие формы выделяются с желчью и мочой в виде карбоксиэтил гидрорксихроманов. Концентрация α-токоферола в ЛПОНП не может быть увеличена более чем в 2-3 раза т.к. процесс абсорбции контролируется.
3.альфа-токоферол инактивируется в печени превращением в токофероновую кислоту и токоферонолактон. Токофероновая кислота и токоферонолактон затем конъюгируют с глюкуроновой и серной кислотой и выделяются с мочой как глюкурониды и сульфаты.
Биологическая роль
264
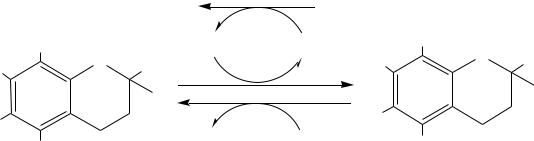
Токоферол является биологическим антиоксидантом, входит в состав неферментативной антиоксидантной системы организма
|
|
|
|
H O |
OH* |
|
|
|
|
|
|
|
2 |
|
|
|
|
CH3 |
|
|
*RCOOH |
RCOOH |
CH |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
CH |
|
H C |
|
O |
CH3 |
H C |
|
|
|
|
||||
|
|
3 |
3 |
|
|
|
||
3 |
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
R |
|
|
|
|
|
|
|
|
||
HO |
|
|
|
|
*O |
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
äåãè äðî àñê î ðáàò |
àñê î ðáàò |
CH |
3 |
|
|
3 |
|
|
|
|
|
|||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
à-Òî ê î ô åðî ë |
|
|
|
|
à-Òî ê î ô åðî ë |
|
||
|
|
|
|
|
|
|
||
Нарушение обмена.
Гиповитаминоз Е. Мало изучен. Из-за диетических ограничений он наблюдается только у недоношенных новорожденных в виде гемолитической анемии и ретинопатии.
У взрослых гиповитаминоз Е возникает из-за генетического дефицита аполипопротеина B (apo B) или α-токоферол транспортного протеина (α-TTP).
Симптомы прежде всего неврологические (из-за демиелинизация аксонов) и включают потерю глубоких сухожильных рефлексов, мозжечковую атаксию, дизартрию и олигофрению, нарушения проприоцептивной чувствительности. Кроме того, может происходить скелетная миопатия и пигментный ретинит, развитие гемолитической анемии, креатинурия, отложения сфинголипидов в мышцах.
ВИТАМИН А (РЕТИНОЛ)
Структура. Витамин А представлен 3 веществами: ретинолом (циклический, ненасыщенный, одноатомный спирт), ретиналем и ретиноевой кислотой.
Физико-химические свойства.
Источники: Витамин А содержится только в животных продуктах: печени крупного рогатого скота и свиней, яичном желтке, молочных продуктах; особенно богат этим витамином рыбий жир.
Каратиноиды (провитамин А) содержаться в растительных продуктах: моркови, красном перце, зеленом салате, помидорах, плодах рябины, шиповнике.
Суточная потребность. Активность витамина А в пищевых продуктах выражается в международных единицах МЕ. 1 МЕ витамина А эквивалентна 0,0003мг ретинола или 0,0006мг β- каротина. Суточная потребность взрослого человека в витамине А составляет от 1 (3300 МЕ) до 2,5мг ретинола или от 2 до 5мг β-каротинов.
Активация. В слизистой оболочке кишечника и печени каратиноиды под действием каратиндиоксигеназы превращаются в ретинол, который потом окисляется в ретиналь и ретиноевую кислоту.
Действие
Витамин А повышает иммунитет множеством различных способов, что увеличивает сопротивляемость организма к инфекциям. Удовлетворение потребностей населения всего мира в витамине А могло бы ежегодно спасать от 1,2 до 2,5 миллиона жизней. Количество смертных
265
