
УП- Биоорганическая химия
.pdf
16 Вычислите общую длину всех полипептидных цепей одной клетки E. coli, содержащей 106 молекул белка (молекулярная масса каждого – 40000). Считайте, что все молекулы собраны в альфа-спирали.
17Волосы растут со скоростью 15-20 см в год. Зона роста находится в основании волоса, где синтезируются и скручиваются нити α-кератина. Основным структурным элементом кератина является α-спираль, виток которой имеет шаг 5,5 ангстрема и содержит 3,6 аминокислотных остатка. Рассчитайте скорость образования пептидных связей кератина (число пептидных связей в секунду), которая обеспечивает наблюдаемый рост волос.
18Какая из аминокислот скорее всего будет на поверхности белка: триптофан или глутамин?
Какую из аминокислот маловероятно встретить внутри белкового пространства: серин или валин?
Какую из аминокислот маловероятно встретить в середине α-спирали: лейцин или изолейцин?
19Вам необходимо ―разрезать‖ пептид NMTQGRCKPVNTFVHEPLVDVQNVCFKE на меньшие фрагменты. Какая из представленных в таблице ниже протеаз расщепит пептид на большее количество фрагментов? А какая на меньшее? Напишите последовательности получаемых в результате гидролиза фрагментов
Таблица 1-4. Специфичность некоторых эндопептидаз.
Место расщепления связи
Фермент |
Источник |
Специфичность |
Комментарии |
|||
|
|
|
|
|||
|
бычья |
Rn-1 = положительно |
|
|||
Трипсин |
поджелудочная |
заряженные остатки: |
Высоко специфичен |
|||
|
железа |
Arg, Lys; Rn |
Pro |
|
||
|
бычья |
Rn-1 = массивные |
Медленно расщепляет |
|||
Химотрипсин |
поджелудочная |
гидрофобные остатки: |
по Rn-1 = Asn, His, Met, |
|||
|
железа |
Phe, Trp, Tyr; Rn Pro |
Leu |
|||
|
бычья |
Rn-1 |
= маленькие |
|
||
|
нейтральные остатки: |
|
||||
Эластаза |
поджелудочная |
|
||||
Ala, Gly, Ser, Val; Rn |
|
|||||
|
железа |
|
||||
|
Pro |
|
|
|||
|
|
|
|
|||
|
Bacillus |
Rn = Ile, Met, Phe, Trp, |
Иногда расщепляет по |
|||
Термолизин |
Rn=Ala, Asp, His, Thr, |
|||||
thermoproteolyticus |
Tyr, Val; Rn-1 |
Pro |
||||
|
устойчив к нагреванию |
|||||
|
|
|
|
|
||
|
бычья слизистая |
Rn = Leu, Phe, Trp, Tyr; |
И другие; весьма |
|||
Пепсин |
неспецифичен; pH |
|||||
желудка |
Rn-1 |
Pro |
|
|||
|
|
оптимум = 2 |
||||
|
|
|
|
|
||
Эндопептидаз |
Staphylococcus aureus |
Rn-1 = Glu |
|
|
||
а V8 |
|
|
||||
|
|
|
|
|
||
|
|
71 |
|
|
||
20 В таблице ниже представлены первые 10 аминокислотных остатков B-спирали миоглобина различных организмов.
Позиция |
1 |
2 |
3 |
4 |
5 |
|
6 |
|
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
человек |
D |
I |
P |
G |
H |
G |
|
Q |
|
E |
V |
L |
|
|
|
|
|
|
|
|
|
|
|
|
|
курица |
D |
I |
A |
G |
H |
G |
|
H |
|
E |
V |
L |
|
|
|
|
|
|
|
|
|
|
|
|
|
аллигатор |
K |
L |
P |
E |
H |
G |
|
H |
|
E |
V |
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
черепаха |
D |
L |
S |
A |
H |
G |
|
Q |
|
E |
V |
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
тунец |
D |
Y |
T |
T |
M |
G |
|
G |
|
L |
V |
L |
|
|
|
|
|
|
|
|
|
|
|
|
|
карп |
D |
F |
E |
G |
T |
G |
|
G |
|
E |
V |
L |
|
|
|
|
|
|
|
|
|
|
|
|
|
Основываясь на этой информации, определите какие из позиций: а) не могут быть изменены;
б) допускают консервативные замены на схожие по структуре или свойствам аминокислотные остатки;
в) заменяются на любые аминокислотные остатки.
21Объясните, почему желатин, являющийся коллагеном, менее питателен, чем другие белки.
22Ферменты способны работать в довольно узком диапазоне рН. Какие процессы происходят в белке при сильном закислении или защелачивании среды, вызывающим потерю активности фермента?
Контрольные вопросы
1На отдельном листочке каждому студенту дается одна из структур (a-f), приведенных на рисунке. Задание: рассмотрите внимательно эти структуры и ответьте на следующие вопросы: а) является ли данная структура пептидом? б) если «да», то изобразите последовательность аминокислот в нем трехбуквенным и
однобуквенным кодом.
2 Пищеварительный тракт личинки платяной моли имеет восстанавливающую среду. Какие преимущества дает личинке это свойство?
4 Дана аминокислотная последовательность:
NMTQGRCKPVNTFVHEPLVDVQNVCFKE
а) изобразите ее, используя трехбуквенный код; б) где в данной последовательности возможно образование изгибов или ß-поворотов? в) где могут образоваться внутримолекулярные дисульфидные мостики? г) представьте, что данный полипептид
– это низкомолекулярный глобулярный белок. Какие аминокислоты экспонированы внутрь белковой глобулы, а какие – во внешнюю?
72

Структурные формулы для Задачи 1
ЦИТИРУЕМАЯ ЛИТЕРАТУРА
[1]Высоцкий Е.С., Маркова С.В., Франк Л.А. Кальций-регулируемые фотопротеины морских кишечнополостных. Молекулярная биология. 2006, 40, 404-417.
[2]Y.J. Gordon, E.G. Romanowski. A Review of antimicrobial peptides and their therapeutic potential as anti-infective drugs. Current Eye Research. – 2005, 30 (7), 505-515.
[3]J.D. Steckbeck, B. Deslouches, R.C. Montelaro. Antimicrobial peptides: new drugs for bad bugs? Expert opinion on biological therapy. – 2014, 14 (1), 11-14.
73
ЧАСТЬ 2. НУКЛЕИНОВЫЕ КИСЛОТЫ
Во второй половине 19-го века считалось, что клетки животных состоят в основном из белков. В 1869 г. швейцарский химик Иоганн Мишер обнаружил в ядрах клеток новую субстанцию, обладающую странными свойствами. Когда чистые ядра клеток из гноя хирургических бинтов обрабатывали слабыми щелочными растворами с последующей нейтрализацией кислотой, получали преципитат в виде тяжей и хлопьев. Поскольку субстанция содержалась в клеточных ядрах, Мишер назвал ее «нуклеин». Было установлено, что нуклеин содержится также в ядрах и других клеток и в его химическом составе помимо обычных элементов – углерода, кислорода, водорода и азота, обнаружили фосфор. Долгое время считалось, что ядра являются неким «фосфорным депо»,
создаваемым клеткой с неизвестной целью. И только в 40-е годы 20-го века было показано, что материал клеточного ядра (нуклеиновые кислоты) переносит наследственную (генетическую) информацию. Чтобы понять, как это происходит, было необходимо установить структуру нуклеиновых кислот. Молекулы этих соединений выделили в чистом виде и были получены кристаллы, пригодные для рентгеноструктурного анализа. В 1953 г. Розалинд Франклин (Королевский колледж,
Лондон) удалось получить удивительно четкие рентгеновские дифракционные фотографии ДНК, которые помогли Джеймсу Уотсону и Френсису Крику в 1953 г.
успешно расшифровать структуру этой молекулы. С тех пор химия нуклеиновых кислот бурно развивалась и сегодня трудно представить, что на памяти всего одного поколения были достигнуты столь ошеломляющие успехи. Возникли новые науки – генетика, генная инженерия, медицинская, популяционная и эволюционная генетика, прочтен генетический код многих организмов, в том числе и человека, появились понимание и надежда на успешное лечение ряда наследственных заболеваний и т.д.
В этой главе мы рассмотрим строение и химические свойства нуклеиновых кислот,
вы узнаете, что они играют важнейшую роль не только в хранении, но и передаче наследственной и другой информации и располагаются не только в ядре клетки.
2.1. Нуклеиновые основания, нуклеозиды, нуклеотиды
Нуклеиновые кислоты (nucleic acids, англ.) представляют собой линейные полимерные молекулы, состоящие из мономеров, называемых нуклеотидами (Рис. 2.1).
Каждый нуклеотид включает три компонента – гетероциклическое основание, углеводный остаток и остаток фосфорной кислоты. Рассмотрим каждый из этих структурных элементов подробно.
74

Рис. 2.1. Нуклеотид – основная единица нуклеиновых кислот.
В состав нуклеиновых кислот входят 5 вариантов гетероциклических оснований – три из них имеют в своей основе шестичленный гетероцикл пиримидин и потому называются
пиримидины. Это тимин (Thy, T), урацил (Ura, U) и цитозин (Cyt, C). Каркас молекул двух других оснований составляет конденсированный пяти- и шестичленный цикл пурина
– это аденин (Ade, A) и гуанин (Gua, G) и их, соответственно, называют пуринами. В
составе гетероциклических оснований много атомов азота, они имеют слабый оснóвный характер и потому их часто называют азотистые основания (Рис. 2.2).
Рис. 2.2. Структура и обозначения гетероциклических оснований.
Все эти молекулы являются ароматическими, т.е. имеют плоскую форму и общую замкнутую систему сопряжения π-электронов, количество которых соответствует правилу Хюккеля (см. Введение). При прохождении ультрафиолетового света через растворы этих
75

соединений наблюдается поглощение, спектры которого имеют максимум при 260 нм,
характерный для всех оснований (Рис. 2.3). На этом же рисунке приведены значения их молярной экстинкции.
Вспомним, что спектры поглощения белков имеют максимум при 280 нм (благодаря поглощению аминокислот с ароматическим боковым радикалом – W и Y, см. Рис. 1.2).
При выделении ДНК из биологического материала важной задачей является их тщательное отделение от белков. Удобным параметром для определения чистоты полученного препарата служит отношение поглощения полученного раствора при длине волны 260 нм к поглощению при 280 нм. Чем ближе это соотношение к значению 1,8, тем чище образец ДНК.
Рис. 2.3. Спектры поглощения и значения молярной экстинкции азотистых оснований (вверху). В скобках показаны значения максимумов. Спектры поглощения нуклеиновых кислот и белков имеют разные максимумы (внизу).
В состав нуклеотидов входят 2 типа углеводных остатков – рибоза и дезоксирибоза. Эти остатки присоединены к основанию через гликозидную связь. Такая двухкомпонентная
молекула называется нуклеозидом (Рис. 2.4) и их в составе нуклеиновых кислот пять:
76

аденозин (A), гуанозин (G), тимидин (T), уридин (U) и цитидин (C). Нуклеозиды с рибозой называются рибонуклеозидами, и в них входят все основания, кроме тимидина, с
дезоксирибозой – дезоксирибонуклеозидами, и в них входят все основания, кроме урацила.
Рис. 2.4. Структура и обозначение нуклеозидов.
Рибозный остаток в этой молекуле принято также считать плоской молекулой, хотя для нее свойственно образование конформаций с изломом цикла типа «конверт».
Обратите внимание – в одной и той же молекуле нуклеозида находятся 2 циклических фрагмента. Во избежание путаницы нумерацию углеродных атомов рибозы
(дезоксирибозы) принято обозначать с верхним штрихом.
Третьим элементом нуклеотида является остаток фосфорной кислоты. Напомним,
что фосфорная кислота – трехоснóвная. При взаимодействии со спиртами она может образовывать, соответственно, моно-, ди- и триэфиры (Рис. 2.5). В углеводных фрагментах нуклеозидов имеется три (для рибо-), либо две (для дезоксирибо-) гидроксильных группы.
Таким образом, присоединение к ним фосфатного остатка с образованием моноэфира
77
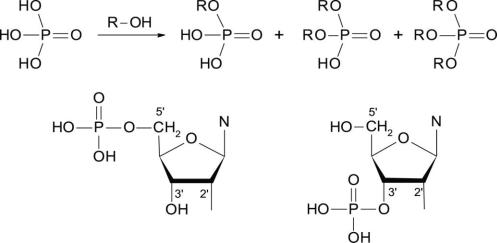
фосфорной кислоты тоже возможно в нескольких вариантах. Чтобы обозначить, где находится остаток фосфорной кислоты, указывают его положение, например, нуклеозид
Рис. 2.5. Вверху. Трехоснóвная фосфорная кислота может образовывать моно-, ди- и триэфирные соединения. Внизу. Структуры 5'- и 3'-дезоксирибонуклеозидфосфатов.
3’- или 5’-фосфат. Нуклеотиды обозначают тремя заглавными буквами 3’(или 5’) АМФ,
ГМФ, ТМФ, ЦМФ, УМФ, или английскими AMP, GMP, TMP, CMP, UMP.В нуклеиновых кислотах нуклеотиды связаны друг с другом с помощью 3’-5’-фосфодиэфирных связей
(Рис. 2.6). Для дезоксирибонуклеиновых кислот это единственный вариант связи. В
кольце рибозы имеется еще и 2’-гидроксильная группа, мало отличающаяся по химическим свойствам от 3’-гидроксила. Однако и для молекул РНК связи между нуклеотидами осуществляются единственным способом – это только 3’- 5’-
фосфодиэфирные связи.
Таким образом, остаток фосфорной кислоты представлен в этих полимерах как диэфир, а третья кислотная группа свободна и в водной среде диссоциирует, как остаток любой кислоты. В результате все молекулы нуклеиновых кислот имеют сильный отрицательный заряд, и, как правило, представлены в виде солей одно-, либо двухвалентных металлов.
Чтобы указать, в каком направлении необходимо читать последовательность, перед нею ставят 5’ или 3’ – номер гидроксила рибозного кольца, который свободен, т.е. не образует фосфодиэфирной связи со следующим нуклеотидом.
78

Полимерные молекулы нуклеиновых кислот в зависимости от размера условно разделяют на олигонуклеотиды (до 50 звеньев в молекуле) и полинуклеотиды, с бóльшим количеством звеньев.
Рис. 2.6. В молекулах нуклеиновых кислот мономеры связаны 3'-5'- фосфодиэфирными связями.
2.2. Строение молекулы ДНК
Мономерными единицами в молекуле ДНК являются дезоксирибонуклеозидфосфаты (т.е. в качестве пентозы здесь находится дезоксирибоза) с
четырьмя из перечисленных выше нуклеозидов – цитидином, тимидином, гуанозином и аденозином.
Как упомянуто ранее, в конце 40-х годов пристальное внимание биохимиков было уделено исследованиям по расшифровке строения молекулы ДНК. Было показано, что
79

именно эта молекула отвечает за передачу наследственной информации от родительской к дочерней клетке, а секрет механизма этой передачи заключается в ее структуре. Д. Уотсон и Ф. Крик установили, что ДНК существует в виде двойной правозакрученной спирали.
Две полинуклеотидных цепи соединены друг с другом водородными связями и образуют правовинтовую спираль вокруг общей оси (Рис. 2.7). Цепи двойной спирали антипараллельны – одна из них направлена от 3’- к 5’-концу, а другая, наоборот, от 5’ к 3’.
Рис. 2.7. Двойная спираль ДНК, установленная Уотсоном и Криком. Пятиугольниками обозначены остатки дезоксирибозы, р – остатки фосфорной кислоты. Серой и зеленой лентами обозначены противонаправленные комплементарные полинуклеотидные цепи.
Кроме того, в ДНК соблюдается принцип комплементарности, т.е. водородные связи образуются только между конкретными парами оснований – G и C или A и T (Рис. 2.8).
Гетероциклические основания направлены в центр спирали, а их плоскости практически перпендикулярны ее оси. Один виток спирали содержит 10 нуклеотидов, его высота равна
3,4 нм. Обратите внимание, пара G-C образует три водородных связи, а пара A-T – две.
80
