
УП- Биоорганическая химия
.pdf
вещества с высокой температурой плавления (см. Табл. 4.1). Наличие одной или нескольких двойных связей в цис-конфигурации, ломающих линейность углеводородной цепи и ограничивающих свободу вращения радикалов относительно друг друга, делает невозможным создание плотной упаковки молекулы. Поэтому непредельные жк представляют собой либо легкоплавкие, либо жидкие вещества (см. Табл. 4.1).
ПНЖК, необходимые животным (и человеку), но не синтезируемые в их организме,
называют незаменимыми. К незаменимым ПНЖК относятся линолевая кислота с двумя двойными связями 18:2 (Δ9,12) и альфа-линоленовая кислота с тремя двойными связями 18:3 (Δ9,12,15). Основная их роль в организме животных и человека состоит в том, что они могут являться биохимическими предшественниками физиологически значимых длинноцепочечных ПНЖК с 20-22 атомами углерода. Длинноцепочечные ПНЖК,
называемые частично незаменимыми, это арахидоновая (эйкозатетраеновая) кислота 20:4 (Δ5,8,11,14), эйкозапентаеновая кислота 20:5 (Δ5,8,11,14,17) и докозагексаеновая кислота 22:6(Δ4,7,10,13,16,19). Пространственные модели этих кислот приведены на рисунке 4.1.
 Светящийся гриб Neonothogamus nambi. Фото К.В. Пуртова,
Светящийся гриб Neonothogamus nambi. Фото К.В. Пуртова,
Институт биофизики СО РАН СО РАН, Красноярск.
Перечисленные закономерности строения жирных кислот в целом сохраняются для всех организмов. Однако к настоящему времени в ряде организмов были обнаружены редкие жирные кислоты с особым строением.
1. Разветвления цепи бокового радикала обнаружены у жирных кислот многих микроорганизмов [1, 2]. Ниже приведены примеры таких структур.
СН3 СН3(СН2)7-СН-(СН2)8-СООН – турберкулостеариновая кислота, из туберкулезной палочки
Micobacterium tuberculosis
CH3 (CH2)5 CH-CH-(CH2)7-COOH – циклопропановая кислота С17:0 из бактерии
CH2 Cupriavidus eutrophus B-10646
141
2. Необычное относительное расположение двойных связей в полиненасыщенных кислотах.
В масле кедрового ореха обнаружены кислоты, в которых двойные связи разнесены более чем на одну этиленовую (СН2) группу. В приведенных ниже структурах эти элементы подчеркнуты.
СН3 (СН2)7-СН=СН-СН2-СН2-СН2-СН=СН-(СН2)4-СООН – октадекадиеновая 18:2, ω9,13
СН3 (СН2)4-СН=СН-СН2-СН=СН-СН2-CH2-CH=СН-(СН2)3-СООН – октадекатриеновая,
18:3, ω6,9,13
СН3 (СН2)5-СН=СН-СН2-СН2-СН=СН-СН2-CH2-CH=СН-(СН2)3-СООН – эйкозатриеновая,
20:3, ω7,11,1
В некоторых организмах обнаружены кислоты с коньюгированными двойными связями, т.е. расположенными подряд, без этиленовых «вставок», например, в грибах Neonothogamus nambi найдены линолевые кислоты, в цис- (с) или транс- (t)
конфигурациях, такие как С18:2, ω9с,11t; С18:2, ω9t,11c; С18:2 и ω10t12c [3].
Показано, что жирные кислоты с коньюгированными двойными связями относятся к высокоактивным биологическим соединениям с ярко выраженной противовоспалительной
ипротивораковой активностью. И этот факт вызывает повышенный интерес исследователей к поиску подобных кислот в других организмах.
3.Среди необычных кислот природного происхождения также находятся так называемые ацетиленовые кислоты, в структуре которых обнаружены как двойные, так
итройные связи. Такие кислоты синтезируются, например, некоторыми водными мхами. Типичным источником таких кислот является Fontinalis antipyretica, обитающий в р. Енисей [4]. В биомассе этого растения обнаружено семь ацетиленовых кислот, среди которых доминирующими являюся октадека-9,12-диен-6-иновая (18:3, 6а,9,12), октадека- 9,12,15-триен-6-иновая (18:4, 6а,9,2,15) и эйкоза-11,14-диен-8-иновая (20:3, 8а,11,14). Подобные сибмионты не синтезируются никакими другими пресноводными гидробионтами и потому их используют как высокоспецифичные биохимические маркеры при изучении спектров питания водных беспозвоночных животных.
Таким образом, живой мир характеризуется огромным разнообразием синтезируемых веществ и, в частности, жирных кислот.
Материал подготовлен и любезно предоставлен д.б.н. Г.С. Калачевой, Институт биофизики СО РАН, г. Красноярск
Воска представляют собой сложные эфиры жирных кислот и длинноцепочечных спиртов с насыщенными углеводородными радикалами переменного состава (Рис. 4.2).
Помимо энергетического запаса соединения этого типа используются рядом водоплавающих птиц и животных для обеспечения водоотталкивающих свойств перьям и шерсти. Растительные воска покрывают листья растений, защищая их от избыточной
142

потери влаги; из воска построены соты пчел. Само слово «воск» происходит от староанглийского «wax», обозначающего материал пчелиных сот.
Глицеролипиды являются липидами, которые представляют собой сложные эфиры жирных кислот с трехатомным спиртом – глицерином (Рис. 4.3), отсюда другое, более традиционное название этих соединений – триацилглицериды (для их обозначения в тексте часто используют сокращение ТАГ). В составе этих соединений могут быть остатки жирных кислот любой длины и насыщенности. Если все жирные кислоты одинаковые, то это простые триацилглицериды и их называют по названию кислоты – тристеарилглицерид, трипальмитоилглицерид и т.д. Большинство триацилглицеридов имеют смешанный жирнокислотный состав и в их названии обязательно указывают место локализации каждого остатка жирной кислоты (см. Рис. 4.3). Молекулы триацилглицеридов гидрофобны и потому практически не растворяются в воде. Эти вещества имеют низкую плотность, и при смешивании с водой всегда образуют верхний слой.
Рис. 4.2. Структурные формулы пчелиного и пальмового восков.
Рис. 4.3. Структура смешанного триацилглицерида 1-стеароил-2-пальмитоил-3- олеиноилглицерина.
143

Основная биологическая функция триацилглицеридов – энергетическая или
запасная. При их гидролизе освобождается значительно большее (почти в 2 раза)
количество энергии, чем при гидролизе такого же количества крахмала или гликогена.
Глицериды гидрофобны, поэтому в них, в отличие от углеводов, не аккумулируется вода,
в этом случае балластная, что, естественно, отражается на удельной энергетической
ценности липидов. Умеренно тучные люди имеют до 20 кг жировой ткани. Это
количество обеспечит энергетические нужды организма в течение месяца. Аналогичные
запасы углеводов обеспечивают организм только на сутки. Запасы жира некоторых
животных обеспечивают их энергией во время зимней спячки. Находящиеся под кожей
жировые ткани обеспечивают также теплоизоляцию северных животных и птиц.
Помимо энергетической триацилглицериды в организме выполняют еще и другие
функции.
Physeter macrocephalus) – морское млекопитающее семейства зубатых китов имеет огромную голову, составляющую до трети от массы всего тела животного. В ней помещается специфический орган, так называемый спермацетовый мешок, заполненный жировой массой – спермацетовым маслом (спермацетом), масса которого может достигать 4-х тонн. Спермацет представляет собой смесь триацилглицеридов и восков с разнообразными как насыщенными, так и ненасыщенными жирными кислотами и имеющими разные температуры плавления. Полагают, что сложный состав спермацета обеспечивает плавное изменение плавучести кита при глубоководном плавании (известно, что в поисках добычи кашалот погружается на глубины до 3 км). При нормальной температуре кашалота (37 °С) спермацет жидкий. При погружении на глубину постепенно падает температура воды и увеличивается ее плотность. Спермацет при этой температуре также постепенно (градиентно) кристаллизуется, становится более плотным, приближенным к плотности воды на глубине. При всплытии температура воды повышается, и спермацет плавится, «подстраивая» плавучесть животного к изменению внешних условий. Кроме того, известно, что добычу кашалот разыскивает с помощью ультразвуковой эхолокации, в которой важную роль играет все тот же спермацетовый мешок, используемый как акустическая линза.
Жиры являются одним из важнейших пищевых продуктов. Причем наибольшую ценность представляют ненасыщенные жирные кислоты, в основном жидкие при нормальной температуре. При их хранении происходит окисление двойных связей с образованием короткоцепочечных альдегидов и карбоновых кислот: масла прогоркают, приобретая неприятный запах и вкус. В пищевой промышленности для повышения срока хранения масел и повышения их стабильности при нагревании (жарке) их подвергают частичному гидрированию. При этом двойные связи восстанавливаются, и, как это свойственно насыщенным жирным кислотам, повышается температура плавления и увеличивается срок хранения таких жиров. Так, например, получают маргарин. Эти обстоятельства делают восстановленные жиры более пригодным продуктом для
144

пищевого производства. К сожалению, процедура частичного восстановления сопровождается изомеризацией оставшихся двойных связей, т.е. часть цис-двойных связей превращаются в транс-двойные. Показано, что употребление транс-изомеров жирных кислот, часто называемых просто транс-кислотами или транс-жирами, увеличивает риск сердечно-сосудистых заболеваний. В настоящее время на использование частично гидрированных жиров в ресторанах и кафе быстрого питания некоторых стран (Дания) и городов (Нью-Йорк) наложен запрет.
4.2. Структурные липиды Глицерофосфолипиды или фосфоглицериды представляют собой сложные эфиры
жирных кислот и трехатомного спирта глицерина, у которых в качестве одной из
кислотных групп в положении 3 находится остаток фосфорной кислоты или ее эфиры с
рядом спиртов (Рис. 4.4). Глицерофосфолипиды называют как соединения, производные
исходной фосфатидной кислоты (Рис. 4.4) в зависимости от названия входящего в состав
спирта: фосфатидилэтаноламин, фосфатидилсерин и т.д.
Рис. 4.4. Структурные формулы глицерофосфолипидов.
145

Глицерофосфолипиды – это большая и разнообразная группа соединений, главным свойством которых является их способность образовывать так называемые билипидные слои при соприкосновении с гидрофильным (водным) окружением. Именно билипидные слои являются основным структурным элементом клеточных мембран. Мембранные липиды являются амфифильными молекулами, в их составе можно выделить гидрофобную часть, образованную эфирами жирных кислот, и гидрофильную часть – заряженную головку молекулы, образованную остатком фосфорной кислоты (Рис. 4.5).
Рис. 4.5. Молекулы фосфолипидов амфифильны, в них можно выделить гидрофобный участок или «хвост» (эфиры жирных кислот) и полярную, заряженную
«головку», как это показано на примере холинфосфоглицерида (лецитина).
При контакте с водой молекулы такого типа ориентируются совершенно определенным образом – полярная головка молекулы обращена к воде, а гидрофобный хвост – наружу. При активном перемешивании такой бифазной системы молекулы фосфолипидов могут образовывать энергетически выгодные структуры: сферические
146
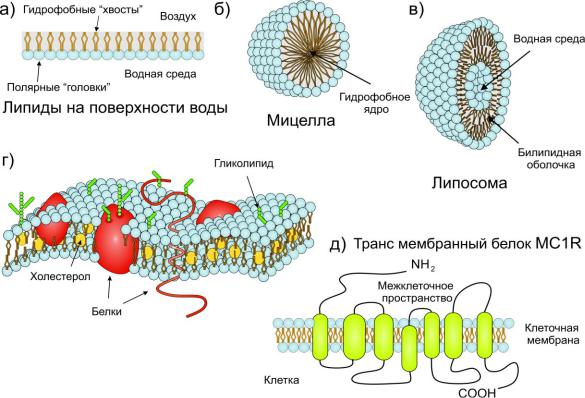
мицеллы – частицы с гидрофобным ядром и полярной поверхностью, либо липосомы –
частицы, образованные билипидным слоем, внутри которых находится водное
содержимое (Рис. 4.6). Примерно так организованы и клеточные мембраны. Современные
представления описывают клеточную мембрану как постоянно меняющуюся подвижную
структуру, основу которой составляет билипидный слой, который обеспечивает с одной
стороны сохранность внутриклеточного содержимого, а с другой – контакты живой клетки с окружением. Для этого на мембране локализованы различные белки,
гликопротеины и гликолипиды. Белки локализованы по-разному: на внешней, внутренней
стороне мембраны, а также могут пересекать ее несколько раз (Рис. 4.6).
Рис. 4.6. а) Глицерофосфаты при контакте с водной средой образуют структуры, в которых гидрофильная головка молекул обращена к водной фазе, а гидрофобные хвосты – от нее. б) Молекулы глицерофосфатов в водной среде формируют капли (мицеллы), внутри которых сосредоточены гидрофобные хвосты жирных кислот, а снаружи – полярные или заряженные головки. в) Крупные капли захватывают внутрь воду и формируют двойной слой – билипидную оболочку. К внешней и внутренней воде в этих частицах (липосомах) обращены полярные головки, а внутри слоя находятся гидрофобные хвосты жирных кислот. г), д) Клеточная мембрана образована билипидным слоем, на котором сосредоточены различные молекулы, обеспечивающие «общение» клетки с внешней средой.
147

Эти молекулы играют роль каналов (в том числе и активных), по которым происходит массообмен клетки, а также различного рода рецепторов, через которые внутрь клетки поступают различные стимулы.
В целом глицерофосфаты составляют 65-80% от массы клеточной мембраны.
Сфинголипиды представляют собой мембранные липиды, каркас молекул которых составляет не глицерин, а длинноцепочечный непредельный аминоспирт – сфингозин
(Рис. 4.7). В мембранах сфингозин представлен в виде церамидов, в молекуле которых аминогруппа ацилирована остатком жирной кислоты (Вопрос: где вы встречали похожую связь?). Церамиды, в молекуле которых последняя гидроксильная группа этерифицирована остатком фосфатидилхолина, называются сфингомиелинами. Также как и в случае глицерофосфатов, в молекуле сфингомиелина на одном конце находится сильнополярная головка (солевой мостик, образованный отрицательным зарядом остатка фосфорной кислоты и положительным зарядом на азоте холинового фрагмента) и два гидрофобных углеводородных хвоста на другом конце молекулы. Сфингомиелины сосредоточены в мембранах животных клеток, и особенно важное место они занимают в
миелине – мембранной оболочке нервных клеток, отсюда и происходит их название.
Рис. 4.7. Сфинголипиды – мембранные липиды, производные длинноцепочечного непредельного аминоспирта – сфингозина.
148

Группа церамидов, в молекулах которых к последней гидроксильной группе с помощью О-гликозидной связи присоединен олигосахарид, называются
гликосфинголипидами. Как правило, первым моносахаридным звеном в этих соединениях является остаток глюкозы. Самые сложные по структуре сфинголипиды –
ганглиозиды – представляют собой молекулы церамида, которые в качестве полярной головки содержат олигосахарид с одним или несколькими остатками N-ацетилнейрамовой
(или сиаловой) кислоты (см. пример на Рис. 4.8). Сиаловая кислота при рН=7
диссоциирована, что придает ганглиозидам отрицательный заряд. Основная функция этих соединений – клеточное узнавание: через них происходит взаимодействие клеток с нейромедиаторами, гормонами, токсинами, антителами и т.д.
Рис. 4.8. Ганглиозиды – это церамиды, которые в качестве полярной головки содержат олигосахарид с одним или несколькими остатками N-ацетилнейрамовой (или сиаловой) кислоты.
4.3. Определение структуры липидов
Поскольку липиды нерастворимы в воде, при их выделении и анализе в отличие от белков и нуклеиновых кислот используются органические растворители. Фракция липидов отделяется от других соединений с помощью экстракции из гомогенизированной в водных средах биомассы (тканей животных, растений или биомассы бактерий)
149
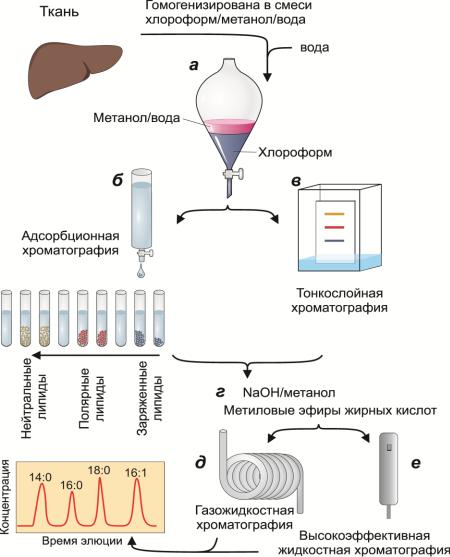
хлороформом с добавками этилового или метилового спиртов. При расслоении
полученной смеси хлороформная фракция образует хорошо разделяемый нижний слой, в
котором находятся липиды, а в верхнем водно-спиртовом слое остаются более полярные
молекулы белков, нуклеиновых кислот и углеводов (Рис. 4.9).
Рис. 4.9. Процесс определения липидного состава образца обычно включает следующие стадии: а) из образца липиды экстрагируют в органический растворитель; б) проводят адсорбционную хроматографию на колонке, заполненной силикагелем в градиенте полярного растворителя (спирта) в неполярном (хлороформ) или в) в тонком слое силикагеля (ТСХ); для определения строения липидов используют высокоэффективную жидкостную хроматографию (ВЭЖХ) или газо-жидкостную хроматографию (ГЖХ); г) чтобы перевести жк в газовую фазу (сделать их «летучими»), часто проводят реакцию этерификации с метанолом. Вопрос: какие соединения жирных кислот при этом получаются?
150
