
УП- Биоорганическая химия
.pdf
Из приведенных на этом рисунке дисахаридов только один – трегалоза, не имеет свободного аномерного атома и, стало быть, является невосстанавливающим углеводом.
Кстати, в природе трегалоза является основным компонентом жидкости, циркулирующей в организме насекомых (гемолимфы), где она служит источником «быстрой» энергии. При гидролизе одной молекулы трегалозы получается две молекулы глюкозы, необходимые для компенсации потерь энергии при полете насекомого.Далее на Рис. 3.11 приведены дисахариды, в состав которых входят разные мономеры, следовательно, это – гетеродимеры. Лактоза, или молочный сахар, состоит из β-галактозы и β-глюкозы,
объединенных 1→4 О-гликозидной связью. Полное название этого соединения О-β-D-
галактопиранозил -(1→4)-D-глюкопираноза, краткое – Gal(β1→4)Glc. Молочный сахар в природе встречается в молоке (до 7%, в зависимости от вида). Поскольку в этом сахариде имеется доступный для окисления аномерный атом С-1 (у глюкозного остатка), он обладает восстанавливающими свойствами.
Сахароза – дисахарид, состоящий из α-глюкозы и β-фруктозы, объединенных 1→2
гликозидной связью. Полное название этого соединения β-глюкопиранозил (1→2 ) β-
фруктофураноза, кратко: Glc(α1→β2)Fru. Обратите внимание, что у фруктозы в гликозидной связи также участвует аномерный углерод. Поэтому сахарозу можно назвать
Рис. 3.11. Гетеродисахариды, образованные молекулами глюкозы и фруктозы (сахароза) и галактозы и глюкозы (лактоза).
121
и «задом наперед», т.е. Fru(β2→α1) Glc. Поскольку оба аномерных атома участвуют в образовании гликозидной связи, сахароза является невосстанавливающим дисахаридом. Сахароза образуется в растительных клетках и является тем самым обычным сахаром на нашем столе.
Свойство сахаров восстанавливать металлы лежит в основе способа их качественного и количественного определения. С помощью реактива Бенедикта (щелочной раствор CuSO4) ранее выявляли наличие глюкозы в крови и моче при диагностике сахарного диабета. При исследовании содержания глюкозы в моче реактив Бенедикта смешивают с несколькими каплями мочи, пробу прогревают и после охлаждения наблюдают изменение окраски. В результате реакции происходит восстановление меди до Cu1+, и оксид меди Cu2O выпадает в виде осадка зеленого, желтого или красного цвета, в зависимости от содержания углевода в образце. При наличии зеленой окраски без осадка проба считается отрицательной.
Вопрос: В каких соединениях вы встречались с N-гликозидными связями?
3.3. Полисахариды
Основное количество углеводов в природе представлено в виде полимерных
молекул, где мономеры соединены гликозидными связями. Они имеют большую (иногда
громадную) молекулярную массу и общее их название – гликаны. Все это разнообразие
делят на 2 класса – гомо- (с одинаковыми мономерами) и гетерополимеры (с двумя и
более типами мономеров). В отличие, например, от белков, гликаны нельзя
охарактеризовать определенным значением молекулярной массы. Если полипептидная
цепь собирается в точном соответствии с матрицей, закодированной в молекулах ДНК, то
сборка гликанов осуществляется вне всякой матрицы, программа синтеза заключена в
самом ферменте, катализирующем полимеризацию мономеров, и специфической команды
для остановки синтеза не существует или таковая пока неизвестна.
Примером гомополисахаридов, выполняющих запасную функцию, являются крахмал
в растительных и гликоген в животных клетках. Мономерным звеном этих гликанов
является молекула глюкозы.
Крахмал содержится во всех клетках растений, но больше но основная масса его
сосредоточена в клубнях и семенах. Крахмал состоит из двух типов полимеров: 1)
длинных неразветвленных цепей амилозы, с молекулярной массой от нескольких тысяч
до миллионов дальтон, в которых мономеры глюкозы соединены α1→4 связями, а также
2) разветвленных цепей амилопектина (молекулярная масса до 100 миллионов дальтон), в
которых неразветвленные участки с α1→4 связями через каждые 24-30 остатков
соединяются разветвлениями с α1→6 связями.
122

Гликоген в целом повторяет структуру амилопектина. Однако разветвления
встречаются гораздо чаще – через каждые 8-12 остатков глюкозы. Запасы гликогена
сосредоточены в клетках печени (до 7% от веса этого органа) в виде нерастворимых
гранул. С этими гранулами связан комплекс ферментов, которые катализируют процессы
гидролиза и синтеза гликогена. Каждая линейная цепь гликогена оканчивается
разветвлением, и поэтому у этой молекулы есть только один восстанавливающий конец
(см. Рис. 3.12).
Рис. 3.12. В состав крахмала входят два типа полимеров глюкозы: линейный (амилоза), в котором мономеры соединены α1-4 гликозидной связью, и разветвленный (амилопектин), в котором между этими линейными участками находятся разветвления с α1-6 гликозидной связью.
Почему клетке удобнее хранить глюкозу в полимерном виде? Показано, что весь
гликоген в гепатоците содержит эквивалентную мономерную глюкозу в концентрации 0,4
123
М. При такой концентрации растворенной глюкозы неизбежно осмотическое проникновение в клетку большого количества воды из межклеточного пространства (там концентрация глюкозы всего 5 мМ), что привело бы к ее разрыву и лизису. Концентрация же нерастворимого полимерного гликогена составляет 0,01 мкМ.
Показано, что полимерная цепь амилозы, состоящая из глюкозных мономеров в конформации кресла, образует спирализованную структуру, характерную для гранул крахмала и гликогена (Рис. 3.12).
Примером гомополисахарида, который выполняет структурную функцию, является целлюлоза. Это прочное волокнистое нерастворимое в воде вещество, которое содержится в клетках стеблей травы и стволов деревьев. Целлюлоза является основным компонентом древесины. А хлопок состоит из нее почти на 98%. Мономером целлюлозы являются молекулы глюкозы, которые связаны в линейный полимер посредством β1→4 связей. Как вы помните, в составе крахмала и гликогена глюкоза представлена в α-конфигурации. Это единственная, казалось бы, незначительная разница является важным фактором,
определяющим свойства этих двух гомополимеров. В желудочно-кишечном тракте животных для расщепления крахмала и гликогена имеются ферменты α-амилазы,
гидролизующие α1→4 связи между остатками глюкозы. Для расщепления β1→4 связей у животных ферментов нет, и потому целлюлоза ими не усваивается. Таким образом,
практически неограниченный запас углеводов на нашей планете в виде целлюлозы растений не является источником пищи для человека. Считалось, что целлюлозу усваивают термиты, но оказалось, что в их желудочно-кишечном тракте находится симбиотический микроорганизм Trichonympha, который и секретирует фермент гидролизующий целлюлозу под названием «целлюлаза». Так же устроена система переваривания целлюлозы у жвачных животных, где симбиотические бактерии сосредоточены в специфическом отделе желудка (рубце). Фермент целлюлаза обнаружен также в проросшем зерне и грибах.
Пространственная структура целлюлозы представлена линейными полимерными цепями без разветвлений (Рис. 3.13), мономеры глюкозы находятся в конформации кресла
икаждый последующий мономер повернут вокруг гликозидной связи на 180º, как это показано для целлобиозы (см. Рис. 3.10). В результате цепи целлюлозы плотно упакованы благодаря сети водородных связей, образующихся как между молекулами одного слоя, так
имежду слоями. Поэтому процесс ее разложения целлюлазами, а также гниение
124

древесины занимают много времени. Растениями нашей планеты ежегодно синтезируется примерно 1012 тонн целлюлозы.
Хитин – еще один гомополимер, выполняющий структурную функцию. Это линейный полимер, мономерным звеном которого являются остатки N-
ацетилглюкозамина, соединенные 1β→4 гликозидными связями (Рис. 3.14).
Рис. 3.13. В целлюлозе мономеры β-глюкозы соединены связями 1→4. Длинные линейные полимеры плотно упакованы благодаря сети водородных связей внутри каждой цепи и между цепями (показаны штрихами).
Рис. 3.14. Структурная формула хитина — гомополимера ацетилглюкозамина.
Хитин образует длинные волокна, подобные целлюлозе, и также как она не переваривается животными
Единственным структурным отличием хитина от целлюлозы является наличие вместо гидроксильной группы по С-2 положению остатка ацетилированного производного аминогруппы (полное химическое название мономера хитина – N-ацетил-D-глюкозо-2-
амин). Хитин составляет основу панцирей приблизительно миллиона видов
125

членистоногих и по некоторым оценкам является вторым по распространенности полисахаридом после целлюлозы – ежегодно в биосфере его образуется около 109 тонн.
Гетерополимерные углеводы представлены широким спектром разнообразных по строению и назначению молекул. Рассмотрим несколько примеров.
Внеклеточное пространство в тканях животных заполнено так называемым внеклеточным матриксом. Одним из обязательных компонентов его являются гетерополисахариды под названием гликозаминогликаны. Как правило, они соединены с белками, т.е. являются составной частью протеогликанов и в свободном виде в организме не встречаются. Одним из звеньев этих молекул всегда является N-ацетиламиноглюкоза или ацетиламиногалактоза, а второй компонент – производное глюкуроновой кислоты.
Часто в них содержатся остатки серной кислоты. Присутствие карбоксильных и сульфогрупп придает молекулам гликозаминогликанов значительный отрицательный заряд. На Рис. 3.15 показана структура молекулы гиалуроновой кислоты.
Рис. 3.15. Структурные формулы гиалуроновой кислоты и хондроитин-4-сульфата.
126
В состав повторяющегося димера входят глюкуроновая кислота и N-ацетилглюкозамин,
соединенные β1→3 связями. Гиалуронаты образуют прозрачные и очень вязкие среды,
которые служат смазкой суставов, входят в состав стекловидного тела глаза позвоночных,
а также являются составляющей матрикса хрящей и сухожилий, придавая им прочность и эластичность. Это очень крупные молекулы, имеют до 50000 дисахаридных звеньев с молекулярной массой, достигающей 1 млн Да Хондроитин 4-сульфат состоит из остатков глюкуроновой кислоты и 4-сульфо-N ацетил-галактозамина. Этот гликозаминогликан имеет гораздо меньшие размеры (20-60 дисахаридных звеньев в цепи) и придает прочность хрящам, сухожилиям и стенкам аорты.
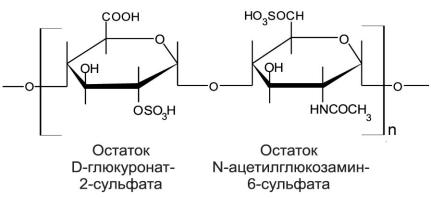
Рис. 3.16. Структура молекулы гепарина.
Гепарин состоит из повторяющихся димеров, в каждый из которых входят остаток глюкуронат-2- сульфата и остаток N-ацетилглюкозамин-6-сульфата (Рис. 3.16). Это соединение обладает противосвертывающей активностью, находится в межклеточном веществе ткани печени, легких, сердца, стенках артерий. Нетрудно видеть, что благодаря присутствию нескольких остатков кислот это соединение имеет значительный отрицательный заряд.
3.4. Гликоконъюгаты: протеогликаны и гликопротеины
Особый научный интерес вызывают соединения, представляющие собой ковалентные конъюгаты углеводов с полипептидами. Это большая группа веществ,
которые условно разделяют на гликопротеины и протеогликаны. В составе гликопротеинов (их еще называют гликозилированными белками) доля углеводов не превышает 15-20%, нет уроновых кислот, углеводные цепи короткие (≤ 15 звеньев)
нерегулярного строения. В протеогликанах доля углеводов, наоборот, велика – до 80-85%,
127

есть уроновые кислоты, углеводные цепи длинные, и, как правило, имеют регулярное строение. В клетке присоединение углеводного фрагмента к белку происходит коили посттрансляционно, то есть одновременно с синтезом белка или после него, действием комплекса специфических ферментов.
Соединения этого класса играют важнейшую биологическую роль медиаторов
(передатчиков) специфических взаимодействий клеток между собой и с внеклеточным содержимым; являются специфическими метками, указывающими направление транспорта или необходимость разрушения белка, если он дефектный или находится в избытке и т.д. Как правило, эти соединения располагаются на поверхности клеток,
образуя углеводный слой толщиной несколько нанометров. Внутри клеток они иммобилизованы в аппарате Гольджи, секреторных гранулах и лизосомах, а также в межклеточном матриксе.
В гликопротеинах углеводный компонент связан с белком связью между аномерным углеродом и гидроксилом боковой цепи серина, треонина или гидроксилизина – О-
гликозидной связью, либо через связь с амидным азотом аспарагина – N-гликозидной связью (Рис. 3.17).
Рис. 3.17. Углеводы присоединяются к белкам О-гликозидными связями к боковым радикалам серина или треонина либо N-гликозидными связями к боковому радикалу аспарагина. В случае коллагена углеводный фрагмент присоединяется по гидроксильной группе 4-гидроксилизина.
128
ВN-связанных олигосахаридах первым звеном всегда выступает β-
ацетилглюкозамин. При этом было обнаружено, что в таком полипептиде по соседству с сайтом гликозилирования через одну аминокислоту всегда находится треонин или серин.
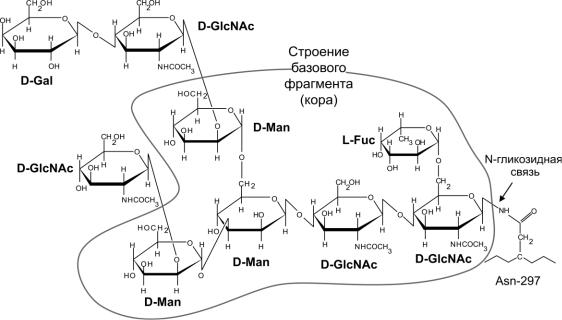
На Рис. 3.18 показан пример присоединения олигосахарида к молекуле иммуноглобулина. Олигосахарид присоединен к белку N-гликозидной связью, первым звеном является β-ацетилглюкозамин. Выделен базовый или кóровый фрагмент сахарида,
характерный для всех иммуноглобулинов, тогда как концевые участки могут иметь различное строение.
Большинство О-гликозидов присоединяются к белковой цепи через дисахарид β-
галактозил (1→3)-α-ацетилгалактозамин [Gal(β1→3α) GalNAc. Реже первым углеводным фрагментом бывают манноза, галактоза или ксилоза. Кстати, именно галактоза является первым звеном при гликозилировании структурного белка коллагена (Рис. 3.17). Здесь О-
гликозидная связь образуется при взаимодействии углевода с гидроксильной группой бокового радикала необычной аминокислоты – гидроксилизина (см. Рис.1-19).
Присоединение углеводного фрагмента к коллагену обеспечивает правильную структуру соединительной ткани, в которой коллаген является одним из основных белков.
Рис. 3.18. Иммуноглобулины являются гликопротеинами. Олигосахаридный фрагмент присоединен к полипептидной цепи N-гликозидной связью по боковому радикалу аспарагина. Выделен базовый фрагмент (кор), общий для иммуноглобулинов всех классов.
129

Олигосахариды, иммобилизованные на поверхности клеток, являются одними из самых известных иммунохимических маркеров. Например, отнесение группы крови в системе АВ0 базируется на комбинации различных олигосахаридных антигенов,
иммобилизованных на поверхности эритроцитов через пептид-гликозидные связи. В
случае группы ―0‖ кóровый олигосахарид представляет собой тетрамер Fuc(α1→2)
Gal(β1→4)GlcNAc(β2→3)Gal (Рис. 3.19). В случае ―A‖ ко второму галактозному фрагменту кóрового сахарида в положении С-3 присоединен еще и фрагмент ацетилгалактозамина; в случае ―B‖ по этому же положению присоединен остаток галактозы; в случае ―AB‖ на поверхности эритроцита находятся оба эти пятичленные олигосахарида.
В каждом организме нарабатываются иммуноглобулины против не свойственных ему антигенов. При переливании «чужой крови» происходит агглютинация чужих эритроцитов, что может привести к опасной закупорке сосудов.
Рис. 3.19. Олигосахаридные антигены на поверхности эритроцитов, определяющие группу крови системы АВ0.
Протеогликаны – это макромолекулы на поверхности клеток, они же являются основным компонентом внеклеточного матрикса (Рис. 3.20). Составы белковой и
130
