
- •1. Ферменти: визначення; властивості ферментів як біологічних каталізаторів
- •2. Класифікація та номенклатура ферментів, характеристика окремих класів ферментів
- •3. Будова та механізми дії ферментів. Активний та алостеричний (регуляторний) центри
- •4. Кофактори та коферменти. Будова та властивості коферментів; вітаміни як попередники в біосинтезі коферментів
- •5. Коферменти: типи реакцій, які каталізують окремі класи коферментів
- •6. Вітамін в1 (тіамін): будова, біологічні властивості, механізм дії
- •7. Вітамін в2 (рибофлавін): будова, біологічні властивості, механізм дії
- •8. Вітамін рр (нікотинова кислота, нікотинамід): будова, біологічні властивості, механізм дії
- •9. Вітамін в6 (піридоксин): будова, біологічні властивості, механізм дії
- •10. Вітамін в12 (кобаламін): біологічні властивості, механізм дії
- •11. Вітамін Вс (фолієва кислота): біологічні властивості, механізм дії.
- •12. Вітамін н (біотин): біологічні властивості, механізм дії
- •13. Вітамін в3 (пантотенова кислота): біологічні властивості, механізм дії
- •14. Вітамін с (аскорбінова кислота): будова, біологічні властивості, механізм дії
- •15. Вітамін р (флавоноїди): будова, біологічні властивості, механізм дії
- •16. Ізоферменти, особливості будови та функціонування, значення в діагностиці захворювань
- •17. Механізми дії та кінетика ферментативних реакцій: залежність швидкості реакції від концентрації субстрату, рН та температури
- •18. Активатори та інгібітори ферментів: приклади та механізми дії
- •19. Типи інгібування ферментів: зворотнє (конкурентне, неконкурентне) та незворотнє інгібування
- •20. Регуляція ферментативних процесів. Шляхи та механізми регуляції: алостеричні ферменти; ковалентна модифікація ферментів
- •21. Циклічні нуклеотиди (цАмф, цГмф) як регулятори ферментативних реакцій та біологічних функцій клітини
- •22. Ензимопатії – уроджені (спадкові) вади метаболізму вуглеводів, амінокислот, порфіринів, пуринів
- •23. Ензимодіагностика патологічних процесів та захворювань
- •24. Ензимотерапія – застосування ферментів, їх активаторів та інгібіторів в медицині
- •25. Принципи та методи виявлення ферментів у біооб'єктах. Одиниці виміру активності та кількості ферментів
- •26. Обмін речовин (метаболізм) - загальні закономірності протікання катаболічних та анаболічних процесів
- •27. Спільні стадії внутрішньоклітинного катаболізму біомолекул: білків, вуглеводів, ліпідів
- •28. Цикл трикарбонових кислот. Локалізація, послідовність ферментативних реакцій, значення в обміні речовин
- •29. Енергетичний баланс циклу трикарбонових кислот. Фізіологічне значення реакцій цтк
- •30. Реакції біологічного окислення; типи реакцій (дегідрогеназні, оксидазні, оксигеназні) та їх біологічне значення. Тканинне дихання
- •31. Ферменти біологічного окислення в мітохондріях: піридин-, флавін-залежні дегідрогенази, цитохроми
- •32. Послідовність компонентів дихального ланцюга мітохондрій. Молекулярні комплекси внутрішніх мембран мітохондрій.
- •33. Окисне фосфорилювання: пункти спряження транспорту електронів та фосфорилювання, коефіцієнт окисного фосфорилювання
- •34. Хеміосмотична теорія окисного фосфорилювання, атф-синтетаза мітохондрій.
- •35. Інгібітори транспорту електронів та роз’єднувачі окисного фосфорилювання
- •36. Мікросомальне окислення: цитохром р-450; молекулярна організація ланцюга переносу електронів.
- •37. Анаеробне окислення глюкози. Послідовність реакцій та ферменти гліколізу
- •2. Перетворення (ізомеризація) глюкоза-б-фосфату у фруктоза-6-фосфат (ферм. Фосфогексоізомеразою)
- •5. Взаємоперетворення двох фосфотріоз (доаф та г -3-ф ), що каталізується ферментом тріозофосфатізомеразою:
- •6.2. Перетворення 1,3-дифосфогліцерату на 3-фосфогліцерат (ферментом фосфогліцераткіназою)
- •38. Аеробне окислення глюкози. Етапи перетворення глюкози до со2 і н2о.
- •39. Окислювальне декарбоксилювання пірувату. Ферменти, коферменти та послідовність реакцій в мультиферментному комплексі
- •40. Порівняльна характеристика біоенергетики аеробного та анаеробного окислення глюкози, ефект Пастера.
- •41. Фосфоролітичний шлях розщеплення глікогену в печінці та м'язах. Регуляція активності глікогенфосфорилази.
- •42. Біосинтез глікогену: ферментативні реакції, фізіологічне значення. Регуляція активності глікогенсинтази.
- •43. Механізми реципрокної регуляції глікогенолізу та глікогенезу за рахунок каскадного цАмф-залежного фосфорилювання ферментних білків.
- •44. Роль адреналіну, глюкагону та інсуліну в гормональній регуляції обміну глікогену в м'язах та печінці.
- •45. Генетичні порушення метаболізму глікогену (глікогенози, аглікогенози).
- •1. Піруват у фосфоенолпіруват. – у дві стадії,
- •2. Фруктозо-1,6-дифосф. У фруктозо-6-фосф.:
- •3. Глюкозо-6-фосф. У глюкозу:
- •47. Глюкозо-лактатний (цикл Корі) та глюкозо-аланіновий цикли.
- •48. Глюкоза крові (глюкоземія): нормоглікемія, гіпо- та гіперглікемії, глюкозурія.
- •49. Гормональна регуляція концентрації та обміну глюкози крові.
- •50. Пентозофосфатний шлях окислення глюкози: схема процесу та біологічне значення
- •2.6 Ізомеризація 5 фрукт.-6-фосф. (ферм. Фосфогексоізомераза).
- •51. Метаболічні шляхи перетворення фруктози та галактози; спадкові ензимопатії їх обміну.
- •52. Катаболізм триацилгліцеролів в адипоцитах жирової тканини: послідовність реакцій, механізми регуляції активності тригліцеридліпази.
- •53. Нейрогуморальна регуляція ліполізу за участю адреналіну, норадреналіну, глюкагону та інсуліну
- •54. Реакції окислення жирних кислот (β-окислення); роль карнітину в транспорті жирних кислот в мітохондрії.
- •55. Окислення гліцеролу: ферментативні реакції, біоенергетика
- •56. Кетонові тіла. Реакції біосинтезу та утилізації кетонових тіл, фізіологічне значення.
- •57. Порушення обміну кетонових тіл за умов патології (цукровий діабет,голодування)
- •58. Біосинтез вищих жирних кислот: реакції біосинтезу насичених жирних кислот (пальмітату) та регуляція процесу.
- •1.Регуляція на рівні ацетил-КоА-карбоксилази.
- •2. Регуляція на рівні комплексу синтетази жирних кислот
- •59. Біосинтез моно- та поліненасичених жирних кислот в організмі людини
- •60. Біосинтез триацилгліцеролів та фосфогліцеридів
- •61. Метаболізм сфінголіпідів. Генетичні аномалії обміну сфінголіпідів – сфінголіпідози.
- •62. Біосинтез холестеролу: схема реакцій, регуляція синтезу холестеролу.
- •63. Шляхи біотрансформації холестерину: етерифікація; утворення жовчних кислот, стероїдних гормонів, вітаміну d3.
- •2. Біосинтез стероїдних гормонів
- •64. Циркуляторний транспорт та депонування ліпідів у жировій тканині. Ліпопротеїнліпаза ендотелію
- •65. Ліпопротеїни плазми крові: ліпідний та білковий (апопротеїни) склад. Гіперліпопротеїнемії
- •66. Патології ліпідного обміну: атеросклероз, ожиріння, цукровий діабет
- •67. Пул вільних амінокислот в організмі: шляхи надходження та використання вільних амінокислот в тканинах.
- •68. Трансамінування амінокислот: реакції та їх біохімічне значення, механізми дії амінотрансфераз.
- •1) Взаємодія амінокислоти, що втрачає аміногрупу, з піридоксальфосфатом з утворенням кетокислоти та піридоксамінфосфату:
- •2) Взаємодія а-кетокислоти, що акцептує аміногрупу, з піридоксамінфосфатом з утворенням нової амінокислоти та регенерацією піридоксальфосфату:
- •69. Пряме та непряме дезамінування вільних l-амінокислот в тканинах
- •70. Декарбоксилювання l-амінокислот в організмі людини. Фізіологічне значення утворених продуктів. Окислення біогенних амінів
- •1. Утворення фізіологічно активних сполук - гормонів, медіаторів, регуляторних факторів місцевої дії:
- •71. Шляхи утворення та знешкодження аміаку в організмі.
- •72. Біосинтез сечовини: послідовність ферментних реакцій біосинтезу, генетичні аномалії ферментів циклу сечовини
- •73. Загальні шляхи метаболізму вуглецевих скелетів амінокислот в організмі людини. Глюкогенні та кетогенні амінокислоти.
- •74. Біосинтез та біологічна роль креатину і креатинфосфату
- •75. Глутатіон: будова, біосинтез та біологічні функції глутатіону
- •76. Спеціалізовані шляхи метаболізму циклічних амінокислот – фенілаланіну, та тирозину
- •1. Шляхи метаболізму фенілаланіну
- •2. Шляхи метаболізму тирозину
- •2.3. Шлях синтезу тиреоїдних гормонів - реалізується в клітинах щитовидної залози і полягає в утворенні йодованих тиронінів.
- •77. Спадкові ензимопатії обміну циклічних амінокислот – фенілаланіну та тирозину
- •78. Метаболізм порфіринів: будова гему; схема реакцій біосинтезу протопорфірину IX та гему
- •3) Взаимодействие двух молекул δ -аминолевуленовой кислоты в реакции дегидратации с образованием порфобилиногена
- •4.1. Синтез із чотирьох молекул порфобіліногену уропорфіриногену ііі:
- •2)Білка уропорфіриноген ііі-косинтази.
1. Піруват у фосфоенолпіруват. – у дві стадії,
1) піруват+СО2+АТФ-> оксалоацетат+ АДФ + Фн. Ферм. піруваткарбоксилаза
2) оксалоацетат + ГТФ -> фосфоенолпіруват+СО2+ГДФ. Ферм. ФЕП-карбоксикіназа (у цитозолі та мітохондріях)
Транспорт оксалоацетату з мітох. в цитозоль – через човникові системи: малатна(основна, малатдегідрогеназа), аспартатна(аспартатамінотрансфераза), цитратна(цитратсинтаза)
2. Фруктозо-1,6-дифосф. У фруктозо-6-фосф.:
фрукт.-1,6-дифосф. + Н2О -> фрукт.-6-фосфат + Фн. Ферм. фруктозо-1,6-дифосфатаза (у печінці, нирках, епітеліоцитах кишечника)
3. Глюкозо-6-фосф. У глюкозу:
глюк-6-фосф.+Н2О -> глюкоза + Фн. Ферм. глюкозо-6-фосфатаза (у мембранах ЕПС гепатоцитів).
Отже, для синтезу 1 глюкози з 2 піруватів треба 6 макроерг. зв’язків
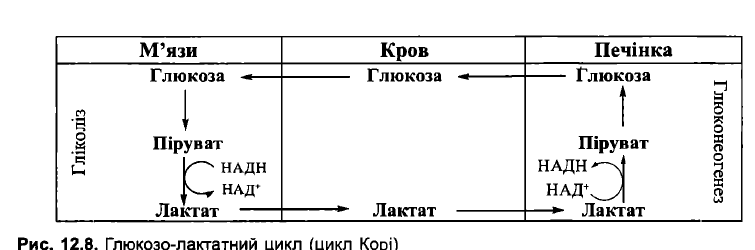
47. Глюкозо-лактатний (цикл Корі) та глюкозо-аланіновий цикли.
Глюкозо-лактатний (цикл Корі) пов’язує процеси утворення лактату в м’язовій тканині (анаер.гліколіз), його вихід у кров через плазмат.мембрани та використання лактату (після реокислення в піруват) у гепатоцитах для глюконеогенезу.
За
рахунок відновлення пірувату в лактат
у м’язах та його подальшого використання
в печінці, м’язи не тільки втрачають
«зайву» мол.кислот, яка утв. при
інтенс.фіз.праці, а й підтримують високий
НАД/НАДН (для активного гліколізу).
Глюкозо-аланіновий цикл:
А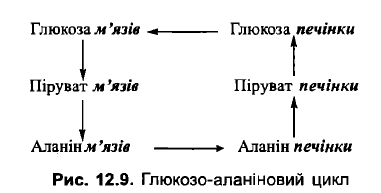 ланін,
який може утворюватися у скелетних
м'язах в оборотній реакції трансамінування
пірувату з глутаматом:
ланін,
який може утворюватися у скелетних
м'язах в оборотній реакції трансамінування
пірувату з глутаматом:
Піруват + Глутамат -> Aланін + а-кетоглутарат
Вивільняючись із працюючих м'язів у кров, аланін поглинається гепатоцитами і (після перетворення в піруват) використовується в глюконеогенезі (глюкозо-аланіновий цикл)
48. Глюкоза крові (глюкоземія): нормоглікемія, гіпо- та гіперглікемії, глюкозурія.
Цукровий діабет – патологія обміну глюкози.
нормоглікемія 3,3 - 5,5 ммоль\л
гіпоглікемія 2.5 и ниже
гіперглікемія више 6
Причини гіпоглікемії:
- Прийом інсуліну ( інсулін активує глікогенез)
- Первинні ензимопатії:
галактоземія ( галактокінази)
непереносимість фруктози (дефіцит фруктозо-1-фосфатальдолази)
- Глікогеноз (печінковий) ( глікоген не може розпадатися, глюкоза не утв, глікогенсинтаза)
- Інсулома (гіперінсулінізм)
- Наднирникова недостатність (хвороба Аддісона) гормони, що стимулюють глікогену
- Гіпофізарна недостатність
- Захворювання ШКТ (мала абсорбція моноз)
УСКЛАДНЕННЯ
Гіпоглікемічна кома – це втрата свідомості за рахунок критичного гіпоергозу нейронів.
Причини гіперглікемії:
• Аліментарна (фізіологічна)
• Стресорна
• Ураження ЦНС
• Печінкова недостатність (цироз)
( с глюкозы синтезируется гликоген,цирроз печени - накапливается глюкоза)
• Ендокринна:
Цукровий діабет
Іценко-Кушинга (гіперкортицизм)
Глюкагонома
Феохромацитома
Гіпофізарний гігантизм
Гіпертиреоз
УСКЛАДНЕННЯ
Діабетична гіперглікемічна кома
Гіперглікемічна гіперосмолярна кома.
Глюкозурі́я — наявність глюкози в сечі.
ГЛЮКОЗУРІЯ
У нормі сеча не містить глюкози, оскільки нирки здатні реабсорбувати (повертати до кровотоку) весь обсяг глюкози, що пройшов через нирковий клубочок в просвіт канальців нефрона. У переважній більшості випадків глюкозурія є симптомом декомпенсованого цукрового діабету як результат патологічного збільшення концентрації глюкози в крові. Рідкісним винятком є порушення реабсорбції в самій нирці — так звана ниркова глюкозурія. Глюкозурія веде до надмірної втрати води з сечею та дегідратації організму.
При перевищенні концентрації глюкози в крові вище ниркового порогу (8,88-9,99 ммоль / л) глюкоза починає надходити в сечу, і виникає глюкозурія
Цукр.Діаб – генетично обумовлений дефіцит інсуліну: зниження продукції бета-клітинами підшлункової залози або нездатність клітинних рецепторів реагувати на інсулін.
1)Інсулінозалежний – внаслідок руйнування (звичайно більше 90%) б-клітин через автоімунний процес. 10-15% усіх випадків, проявляється гіперглікемією та схильністю до кетонемії та кетоацидозу.
2)Інсулінонезалежний – збереження бета-клітин, але порушення специфічних реакцій на дію інсуліну або регуляцію його секреції під впливом підвищеної конц. глюкози крові.
