
- •1. Ферменти: визначення; властивості ферментів як біологічних каталізаторів
- •2. Класифікація та номенклатура ферментів, характеристика окремих класів ферментів
- •3. Будова та механізми дії ферментів. Активний та алостеричний (регуляторний) центри
- •4. Кофактори та коферменти. Будова та властивості коферментів; вітаміни як попередники в біосинтезі коферментів
- •5. Коферменти: типи реакцій, які каталізують окремі класи коферментів
- •6. Вітамін в1 (тіамін): будова, біологічні властивості, механізм дії
- •7. Вітамін в2 (рибофлавін): будова, біологічні властивості, механізм дії
- •8. Вітамін рр (нікотинова кислота, нікотинамід): будова, біологічні властивості, механізм дії
- •9. Вітамін в6 (піридоксин): будова, біологічні властивості, механізм дії
- •10. Вітамін в12 (кобаламін): біологічні властивості, механізм дії
- •11. Вітамін Вс (фолієва кислота): біологічні властивості, механізм дії.
- •12. Вітамін н (біотин): біологічні властивості, механізм дії
- •13. Вітамін в3 (пантотенова кислота): біологічні властивості, механізм дії
- •14. Вітамін с (аскорбінова кислота): будова, біологічні властивості, механізм дії
- •15. Вітамін р (флавоноїди): будова, біологічні властивості, механізм дії
- •16. Ізоферменти, особливості будови та функціонування, значення в діагностиці захворювань
- •17. Механізми дії та кінетика ферментативних реакцій: залежність швидкості реакції від концентрації субстрату, рН та температури
- •18. Активатори та інгібітори ферментів: приклади та механізми дії
- •19. Типи інгібування ферментів: зворотнє (конкурентне, неконкурентне) та незворотнє інгібування
- •20. Регуляція ферментативних процесів. Шляхи та механізми регуляції: алостеричні ферменти; ковалентна модифікація ферментів
- •21. Циклічні нуклеотиди (цАмф, цГмф) як регулятори ферментативних реакцій та біологічних функцій клітини
- •22. Ензимопатії – уроджені (спадкові) вади метаболізму вуглеводів, амінокислот, порфіринів, пуринів
- •23. Ензимодіагностика патологічних процесів та захворювань
- •24. Ензимотерапія – застосування ферментів, їх активаторів та інгібіторів в медицині
- •25. Принципи та методи виявлення ферментів у біооб'єктах. Одиниці виміру активності та кількості ферментів
- •26. Обмін речовин (метаболізм) - загальні закономірності протікання катаболічних та анаболічних процесів
- •27. Спільні стадії внутрішньоклітинного катаболізму біомолекул: білків, вуглеводів, ліпідів
- •28. Цикл трикарбонових кислот. Локалізація, послідовність ферментативних реакцій, значення в обміні речовин
- •29. Енергетичний баланс циклу трикарбонових кислот. Фізіологічне значення реакцій цтк
- •30. Реакції біологічного окислення; типи реакцій (дегідрогеназні, оксидазні, оксигеназні) та їх біологічне значення. Тканинне дихання
- •31. Ферменти біологічного окислення в мітохондріях: піридин-, флавін-залежні дегідрогенази, цитохроми
- •32. Послідовність компонентів дихального ланцюга мітохондрій. Молекулярні комплекси внутрішніх мембран мітохондрій.
- •33. Окисне фосфорилювання: пункти спряження транспорту електронів та фосфорилювання, коефіцієнт окисного фосфорилювання
- •34. Хеміосмотична теорія окисного фосфорилювання, атф-синтетаза мітохондрій.
- •35. Інгібітори транспорту електронів та роз’єднувачі окисного фосфорилювання
- •36. Мікросомальне окислення: цитохром р-450; молекулярна організація ланцюга переносу електронів.
- •37. Анаеробне окислення глюкози. Послідовність реакцій та ферменти гліколізу
- •2. Перетворення (ізомеризація) глюкоза-б-фосфату у фруктоза-6-фосфат (ферм. Фосфогексоізомеразою)
- •5. Взаємоперетворення двох фосфотріоз (доаф та г -3-ф ), що каталізується ферментом тріозофосфатізомеразою:
- •6.2. Перетворення 1,3-дифосфогліцерату на 3-фосфогліцерат (ферментом фосфогліцераткіназою)
- •38. Аеробне окислення глюкози. Етапи перетворення глюкози до со2 і н2о.
- •39. Окислювальне декарбоксилювання пірувату. Ферменти, коферменти та послідовність реакцій в мультиферментному комплексі
- •40. Порівняльна характеристика біоенергетики аеробного та анаеробного окислення глюкози, ефект Пастера.
- •41. Фосфоролітичний шлях розщеплення глікогену в печінці та м'язах. Регуляція активності глікогенфосфорилази.
- •42. Біосинтез глікогену: ферментативні реакції, фізіологічне значення. Регуляція активності глікогенсинтази.
- •43. Механізми реципрокної регуляції глікогенолізу та глікогенезу за рахунок каскадного цАмф-залежного фосфорилювання ферментних білків.
- •44. Роль адреналіну, глюкагону та інсуліну в гормональній регуляції обміну глікогену в м'язах та печінці.
- •45. Генетичні порушення метаболізму глікогену (глікогенози, аглікогенози).
- •1. Піруват у фосфоенолпіруват. – у дві стадії,
- •2. Фруктозо-1,6-дифосф. У фруктозо-6-фосф.:
- •3. Глюкозо-6-фосф. У глюкозу:
- •47. Глюкозо-лактатний (цикл Корі) та глюкозо-аланіновий цикли.
- •48. Глюкоза крові (глюкоземія): нормоглікемія, гіпо- та гіперглікемії, глюкозурія.
- •49. Гормональна регуляція концентрації та обміну глюкози крові.
- •50. Пентозофосфатний шлях окислення глюкози: схема процесу та біологічне значення
- •2.6 Ізомеризація 5 фрукт.-6-фосф. (ферм. Фосфогексоізомераза).
- •51. Метаболічні шляхи перетворення фруктози та галактози; спадкові ензимопатії їх обміну.
- •52. Катаболізм триацилгліцеролів в адипоцитах жирової тканини: послідовність реакцій, механізми регуляції активності тригліцеридліпази.
- •53. Нейрогуморальна регуляція ліполізу за участю адреналіну, норадреналіну, глюкагону та інсуліну
- •54. Реакції окислення жирних кислот (β-окислення); роль карнітину в транспорті жирних кислот в мітохондрії.
- •55. Окислення гліцеролу: ферментативні реакції, біоенергетика
- •56. Кетонові тіла. Реакції біосинтезу та утилізації кетонових тіл, фізіологічне значення.
- •57. Порушення обміну кетонових тіл за умов патології (цукровий діабет,голодування)
- •58. Біосинтез вищих жирних кислот: реакції біосинтезу насичених жирних кислот (пальмітату) та регуляція процесу.
- •1.Регуляція на рівні ацетил-КоА-карбоксилази.
- •2. Регуляція на рівні комплексу синтетази жирних кислот
- •59. Біосинтез моно- та поліненасичених жирних кислот в організмі людини
- •60. Біосинтез триацилгліцеролів та фосфогліцеридів
- •61. Метаболізм сфінголіпідів. Генетичні аномалії обміну сфінголіпідів – сфінголіпідози.
- •62. Біосинтез холестеролу: схема реакцій, регуляція синтезу холестеролу.
- •63. Шляхи біотрансформації холестерину: етерифікація; утворення жовчних кислот, стероїдних гормонів, вітаміну d3.
- •2. Біосинтез стероїдних гормонів
- •64. Циркуляторний транспорт та депонування ліпідів у жировій тканині. Ліпопротеїнліпаза ендотелію
- •65. Ліпопротеїни плазми крові: ліпідний та білковий (апопротеїни) склад. Гіперліпопротеїнемії
- •66. Патології ліпідного обміну: атеросклероз, ожиріння, цукровий діабет
- •67. Пул вільних амінокислот в організмі: шляхи надходження та використання вільних амінокислот в тканинах.
- •68. Трансамінування амінокислот: реакції та їх біохімічне значення, механізми дії амінотрансфераз.
- •1) Взаємодія амінокислоти, що втрачає аміногрупу, з піридоксальфосфатом з утворенням кетокислоти та піридоксамінфосфату:
- •2) Взаємодія а-кетокислоти, що акцептує аміногрупу, з піридоксамінфосфатом з утворенням нової амінокислоти та регенерацією піридоксальфосфату:
- •69. Пряме та непряме дезамінування вільних l-амінокислот в тканинах
- •70. Декарбоксилювання l-амінокислот в організмі людини. Фізіологічне значення утворених продуктів. Окислення біогенних амінів
- •1. Утворення фізіологічно активних сполук - гормонів, медіаторів, регуляторних факторів місцевої дії:
- •71. Шляхи утворення та знешкодження аміаку в організмі.
- •72. Біосинтез сечовини: послідовність ферментних реакцій біосинтезу, генетичні аномалії ферментів циклу сечовини
- •73. Загальні шляхи метаболізму вуглецевих скелетів амінокислот в організмі людини. Глюкогенні та кетогенні амінокислоти.
- •74. Біосинтез та біологічна роль креатину і креатинфосфату
- •75. Глутатіон: будова, біосинтез та біологічні функції глутатіону
- •76. Спеціалізовані шляхи метаболізму циклічних амінокислот – фенілаланіну, та тирозину
- •1. Шляхи метаболізму фенілаланіну
- •2. Шляхи метаболізму тирозину
- •2.3. Шлях синтезу тиреоїдних гормонів - реалізується в клітинах щитовидної залози і полягає в утворенні йодованих тиронінів.
- •77. Спадкові ензимопатії обміну циклічних амінокислот – фенілаланіну та тирозину
- •78. Метаболізм порфіринів: будова гему; схема реакцій біосинтезу протопорфірину IX та гему
- •3) Взаимодействие двух молекул δ -аминолевуленовой кислоты в реакции дегидратации с образованием порфобилиногена
- •4.1. Синтез із чотирьох молекул порфобіліногену уропорфіриногену ііі:
- •2)Білка уропорфіриноген ііі-косинтази.
18. Активатори та інгібітори ферментів: приклади та механізми дії
Активування ферментів. Речовини, які підвищують активність ферментів, одержали назву активаторів. Присутність активатора вкрай важлива для ферменту. До активаторів належать кофактори, іони металів, різноманітні модифікатори тощо. Субстрат у певних межах концентрацій є активатором - після досягнення насичених концентрацій субстрату активність ферменту не зростає. Субстрат полегшує формування потрібної конформації активного центру ферменту (індукція), підвищує його стабільність. Досить часто роль активаторів виконують іони металів: вони можуть входити до складу каталітичної ділянки активного центру ферменту; сприяти зв'язуванню субстрату з посадочною ділянкою ферменту (зв'язуючий місток); іноді метали можуть сполучатися не з ферментом, а із субстратом, утворюючи металосубстратний комплекс; вони можуть діяти непрямим шляхом, зв'язуючи присутній інгібітор тощо.
Алостерична регуляція ферментів. Активування ферментів може здійснюватися шляхом приєднання до алостеричного центра фермента специфічної модифікуючої групи (активатора), що сприяє зміні конформації фермента, його активного центра та, як наслідок, прискоренню ферментативної реакції (алостерична активація). Вона характерна для олігомерних ферментів, які складаються з кількох протомерів або мають доменну структуру. У центральних метаболічних шляхах вихідні речовини можуть виступати активаторами ключових ферментів, при цьому алостеричній активації підлягають ті ферменти, які каталізують ключові реакції заключних етапів метаболічного шляху:
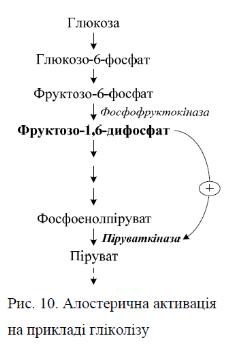
У якості прикладу розглянемо гліколіз – специфічний шлях розпаду глюкози: при утворенні надмірної кількості фруктозо-1,6-дифосфату спостерігається алостерична активація фермента піруваткінази (рис. 10).
Роль активаторів можуть виконувати також органічні речовини (жовчні кислоти посилюють дію ліпази підшлункової залози) та неорганічні (іони хлору є активаторами амілази слини; іони водню посилюють активність пепсину).
Ковалентна модифікація ферментів – один із механізмів контролю метаболічних процесів, що може відбуватися шляхом зворотного фосфорилування-дефосфорилування, метилування, аденілування, АДФ-рибозилування білків-ферментів. Фосфорилують білки спеціальні ферменти протеїнкінази, які за допомогою залишку фосфату АТФ здійснюють фосфорилування серинового, тирозинового чи треонінового радикалу відповідного білка. Зворотну реакцію – дефосфорилування білків – каталізують протеїнфосфатазами. Субстратами протеїнкіназ є численні ферментативні білки (глікогенфосфорилаза, кіназа фосфорилази b, глікогенсинтаза, тригліцеридліпаза, піруватдегідрогеназа, ацетил–КоА-карбоксилаза тощо), деякі білки мембранних каналів, гістони хроматину тощо. Приєднання залишка фосфорної кислоти призводить до зміни конформації активного центра, при цьому результат може бути двояким: фосфорилування багатьох білків-ферментів трансформує їх у каталітично активну форму (фосфорилування глікогенфосфорилази, кінази фосфорилази b, тригліцеридліпази тощо), тоді як фосфорилування інших ферментативних білків (глікогенсинтази, β-ГОМК-редуктази) є, навпаки, механізмом їх інактивації (рис. 8).
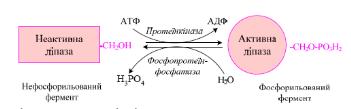
Рис. 8. Регуляція активності ліпази
Зміна активності фермента внаслідок фосфорилування зазвичай зворотна і регулюється гормонами, що дозволяє швидко змінювати активність ключових ферментів метаболічних шляхів.
Активація ферментів шляхом обмеженого протеолізу.
Активація низки ферментів (здебільшого травного тракту або плазми крові) може відбуватися протеолітичним шляхом. Такі ферменти синтезуються в неактивній формі у вигляді проферментів або зимогенів (попередників ферментів), активний центр яких замаскований додатковою ділянкою пептидного ланцюга, внаслідок чого субстрат не може взаємодіяти з активним центром. Наприклад, проферментом пепсину є пепсиноген, який синтезується головними клітинами шлункових залоз. Відщеплення від його молекули невеликого пептидного ланцюга за участі хлоридної кислоти шлункового соку призводить до утворення пепсину та формування його активного центра. Профермент трипсиноген, який утворюється в підшлунковій залозі, у дванадцятипалій кишці під впливом ферменту ентерокінази шляхом відщеплення гексапептиду перетворюється на трипсин. Після цього створюються умови, які сприяють утворенню активного центру ферменту, і трипсиноген перетворюється на трипсин. Ці процеси можуть також відбуватися аутокаталітично, тобто під впливом вже утвореного пепсину чи трипсину відповідно.
Активація шляхом білок-білкових взаємодій включає в себе два механізми: активацію в результаті приєднання регуляторних білків і зміну каталітичної активності внаслідок асоціації чи дисоціації протомерів фермента.
До регуляторних білків, які можуть чинити вплив на активність ферментів належать:
-кальмодулін-кальційвмісний білок, який, зв’язуючись з чотирма іонами кальцію, сприяє збільшенню цитозольної концентрації останнього при певних біохімічних та фізіологічних процесах у клітині. Утворений комплекс кальмодулін-кальцій здатний до активації багатьох ферментів, зокрема фосфодіестерази циклічних нуклеотидів, кінази легких ланцюгів міозину тощо;
-протеїназні інгібітори блокують активність тканинних протеїназ – ферментів, здатних розщеплювати власні білки організму. Найактивнішими протеїназами є α2 – макроглобулін та α1 – антитрипсин (α1- протеїназний інгібітор), які блокують активність серинових та інших протеїназ;
-антигемофільний глобулін А (фактор VІІІ згортальної системи крові). Цей білок бере участь в активації фактора Х, який запускає весь коагуляційний каскад, що призводить до утворення тромба.
Інгібування ферментів. Дія багатьох ферментів може бути загальмована, а в низці випадків і повністю припинена під впливом певних хімічних речовин – інгібіторів. Останні за тією або іншою причиною частково або повністю перешкоджають утворенню активного фермент-субстратного комплексу. Зокрема, токсичність багатьох отрут для живих організмів, лікувальні ефекти деяких лікарських речовин зумовлені їх інгібуючою дією на ферменти. Серед інгібіторів є як синтетичні речовини, так і природні метаболіти (приклади інгібіторів – наступне питання).
