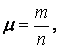- •1Техническая термодинамика
- •Тема 1. Основные термодинамические понятия и законы
- •1.1.Предмет и метод технической термодинамики
- •1.2.Термодинамическая система
- •1.3.Термодинамическое состояние и термодинамический процесс
- •1.4.Термические и калорические параметры состояния
- •1.4.1.Термические параметры состояния
- •1.4.2.Калорические параметры состояния
- •1.6.Уравнение состояния
- •1.7.Работа изменения объёма газа
- •Тема 2. Теплоёмкость газов
- •2.1.Массовая, объёмная и мольная удельные теплоёмкости
- •2.2.Средняя и истинная теплоёмкости
- •2.3.Теплоёмкости при постоянном объёме и давлении
- •2.4. Таблицы теплоёмкости
- •2.5.Теплоёмкость смеси рабочих тел (газовой смеси)
- •Тема 3. Первый закон термодинамики
- •3.1.Сущность первого закона термодинамики
- •3.2. Аналитическое выражение первого закона термодинамики для цикла и разомкнутого процесса
- •3.3. Уравнение первого закона термодинамики для движущегося рабочего тела
- •Тема 4. Термодинамические процессы
- •4.1.Схема анализа изменения состояния рабочего тела
- •4.2.Термодинамические процессы: изохорный, изобарный, изотермический, адиабатный, политропный
- •4.2.4.Адиабатный процесс
- •4.2.5. Политропный процесс
- •Тема 5. Второй закон термодинамики
- •5.1.Сущность и формулировки второго закона термодинамики
- •5.2.Обратимые и необратимые процессы
- •5.3.Круговые термодинамические процессы или циклы
- •5.4.Термический коэффициент полезного действия
- •5.5.Аналитическое выражение второго закона термодинамики
- •5.5.1.Цикл Карно
- •5.5.2.Соотношения, связанные с циклом Карно
- •5.6.Изменение энтропии в обратимых и необратимых процессах
- •Тема 6.Водяной пар
- •6.1.Основные понятия и определения
- •6.2.Схема парогенератора
- •6.3.Процесс парообразования в pv-координатах
- •6.4.Таблицы водяного пара
- •6.6.Процессы водяного пара на is-диаграмме
- •Тема 7. Тепловые двигатели
- •7.1.Классификация и принцип действия поршневых двигателей внутреннего сгорания
- •7.2.Цикл д. В. С. С подводом тепла при постоянном объёме (цикл Отто)
- •7.3.Цикл д. В. С. С подводом тепла при постоянном давлении (цикл Дизеля)
- •Тема 8. Паросиловые установки
- •8.1.Принципиальная схема паросиловой установки
- •8.2.Цикл Ренкина
- •8.3.Влияние параметров пара на термический к. П. Д. Цикла Ренкина
- •8.4.Пути повышения экономичности паросиловых установок
- •Тема 9. Теплопроводность
- •9.1.Основные понятия и определения
- •9.2.Закон Фурье
- •9.3.Коэффициент теплопроводности
- •9.4.Дифференциальное уравнение теплопроводности в плоской стенке при граничных условиях первого рода
- •9.4.1.Дифференциальное уравнение теплопроводности
- •9.4.2.Краевые условия
- •9.4.3.Теплопроводность через плоскую стенку при граничных условиях первого рода
1.4.Термические и калорические параметры состояния
К термическим параметрам состояния относятся давление P, удельный объем v,температура Т.
К калорическим параметрам состояния относятся следующие основные термодинамические величины: энтропия S,внутренняя энергия U и энтальпия H = U + PV .
1.4.1.Термические параметры состояния
Давление — физическая величина, численно равная отношению нормальной составляющей силы к площади, на которую действует эта сила.
Единицей давления в СИ является Паскаль — давление, вызываемое силой в 1 Н, равномерно распределенной по поверхности площадью 1 м2 (1Па=1 Н/м2).
В табл. 1.1 приведены соотношения между ранее применявшимися единицами измерения давления и единицами давления в СИ.
Таблица 1.1 |
||||||
Единица |
Па |
бар |
кгс/см2 |
мм рт.ст. |
мм вод.ст. |
|
1 Па |
1 |
10-5 |
1,02·10-5 |
7,5024·10-3 |
1,02·10-1 |
|
1 бар |
105 |
1 |
1,02 |
7,5024·102 |
1,02·104 |
|
1 кгс/см2 |
9,8067·104 |
0,98067 |
1 |
735 |
104 |
|
1 мм рт.ст. |
133 |
1,33·10-3 |
1,36·10-3 |
1 |
13,6 |
|
1 мм вод.ст. |
9,8067 |
9,8067·10-5 |
10-4 |
7,35·10-2 |
1 |
|
Различают атмосферное, или барометрическое давление Pб, абсолютное давление Ра, манометрическое Рм, или избыточное Ризб давление, разрежение, или вакуум.
Давление, создаваемое атмосферным воздухом, называется барометрическим, или атмосферным.
Абсолютным давлением, называется давление отсчитываемое от нуля (абсолютного вакуума).
Избыточным, или манометрическим, давлением называется давление сверх атмосферного, то есть избыточное давление — это разность между абсолютным и барометрическим давлениями: Pизб = Pa - Pб.
Разрежением, или вакуумом, называется разность между атмосферным давлением и абсолютным давлением той среды, где измеряется давление. Если абсолютное давление газа или пара в сосуде ниже барометрического, то есть Pа < Pб, то разность Pв = Pa – Pб называется разрежением, или вакуумом.
Вакуум показывает, насколько давление газа (пара) меньше давления окружающей среды. Давление атмосферного воздуха измеряется барометрами, избыточное давление — манометрами, а давление разрежения — вакуумметрами.
В термодинамических уравнениях всегда используют значения абсолютного давления ввиду того, что оно является параметром, характеризующим состояние термодинамической системы.
Атмосферное давление — величина переменная, поэтому в технике применяется нормальное атмосферное давление, Рб =0,10132 МПа (760 мм рт. ст.).
Температура тела есть мера его нагретости. Температура определяет направление передачи теплоты. Если два тела А и В имеют соответственно температуру Т1 и Т2 и Т1>Т2, то теплота переходит от тела А к телу В. При этом температура тела А уменьшается, а тела В - увеличивается.
С точки зрения молекулярно-кинетической теории температура есть мера интенсивности теплового движения молекул.
В термодинамике рассматривают температуру как среднестатистическую величину, которая характеризует систему, состоящую из очень большого числа молекул (частиц), находящихся в хаотическом (тепловом) движении. Поэтому к единичным молекулам понятие температуры не применимо. При температуре абсолютного нуля тепловое движение молекул отсутствует. Эта предельная минимальная температура называется абсолютным нулем и является началом для отсчета температур. Понятно, что не может быть Т< 0, то есть абсолютная температура всегда положительна.
Температура, отсчитываемая от абсолютного нуля, называется абсолютной, а шкала температур называется шкалой Кельвина.
Практически измерять кинетическую энергию молекул газа непосредственно невозможно. Поэтому для измерения температуры используют различные косвенные методы. Температура измеряется при помощи различных термометрических устройств – (термометров).
Использование термометров основано на том факте, что два соприкасающихся тела с разными температурами через некоторое время приходят к состоянию теплового равновесия и принимают одинаковую температуру.
Численный отсчет температуры производится по шкале температур. За основную единицу измерения температуры принимают градус, имеющий разную величину в различных температурных шкалах. Шкала температур устанавливается путем деления разности показаний термометра в двух произвольно выбранных постоянных температурных точках, называемых реперными или опорными, на некоторое число равных частей — градусов.
Ввиду того, что выбор постоянных температурных точек и цены деления шкалы является произвольным, имеется ряд различных шкал температуры.
В настоящее время кроме абсолютной температуры применяются другие температурные шкалы, такие, например, как: Цельсия, Фаренгейта, Реомюра, Ранкина.
По шкале Цельсия (![]() )
приняты следующие постоянные температурные
точки: О°C — температура таяния льда,
100°C — температура кипения воды при
нормальном атмосферном давлении.
)
приняты следующие постоянные температурные
точки: О°C — температура таяния льда,
100°C — температура кипения воды при
нормальном атмосферном давлении.
В 1724 г. Фаренгейт предложил термометр, в качестве реперных точек которого приняты: +212°F — температура кипения воды при нормальном атмосферном давлении; +32°F - температура таяния льда. Разность температур кипения воды и таяния льда по шкале Фаренгейта равна 212°— 32° = 180 °F, а по шкале Цельсия — 100°C. Следовательно, 1°F соответствует 5/9 °C, а 1°C — 1,8°F.
Шкала Реомюра (![]() )
имеет следующие реперные точки: О°R —
температура таяния льда, 80°R — температура
кипения воды при нормальном атмосферном
давлении.
)
имеет следующие реперные точки: О°R —
температура таяния льда, 80°R — температура
кипения воды при нормальном атмосферном
давлении.
Шкала Ранкина (![]() )
— это шкала Фаренгейта, отсчитанная от
абсолютного нуля. В этой шкале температура
таяния льда
)
— это шкала Фаренгейта, отсчитанная от
абсолютного нуля. В этой шкале температура
таяния льда
![]() (T0=273,15
К) соответствует 491,67°Ra, а температура
кипения воды при нормальном атмосферном
давлении (T0=373,15 К) соответствует
671,67°Ra.
(T0=273,15
К) соответствует 491,67°Ra, а температура
кипения воды при нормальном атмосферном
давлении (T0=373,15 К) соответствует
671,67°Ra.
Решением Международного комитета мер и весов приняты две шкалы: термодинамическая температурная шкала, которая принята основной, и Международная практическая температурная шкала (МПТШ-68), выбранная таким образом, чтобы температура, измеренная по этой шкале, была близка к термодинамической. В основу построения термодинамической шкалы положен тот факт, что в циклах Карно, располагающихся между двумя адиабатами, разность температур изотерм считается постоянной, если в механическую работу превращаются одинаковые количества теплоты. Наиболее универсальной шкалой температур является абсолютная термодинамическая шкала температур — шкала Кельвина.
В шкале Кельвина используется единственная экспериментальная реперная точка — тройная точка химически чистой воды (в термодинамическом равновесии находятся три агрегатных состояния; лед, жидкая вода и пар). Этому состоянию соответствует температура 273,15К (0,01°С). Второй постоянной точкой является абсолютный нуль температур (0К). Кельвин — единица измерения температуры по термодинамической температурной шкале, равная 1/273,15 части интервала от абсолютного нуля температуры до температуры тройной точки воды.
Практическим осуществлением термодинамической шкалы температур является Международная практическая температурная шкала. В этой шкале используется одиннадцать реперных точек. В табл. 1.2 приведены значения основных реперных точек.
Таблица 1.2 |
||
Равновесное состояние |
МПШТ-68 |
|
T68 |
t68 |
|
Точка кипения кислорода |
90,188 К |
-182,962 0C |
Тройная точка воды |
273,16 К |
+0,01 0C |
Точка кипения воды |
373,15 К |
+100,0 0C |
Точка плавления цинка |
692,73 К |
+419,58 0C |
Точка плавления серебра |
1235,08 К |
+961,93 0C |
Точка плавления золота |
1337,58 К |
+1064,43 0C |
Температуры кипения и плавления даны при давлении 101325 Па |
||
Удельный объем вещества ν — это объем, занимаемый единицей массы данного вещества.
Плотность вещества ρ— величина, обратная удельному объему и определяющая количество вещества, заключенное в единице объема.
Единица плотности в СИ — кг/м3, в системе СГС — г/см3. Плотность и удельный объем зависят от температуры и давления, то есть от термодинамического состояния вещества. Обычно в справочниках приводятся их значения при нормальных физических условиях. За нормальные физические условия принимают давление, равное 101,325 кПа (760 мм рт. ст.), и температуру, равную О °С.
Количество вещества. Единицей количества вещества в СИ является моль. Кроме моля применяют кратные и дольные части от моля (кмоль, Ммоль и др.). Количество вещества — это физическая величина, определяемая числом структурных элементов (атомов, молекул, ионов, электронов). Моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг.
Молярной массой вещества называют отношение массы вещества к его количеству:
|
где μ — молярная масса. Если
![]() выразить
в кг,
выразить
в кг,
![]() —
в молях, μ — выразится в кг/моль.
—
в молях, μ — выразится в кг/моль.