
- •Лекция 7. Химические процессы и реакторы Виды химических реакторов
- •4.2. Процесс в химическом реакторе
- •4.2.1. Математическая модель процесса в химическом реакторе
- •4.2.2. Анализ процесса в химическом реакторе
- •4.3. ИзотермическиЙ процесс в химическОм реакторЕ
- •4.3.1. Режимы идеального смешения периодический и идеального вытеснения
- •4.3.2. Режим идеального смешения в проточном реакторе
- •4.3.3. Сопоставление непрерывных процессов в режимах идеального смешения и вытеснения
- •4.4. Неизотермический процесс в химическом реакторе
- •4.4.1. Режимы идеального смешения периодический и идеального вытеснения с теплообменом
- •Температурный режим в проточном реакторе идеального смешения
- •Сопоставление адиабатического процесса в проточных режимах идеального смешения и вытеснения и выбор эффективного ректора при протекании простых реакций аr q
- •Каскад ректоров ис (к-ис)
- •Состав и структура химико-технологической системы
- •Элементы хтс
- •Состояние хтс синтез и анализ хтс
- •Основы разработки эффективных хтс
- •Задачи синтеза и анализа хтс
- •Лекция 12
- •Анализ хтс
- •Основы расчёта материального баланса химико-технологической системы
- •1. Общий вид уравнений материального баланса
- •2. Химико-технологическая система и её расчётная схема
- •2.1. Материальный баланс элементов хтс
- •2. Общий вид уравнений теплового (энергетического) баланса
- •3. Форма представления материального баланса
- •1. Концепция полного использования сырьевых ресурсов
- •7) Комбинирование производств
- •2. Концепция полного использования энергетических ресурсов
- •4) Вторичные энергетические ресурсы
- •5). Энерго-технологическая система
- •3. Концепция минимизации отходов
- •4. Концепция эффективного использования оборудования
- •6) Совмещение процессов
- •7) Перестраиваемые (гибкие) химико-технологические системы
- •12.05.20. Лекция 14. ОПтимальные схемы реакторов ив и ис
- •5.6.1. Система химических реакторов
- •Примеры построения эффективных химических производств
- •Производство серной кислоты
- •Хтс производства азотной кислоты
Состояние хтс синтез и анализ хтс
Анализ ХТС
Чтобы судить о свойствах ХТС, показателях ее функционирования, эффективности управления процессами в ней, необходимо определить состояние ХТС.
Состояние, или режим, ХТС определяется параметрами (показателями) потоков (связей) и состоянием аппаратов (элементов)
Параметры потоков - химические, физико-химические и физические данные о потоке. К ним относятся:
параметры состояния: количество потока в единицу времени (расход), фазовый состав, химический состав, температура, давление, теплосодержание;
параметры свойств: теплоемкость, плотность, вязкость и другие.
Состояние элемента (аппарата, машины, агрегата) включают данные, от которых зависит изменение в элементе показателей потока. Это могут быть:
регулирующие воздействия, например температура хладагента, отводящего тепло из реактора, или подача пара в паровую турбину;
возмущения, возникающие при эксплуатации характеристики аппарата, например изменение условий процесса в реакторе вследствие дезактивации катализатора или в теплообменнике из-за загрязнения его поверхности.
Основы разработки эффективных хтс
Основу разработки (построения) составляют синтез и анализ ХТС
Задачи синтеза и анализа хтс
Выделим основные задачи синтеза и анализа ХТС
Синтез ХТС
Анализ ХТС![]()

|
Дано: сырье, материалы, виды Энергии и топлива, набор оборудования, т.е.
заданы входные
потоки
отходы будут
получены, т.е.
Надо:
операции и выбрать главные элементы (аппараты);
наилучшие технологические связи между элементами, которые формируют структуру ХТС;
|
Дано: структура
ХТС (первый вариант), входные потоки
Надо:
2) Исследовать свойства ХТС (надежность, чувствительность, устойчивость и др.) которые могут появиться при синтезе ТТС 3)Выбрав критерий эффективности (как правило, один из экономических показателей) провести технико-экономический анализ ХТС и ее оптимизацию. При невыполнении ааданного критерия эффективности -вернуться на стадию синтеза ХТС. |
Т.о. в процессе разработки ХТС происходит постоянная циркуляция от синтеза к анализу ХТС и наоборот, до получения в итоге желаемого варианта ее организации и функционирования.
Расчет ХТС определение параметров потоков в ХТС заданной структуры и с заданным состоянием ее элементов.
Очевидно, что при любых изменениях состояния потоков в элементе ХТС, ее подсистеме или ХТС в целом должны соблюдаться законы сохранения массы и энергии.
Пусть имеется ХТС, состоящая из теплообменника, реактора и системы разделения (см. слайд) В ней пунктирными линиями выделены как оболочкой один элемент - реактор (I), подсистема реактор с теплообменником (II) и вся ХТС (III). В каждую из этих "оболочек" какие-то потоки входят и какие-то выходят. Внутри каждой оболочки происходят какие-то изменения входящих в нее потоков в выходящие. Фактически каждая из "оболочек" есть подсистема ХТС. В соответствие с законами сохранения массы и энергии в стационарном состоянии должны соблюдаться следующие соотношения для каждого элемента ХТС или подсистем, как они были представлены выше:
сохранение массы для потоков
![]() ;
;
сохранение массы для каждого i-го компонента
![]() ;
;
сохранение энергии
![]() .
.
Представленные уравнения есть балансы равенства массы и тепла между входящими и выходящими потоками для каждого элемента или подсистемы ХТС. Связь между элементами не меняет состояние потока, и потому масса и энергия в нем не меняется. Таким образом, расчет ХТС представляет собой установление балансов массы и тепла для всех его элементов с учетом связей между ними . Такой расчет называют балансовым расчетом или просто балансом, различая материальный баланс и тепловой баланс химико-технологической системы и ее частей.
Материальный и тепловой балансы должны соблюдаться всегда, не зависимо от того, как протекают превращения потока внутри таких "оболочек"-подсистем. Поскольку изменение состояния потоков меняются в технологических аппаратах, сначала разберем составление материального и теплового балансов между входными и выходными потоками элементов ХТС, а затем – способы расчета балансов ХТС в целом с учетом связей между ее элементами. Химический состав и количество многокомпонентной смеси позволяет определить почти все свойства ее, рассчитать количество каждого компонента и, следовательно, производительность, расход исходной смеси, количество отходов и многое другое. Для расчета тепловых потоков также необходимы состав и количество материальных потоков. Поэтому материальный баланс необходим при любых расчетах ХТС, и с него начнем расчет состояния химико-технологической системы.
Заранее оговорим, что материальный баланс основан на законе сохранения массы веществ, и потому далее количества веществ и величины потоков будем определять, как правило, в массовых величинах, обозначаемых буквой G с необходимыми индексами.
Материальный баланс элемента химико-технологической системы с химическими превращениями
Химические превращения протекают в реакционном элементе (реактор, реакторный узел). Изменение химического состава реагирующей смеси описывается стехиометрическими уравнениями. Ранее были описаны правила и приемы их составления: они должны быть стехиометрически независимыми; их количество строго определяется; методами линейной алгебры можно исключить "лишние" стехиометрические уравнения; Напомним некоторые соотношения, нужные при расчете ХТС:
количество i-го
компонента 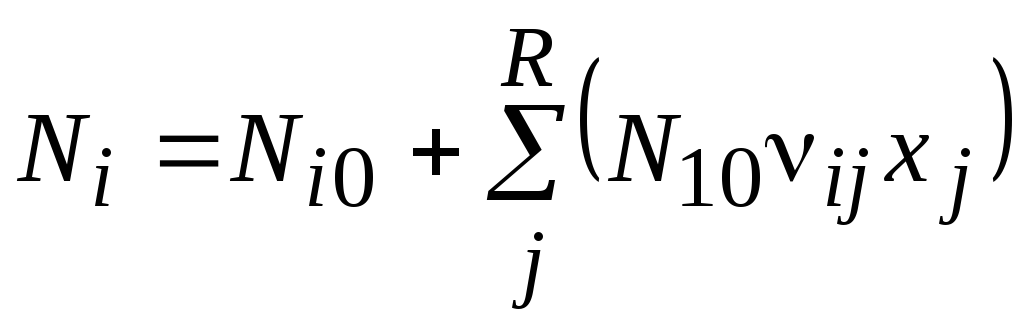 ;
;
концентрация i-го
компонента 
парциальное давление компонента pi = PCi
селективность по
i-му
продукту 
При составлении материального баланса обычно задаются степени превращения исходного вещества в стехиометрических уравнениях как результат химического превращения в реакционном элементе. Их должно быть столько, сколько есть независимых стехиометрических уравнений. Стехиометрические уравнения с "массовыми" стехиометрическими коэффициентами. В расчетах материального баланса реакционного элемента используют и другие формы записи химических превращений. Стехиометрические коэффициенты в химических уравнениях показывают количества компонентов, вступающих в химическое взаимодействие. Традиционно эти количества измеряют в молях. Но можно стехиометрические коэффициенты выразить в массовых величинах, умножив "мольные" коэффициенты на мольную массу.
Суммарное стехиометрическое уравнение. В ряде случаев необходимо получить материальный баланс подсистемы и даже ХТС в целом, где протекают последовательно ряд превращений. Рассмотрим пример: в производстве азотной кислоты определить количество НNО3, образующейся из 1 тонны аммиака. В химико-технологическом процессе протекают следующие реакции:
окисление аммиака
4NН3 + 5О2 = 4NО + 6Н2О
окисление оксида азота
2NО + О2 = 2NО2
хемосорбция диоксида азота
3NО2 + Н2О = 2НNО3 + NО
В абсорбционную колонну подается кислород, и образующийся оксид азота повторно окисляется до NО2.
4NН3 + 8О2 = 4НNО3 + 4Н2О
Конечно, такая реакция неизвестна. Но стехиометрическое уравнение показывает, в каких соотношениях реагенты вступают во взаимодействие друг с другом не зависимо от схемы превращений,
