- •Глава V. Общие сведения о паросиловых установках и их оборудовании 125
- •Глава VI. Паровые двигатели 134
- •Глава VII. Двигатели внутреннего сгорания 139
- •Глава VIII. Холодильные установки 145
- •Раздел 3. Тепловые процессы 149
- •Глава IX. Основы теплопередачи . 149
- •Глава X. Теплообменные аппараты 175
- •Глава XI. Трубчатые печи 189
- •Раздел 4. Массообменные процессы 216
- •Глава XII. Основы теории массопередачи 216
- •Глава XIII. Теория перегонки 229
- •Глава XIV. Ректификация 254
- •Глава XV. Абсорбция и десорбция 2s5
- •Глава XX. Очистка газов 348
- •Глава XXI. Гидравлика сыпучих материалов 355
- •Раздел 6. Химические процессы 371
- •Глава XXII. Основы теории химических процессов 371
- •Глава XXIII. Реакторные устройства 377
- •Глава I
- •1. Классификация основных процессов и аппаратов
- •2. Составление материальных и тепловых балансов
- •3. Определение внутренних потоков в аппарате
- •4. Системы единиц
- •5. Понятие о моделировании процессов и аппаратов
- •Раздел 1
- •Глава II
- •1. Основные понятия и определения
- •2. Физические свойства жидкостей
- •3. Элементы гидростатики
- •4. Элементы гидродинамики
- •3 Молоканов ю. К-
- •Глава III
- •1. Общая характеристика насосов
- •2. Центробежные насосы
- •3. Насосы для перекачки кислот и щелочей
- •4. Поршневые насосы
- •Раздел 2
- •Глава IV
- •3. Основные реакции горения топлива и расход кислорода и воздуха
- •4. Способы сжигания топлива различных ридов
- •Глава V
- •I. Направления развития теплоэнергетики в ссср
- •Мощность электростан- ций, гВт 1,14 1,23 6,92 22,1 66,7 142,5 165,6 217,5 228,3 237,8 Выработка электроэнер- гии, тВт-ч 2,04 0,52 26,3 104 292,3 638,7 740 1038 1111 1150
- •2. Принципиальная схема котельной установки
- •3. Основные типы котельных агрегатов
- •5 Молоканов ю. К-
- •4. Тепловой баланс котельной установки
- •5. Вспомогательные устройства
- •6. Использование отбросного тепла на нефтехимических комбинатах
- •Глава VI
- •1. Циклы паровых машин
- •2. Паровые турбины
- •Глава VII
- •1. Двигатели с внешним смесеобразованием
- •2. Двигатели с внутренним смесеобразованием (дизели)
- •3. Термодинамические циклы двигателей внутреннего сгорания
- •Глава VIII
- •1. Компрессионные холодильные установки
- •(VIII,2)
- •2. Абсорбционные холодильные установки
- •3. Пароэжекторные холодильные установки
- •Раздел 3
- •Глава IX
- •1. Способы передачи тепла и основные закономерности
- •2. Основные характеристики интенсивности передачи тепла
- •3. Основные схемы взаимного движения теплообменивающихся потоков
- •4. Средняя разность температур
- •5. Передача тепла через стенку
- •6. Передача тепла конвекцией
- •6 Молоканов ю. К-
- •7. Передача тепла лучеиспусканием
- •Излучение Космическое
- •0,05 0,05—0,10 0,10—2,00 2,00—350 350—700 700—4.10* 4-Ю5 и более
- •8. Передача тепла лучеиспусканием и конвекцией
- •9. Потери тепла в окружающую среду и меры по их уменьшению
- •Глава X
- •1. Основные виды теплообменных аппаратов
- •2. Кожухотрубчатые теплообменники
- •3. Теплообменники типа «труба в трубе»
- •4. Подогреватели с паровым пространством (рибэйлеры)
- •5. Теплообменные аппараты воздушного охлаждения
- •6. Тепловой расчет теплообменных аппаратов
- •Водяные конденсаторы паров бензина .... 230—450 Кипятильники, обогреваемые водяным паром 300—850 жидкими нефтепродуктами 140—350
- •7. Гидравлический расчет теплообменников
- •8. Особенности теплового расчета холодильников и конденсаторов
- •1. Назначение, типы и классификация трубчатых печей
- •Глава XI
- •2. Элементы конструкций трубчатых печей
- •3. Основные показатели работы трубчатых печей
- •4. Основные характеристики продуктов сгорания топлива
- •5. Тепловой баланс трубчатой печи
- •6. Тепловой расчет камеры радиации по методу н. И. Белоконя
- •7. Тепловой расчет камеры конвекции
- •V Krti
- •8. Расчет воздухонагревателя
- •9. Расчет пароперегревателя
- •10. Гидравлический расчет змеевика трубчатой печи
- •11. Газовое сопротивление и тяга
- •Раздел 4
- •Глава XII
- •1. Понятие о массообменных процессах
- •2. Способы выражения состава фаз
- •3. Понятие о равновесии между фазами
- •4. Основные законы процесса межфазного массообмена
- •5. Основное уравнение массопередачи
- •6. Закон аддитивности фазовых сопротивлений массопереносу
- •7. Средняя движущая сила процесса массопередачи
- •8. Материальный баланс процессов массообмена
- •10. Число теоретических ступеней контакта (теоретических тарелок)
- •Глава XIII
- •1. Основные законы термодинамики равновесных систем
- •2. Равновесные системы
- •3. Испарение и конденсация бинарных и многокомпонентных смесей
- •Глава XIV
- •1. Сущность процесса ректификации бинарных смесей
- •2. Принципиальное устройство ректификационной колонны
- •Материальный баланс ректификационной колонны
- •Тепловой баланс колонны
- •5. Уравнение рабочей линии
- •6. Определение числа теоретических тарелок графическим методом
- •7. Сопряжение составов потоков в питательной секции
- •8. Аналитические методы расчета
- •10. Способы создания орошения в колонне
- •12. Расчет температурного режима колонны
- •13. Выбор давления в колонне
- •14. Особенности расчета сложных колонн
- •15. Основные типы ректификационных колонн
- •16. Тарельчатые колонны
- •10 Молоканов ю. К.
- •Глава XV
- •1. Сущность процессов абсорбции и десорбции
- •3. Расчет числа теоретических тарелок в абсорбере
- •4. Тепловой баланс абсорбера
- •5. Расчет процесса десорбции
- •6. Тепловой баланс десорбера
- •Глава XVI
- •1. Сущность процесса экстракции
- •2. Основные методы экстрагирования
- •3. Основы расчета экстракторов
- •Глава XVII
- •Раздел 5
- •Глава XVIII
- •11 Молоканов ю. К. 321
- •Глава XIX
- •Глава XX
- •2. Газоочистительные аппараты
- •Раздел 6
- •Глава XXII
- •I 1 скорости реакции от
- •I температуры при оп-
- •Глава XXIII
- •101 Сл. Объемные 70
Абсорбция
и десорбция
*
Сорбция, сопровождаемая химическими
реакциями.Глава XV
1. Сущность процессов абсорбции и десорбции
Абсорбция
— процесс избирательного поглощения
компонентов газовой смеси жидким
поглотителем (абсорбентом). Процесс
выделения из абсорбента поглощенных
компонентов газа называется
десорбцией.В
отличие от ректификации процесс
абсорбции происходит в основном
однонаправленно, т. е. из газа извлекаются
соответствующие компоненты, а из
абсорбента в газовую фазу они практически
не переходят. Аналогичное замечание
относится и к десорбции.В
нефте- и газоперерабатывающей
промышленности процесс абсорбции
применяют для разделения, осушки и
очистки углеводородных газов. Из
природных и попутных газов извлекают
зтан, пропан, бутан и компоненты бензина,
сероводород (хемо- сорбция *), разделяют
газы пиролиза и каталитического крекинга
и т. п.Схематически
процесс абсорбции (десорбции) представлен
на рис. XV-1.Для
осуществления процесса абсорбции
необходимо, чтобы парциальное давление
извлекаемого компонента в газовой фазе
рг
было больше, чем в абсорбенте
рж.
Разность этих давлений Ар =
рг
— рж
определяет движущую силу процесса
абсорбции. При АР > 0 происходит процесс
абсорбции, при АР < 0 — процесс
десорбции. Процесс абсорбции (десорбции)
прекращается, когда система достигает
состояния равновесия, т. е.
рг
= Рг
= Рж-Поскольку
парциальное давление компонента
пропорционально его концентрации,
движущую силу при абсорбции (десорбции)
можно измерять также разностью
концентраций в газовой и жидкой
фазах: Аг/' =
у'
—
у'*
или
Ах' = х'* — х'
(см. ГЛ.
XII).
tf |
'
m |
6 |
|
|
|
|
|
|
\ * |
|
2 |
|
7 |
|
|
Процессы
абсорбции и десорбции обычно осуществляют
на одной установке, включающей абсорбер
и десорбер (рис. XV-2).
Регенерированный
абсорбент возвращают в абсорбер.
__
un+i
Gi
L0
(XV,3)
Xi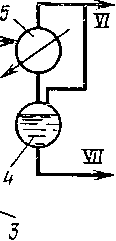
Gn+i
J^iYi
e
jjq
KiGi
Gn+1
LiiKfit
=
Ai (XV,4)
называется
фактором абсорбции,
а
Lo/Gn+i
= l (XV,4а)
удельным
расходом абсорбента.
AiYi^lXi (XV,5)
(Уп+1
- Ki)
=
(Хя
- х0) (XV,6)
Уп+1-Уг=ЦХп-Х0) (XV,7)
Уравнение
равновесия относительно приведенных
концентра-
ций
запишется следующим образом:Входящий
в это выражение комплекс величинТаким
образом уравнение равновесия примет
следующий вид:Материальный
баланс абсорбера в приведенных
концентрациях
запишется
так:илиОткуда
удельный расход абсорбента1
=
¥у+1~1г <XV'8)
уп
= уп+1
— у1
+ Аоуо (XV,9)
Ап
=
<?«+!
IXi+i—Yi)
HXi-Xi_1)=Yi+i~Yi
AIYI-Ai^I^YM-YI
у.
=
1
+
А[
Gi
При
идеальной подготовке абсорбента
Х0
«
0.Если
вместо Х0
и Х„ в уравнение (XV,7) подставить их
вы-
ражения
через концентрации газовой равновесной
фазы
Y0
и
Yn,
то
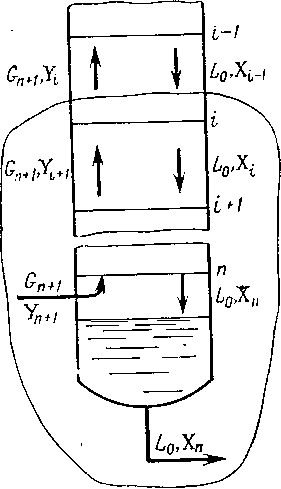
получимДля
произвольной
i-й
тарелки абсорбера (рис. XV-3)
материаль-
ный
баланс запишется следующим образом:илиВместо
Xt
и
Х£_х
подставим их выражения из уравнения
рав-
новесия,
т. е.Откуда
УгЧ1
tAiAlYl~x (xv'
10>Это
уравнение связывает составы газа на
двух смежных тарелках
абсорбера.
Чтобы выяснить влияние основных факторов
на про-или
Gn+iYi
+
L0xn
—
Gn+±Yn+1
+
i
Y2
+ A0Yq
1
+ Аг
(XV,
11)
Рис.
XV-3. Схема
потоков для нижней части абсорбера.
или
Yi
Lo
X,Из
рассмотрения этого выражения вытекает,
что содержание
извлекаемого
компонента в потоке газа на выходе из
абсорбератем
меньше, чем ниже концентрация
этого
компонента в абсорбенте на входе
Х0
и чем больше фактор абсорбции
А.
Последний
же тем больше, как это сле-
дует
из выражения (XV,4), чем больше
расход
абсорбента
L
и
меньше константа
равновесия
К. Таким образом, понижение
температуры
процесса благоприятствует
абсорбции
(меньше К).Материальный
баланс для нижней ча-
сти
абсорбера (рис. XV-3)
запишется
в
следующем виде:цесс
абсорбции, рассмотрим работу
однотарельчатого абсорбера (i
=
1). Тогда из уравнения (XV, 10) следует, что