
Хирургия аорты и магистральных артерий. Шалимов А.А
..pdf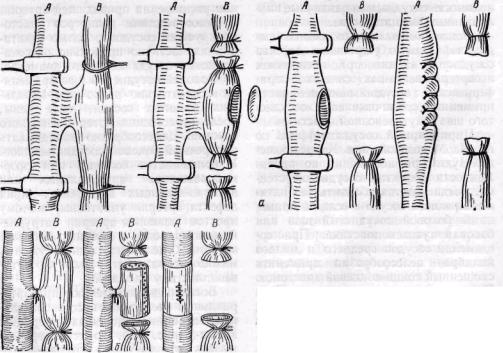
299
medwedi.ru
300
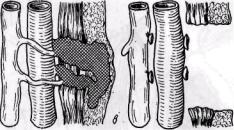
Рис. 144. Схема этапов операций Ратнера (а) и Караванова (б) при артерио-венозных свищах (по Б. В. Петровскому и Б.
О. Милонову, 1970). Л — артерия, В — вена 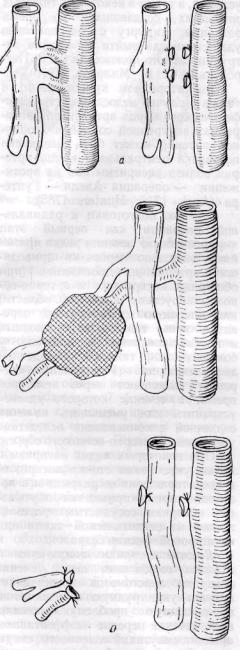
ного свища выполняют при узких сформировавшихся артерио-венозных свищах (рис. 143, а). Однако эту операцию очень редко удается произвести. Практически редко в настоящее время применяют при широком свище
Рис. 145. Схемы операций при врожденных артерио-венозных соустьях и аневризмах: я — перевязка и пересечение свищей; б — перевязка приводящих и отводящих сосудов, удаление аневризмы; в — удаление патологических соустий вместе с измененными тканями (по Ю. Ф. Исакову и Ю. А. Тихонову, 1974)
боковой трансвенозный сосудистый шов (операция Bickham, 1905, рис. 143, б), операцию Ратнера или Караванова (рис. 144). При врожденных артерио-венозных свищах и аневризмах применяют подобные операции, представленные на рис. 145.
В последние годы используют также метод эмболизации множественных артерио-венозных свищей (Na-tali u Merland, 1976, и др.).
301
Если в аневризматический мешок открывается несколько сосудов, может быть выполнен внутримешковой шов этих сосудов. Приводящую и отводящую артерии перевязывают, а восстановление артериального кровотока осуществляют методом обходного шунтирования. Мы в своей практике чаще всего использовали методы замещения артериальных аневризм венозным трансплантатом, резекцию аневризмы с анастомозом артерии конец в конец, боковую венопластику артерии, пересечение артерио-венозного соустья с анастомозом артерии конец в
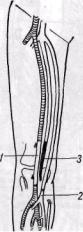
конец и боковым швом вены. У 1 больного выполнена резекция аневризмы подколенной артерии с пластикой ее аутовенозным трансплантатом и са-фено-подколенным венозным анастомозом (рис. 146).
Лигатурные и паллиативные операции. Сущность лигатурных операций
Рис. 146. Схема операции реконструкции сосудов при аневризме подколенной артерии, осложненной тромбозом подколенной вены:
/ — замещение подколенной артерии аутовеноз-ным трансплантатом; 2 — сафено-подколенный венозный анастомоз; 3 — тромбированная подколенная вена
состоит в перевязке сосудов с целью полного выключения аневризмы или артерио-венозного соустья. Они ликвидируют проходимость магистральных сосудов и таят в себе опасность развития тяжелой ишемии и гангрены конечности. На рис. 147 представлены схемы лигатурных операций. Операция Антиллуса состоит в перевязке артерии выше и ниже аневризмы, вскрытии ее и открытой тампонаде полости мешка. При операции Филагриоса перевязывают и пересекают приводящую и отводящую артерии, а также коллатерали, открывающиеся в полость аневризматиче-ского мешка с удалением последнего. Операция Матас-1 (Короткова — Ки-куци) состоит в прошивании и перевязке всех открывающихся в аневризматический мешок сосудов из полости мешка.
Паллиативные операции отличаются от описанных выше лигатурных тем, что направлены на замедление кровотока, способствуя тем самым тромбозу аневризмы. При трудно-удалимых аневризмах вследствие сложных анатомо-топографических условий, а также в некоторых тяжелых ситуациях, создавшихся во время операции, хирургу с их помощью удается иногда выйти из крайне затруднительного положения (Б. В. Петровский, О. Б. Милонов, 1970).
При вторичном кровотечении, а также в случае недосягаемости периферического конца артерии при аневризмах внутренней сонной и ягодичной артерий может быть выполнена перевязка центрального конца артерии вблизи аневризмы или на протяжении — операция Анеля — Гунтера (And, 1710; Hunter, 1785).
С целью подготовки к радикальной операции как первый этап хирургического лечения редко применяют операцию перевязки приводящих артерий на протяжении (при обширных аневризмах и артерио-ве-нозных соустьях ягодичной области) или операцию изолированной перевязки вены при артерио-венозных и комбинированных аневризмах у больных с тяжелой сердечной декомпенсацией. Радикальную операцию выполняют через некоторое время, в течение которого удается устранить или уменьшить явления сердечной декомпенсации вследствие уменьшения артерио-венозного сброса.
При некоторых видах аневризм с целью укрепления стенки аневризмы и предотвращения ее разрыва и в настоящее время применяют окутывание аневризм сосудистым протезом, лентой из синтетической ткани или из широкой фасции бедра.
Лечение аневризм анастомозов и области сосудистого шва. Лечение аневризм
анастомозов представляет актуальную, трудную и недостаточно решенную проблему. К сожале-
medwedi.ru

302
нию, лечение нередко неэффективное, процент ампутаций конечности, смертность больных, особенно от аневризм анастомозов аорты, остаются высокими. Сложность лечения в значительной мере зависит от наличия инфекции и кровотечения.
При разрыве аневризмы и кровотечении прежде всего следует оста-
Рис. 147. Схемы лигатурных операций Антиллуса (а), Филагриоса (б), Матас-1 (в) (по
Б. В. Петровскому и О. Б. Милонову, 1970)
новить кровотечение. Наиболее опасны разрывы аневризмы анастомоза протеза с аортой, которые очень часто приводят к летальному исходу. Обычно производят простое ушивание отверстия, перевязку сосудов, дренирование и подведение микроирригаторов для введения антибиотиков. При инфицировании протеза выздоровление бывает крайне редко, кровотечение обычно возникает повторно. Мы наблюдали 7 больных с аневризмами анастомоза протеза и брюшной аорты, осложнившихся разрывом и кровотечением. Всего им было выполнено 15 операций по поводу повторного кровотечения в забрюшинное пространство: ушивание отверстия — 8 операций, вскрытие гнойника и дренирование забрюшинного пространства — 3, выключение аневризмы и обходное аорто-бедренное шунтирование протезом вне гнойного очага — 1, подмышечнобедренное шунтирование веной — 1 операция. Удаление инфицированного протеза производилось как самостоятельное вмешательство или в сочетании с шунтированием вне гнойного очага. Выздоровели 3 больных, 4 — умерли. Для обходного аорто-бедренного шунтирования вне гнойного очага у 1 больного мы применили расширенный кзади правосторонний забрю-шинный доступ по Робу с резекцией XII ребра. Доступ оказался достаточно удобным для выделения инфраре-нального отдела аорты, наложения анастомоза протеза с аортой в этом участке и перевязки брюшной аорты с целью выключения кровоточащей аневризмы анастомоза аорты и инфицированного бифуркационного протеза.
Для проведения обходного шунта вне зоны гнойного очага и инфицированного аорто-бедренного или аорто-подвздошного протеза используют различные пути, представленные на рис. 148: 1 — через брюшную стенку, во влагалище прямой мышцы живота, анастомозируя протез с аортой в ее супраренальном отделе и с наружной подвздошной или бедренной артериями (Veith с соавт., 1964; Wolf, Pate, 1967); 2 — забрюшинный доступ от неинфицированного участка брюшной или грудной аорты к подвздошным или бедренным артериям (Blaisdell с соавт., 1961; Shaw, Baue, 1963); 3 и 4 — подкожно от подмышечной к бедренной артерии или от бедренной артерии здоровой конечности в случае односторонней реконструкции подвздошного сегмента.
При инфицированных аневризмах и инфицировании анастомоза протеза с бедренной артерией в области паха обходное шунтирование веной вне гнойного очага может быть осуществлено через
303
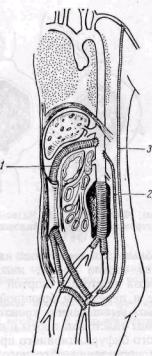
запирательное отверстие (Shaw и Baue, 1963; Mahoney, Whelan, 1966, и др., рис. 149) или через
Рис. 148. Методы обходного шунтирования вне зоны гнойного очага при инфицировании аорто-подвздошного протеза (объяснение в тексте) (no Rykowski и Noszczyk, 1974)
разрез в фасции между паховой связкой у места ее прикрепления к передней верхней ости подвздошной кости и подвздошной мышцей (Leather и Каг-mody, 1977, рис. 150).
Доступ к запирательному отверстию сверху осуществляют через поперечный или вертикальный разрез внизу живота над лобком. Прямую мышцу пересекают или отводят крючком. Брюшину смещают кверху и медиально, после чего достигают верхней части запирательного отверстия и выделяют наружную подвздошную артерию. Затем проводят разрез в верхней части бедра длиной 10—12 см непосредственно над сухожилиями приводящих мышц. Обнажают длинную и большую приводящие мышцы ближе к их началу. Длинную приводящую мышцу оттягивают лате-рально, чтобы обнажить запиратель-ный нерв, лежащий на короткой приводящей мышце. Тупо пальцем производят диссекцию между указанными мышцами, чтобы
достигнуть наружной запирательной мышцы. Запи-рательную мембрану рассекают по переднему краю запирательного отверстия кпереди и медиально по отношению к нерву и сосудам. Отверстие увеличивают тупо с помощью пальца сверху вниз, чтобы через него проходило 2 пальца. Канал на бедре может быть продлен вниз до гунте-рового канала, где обнажают поверхностную бедренную артерию для наложения анастомоза.
При латеральном пути обходного шунтирования выделяют подвздошные артерии забрюшинным доступом над паховой складкой. Наружную подвздошную артерию перевязывают. Крестообразно рассекают фасцию между паховой связкой и подвздошной мышцей ниже латерального прикрепления связки к передней верхней ости подвздошной кости. Через латеральный разрез на бедре разделяют продольно волокна m. tensor fasciae latae, затем между ней и m. sar-torius образуют туннель под паховой связкой, затем тупо продолжают туннель в медиальном направлении до гунтерового канала. Поверхностную бедренную артерию выделяют через типичный медиальный доступ в нижней трети бедра. Через образованный таким образом туннель проводят шунт и анастомозируют его с подвздошной и поверхностной бедренной (или подколенной) артериями.
Вслучае инфицирования анастомоза, осложнившегося кровотечением, показано удаление протеза.
Вслучае тяжелого кровотечения следует, прежде всего, спасать жизнь больного. Кровотечение остановить обычно удается только путем перевязки магистральных артерий, что приводит нередко к гангрене и ампутации конечности. Восстановление кровотока может быть осуществлено, если не
medwedi.ru

304
развилась гангрена конечности, во втором этапе, после заживления раны и излечения инфекции.
Рис. 149. Использование запирательного отверстия для проведения обходного шунта вне зоны гнойного очага при инфицировании анастомоза протеза с бедренной артерией
Использование синтетических протезов для обходного шунтирования вне зоны гнойного очага, как показывают также наши наблюдения, всегда связано с опасностью его инфицирования или во время операции, или гематогенным путем. Более перспективным является использование аутовенозного шунта.
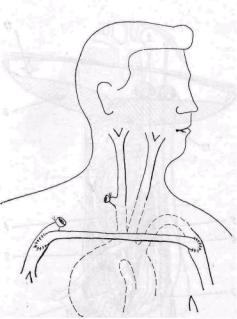
При инфицировании протезов и анастомозов подключичного артериального сегмента, осложнившегося кровотечением, может быть применено обходное шунтирование аутовеной из сосудистого бассейна контралате-ральной (здоровой) конечности, то есть аксиллярно-аксиллярное или аксиллярно-брахиальное шунтирование. В литературе имеются лишь единичные сообщения об этой операции при атеросклеротической окклюзии артерий (Jacobson, Baron, 1974; Lee Veen с соавт., 1974). Мы применили аксиллярно-брахиальное шунтирование у больного с инфицированием протеза правой подключичной артерии, осложнившегося кровотечением (А. А. Шалимов, 1976, рис. 151). После удаления протеза развилась тяжелая ишемия верхней конечности, в связи с чем произведено шунтирование вне зоны гнойного очага. В качестве трансплантата использована большая подкожная вена бедра. Шунт проведен подкожно впереди грудной клетки. Больной выздоровел, работает по специальности шофером.
305
Рис. 150. Использование латерального пути для шунтирования бедренной артерии вне зоны гнойного очага при инфицировании анастомоза протеза с бедренной артерией:
1 — a. iliaca externa; 2 — a. femoralis communis; 3 — a. femoralis profunda; 4 — a. femoralis su-perficialis; 5 — m. sartorius; 6 — m. iliacus; 7
— m. tensor fasciae latae; 8 — шунт; 9 — m. rectus femoris; 10 — m. psoas major; // — крестообразный разрез фасции для проведения шунта (по Leather и Karmody, 1977)
Лечение неинфицированных аневризм анастомозов более эффективно. Около 70% аневризм анастомозов развиваются в области общей бедренной артерии. Редко развиваются аневризмы в области шва сосуда, венозной заплаты, венозного трансплантата. Выбор метода операции должен быть индивидуальным. Рекомендуется удаление старого протеза или части протеза, прилежащей к анастомозу, и замена его новым протезом. При выраженном атеросклеротическом по-
Рис. 151. Контралатеральное аксиллярно брахиальное аутовенозное шунтирование при инфицированной аневризме анастомоза протеза и подключичной артерии
ражении поверхностной бедренной артерии и значительно суженном ее просвете можно соединить новый протез с глубокой артерией бедра конец в конец. При этом выкраивание каймы из стенки общей бедренной артерии вокруг устья глубокой артерии бедра делает возможным анастомозирование последней с протезом значительно большего диаметра.
При аневризмах анастомоза общей бедренной артерии больших размеров возникают значительные трудности в случае разрыва ее до того, как выделены из рубцово измененных тканей бедренные артерии. Временный гемостаз может быть выполнен с помощью перекрытия сосудов введенными в их просвет баллонными катетерами. Этот оперативный прием позволяет продолжить в последующем обнажение артерий. При больших аневризмах операция может быть выполнена в 2 этапа. Вначале выполняют обходное шунтирование области аневризмы через запирательное отверстие, а через 2—3 нед — резекцию аневризмы.
Следует уделять большое внимание профилактике инфекции. В первую очередь важна техника операции, предусматривающая щажение тканей и лимфатических сосудов, и строгое соблюдение условий асептики, поскольку загрязнение раны микроорганизмами происходит, как правило, во время операции извне, чаще всего через руки хирурга, а также в результате вскрытия инфицированных лимфатических сосудов у больных с очагами инфекции на конечности.
Мы наблюдали 33 больных с приобретенными аневризмами периферических артерий: подключичной — у 5 больных, подмышечной — у 2, плечевой — у 5, лучевой и локтевой —• у 2, бедренных — у 11, подколенной — У 6, сонных артерий — у 2 больных. При восстановлении артерий были использованы различные хирургические методы: трансплантация вены (10), боковая аутовеноплас-тика (6), циркулярный шов (8), боковой шов (1), аллопластика протезом (1), перевязка приводящих и отводящих сосудов (4), укрепление стенки аневризмы фасцией (2), ушивание стенки аневризмы швом с помощью УАП (1).
Ближайшие результаты лечения были хорошими и удовлетворительными. У 2 больных наблюдалось кровотечение в ранний послеоперационный период, в связи с чем 1 больной оперирован повторно. У 2 больных, поступивших с тромбозом аневризмы подколенной артерии, сосудов голени и тяжелой степенью ишемии, выполнены ампутации конечности в ранний послеоперационный период в связи с тяжелым общим состоянием вследствие интоксикации и
medwedi.ru
306
необратимых изменений в дисталь-ных отделах конечности. Одна из этих больных умерла на 9-е сутки после операции вследствие почечной недостаточности и декомпенсации сахарного диабета. За период с 1972 по 1977 г. в нашей клинике обследованы 60 больных с врожденными ангиодисплазиями типа синдрома Вебера — Рубашова и Клиппеля — Треноне. 17 больным с синдромом Вебера — Рубашова произведена скелетизация магистральных артерий и перевязка артерио-венозных соустий, 3 из них — в несколько этапов. У 23 больных выполнена венэктомия с надфасциальной перевязкой коммуникантных вен, 5 — операция Линтона. У 12 больных произведено иссечение гемангиоматоза тканей с перевязкой приводящих сосудов.
307
ПРИНЦИПЫ ЛЕЧЕНИЯ БОЛЬНЫХ ПОСЛЕ ОПЕРАЦИЙ
НА ПЕРИФЕРИЧЕСКИХ АРТЕРИЯХ
Основными задачами в ранний послеоперационный период являются сохранение восстановленного кровотока и профилактика осложнений, в первую очередь тромбозов, кровотечений, нагноения ран и сосудистых трансплантатов.
Поддержание показателей общей и центральной гемодинамики является важнейшим условием профилактики тромбозов.
После реконструктивных операций на артериальных сосудах следует систематически, через 1— 2 ч, в течение первых суток осуществлять контроль за артериальным давлением и пульсом. Даже кратковременное падение артериального давления в ранний послеоперационный период может привести к тромбозу сосудов в месте операции.
Внезапное падение давления может быть обусловлено следующими основными причинами: 1) кровотечением в результате негерметичности сосудистого шва; 2) кровотечением из пересеченных сосудов после элек-трокоагуляционного гемостаза; 3) сер-дечяой недостаточностью, обычно вследствие инфаркта миокарда; 4) развивающимся токсикозом (метаболический ацидоз) вследствие включения ишемизированной конечности; 5) скрытым внутренним желудочнокишечным кровотечением на фоне антикоагулянт-ной терапии, а также вследствие развития стрессовых язв.
Для своевременной диагностики причины внезапного падения артериального давления следует осуществлять контроль гемоглобина, эритроцитов, гематокрита, по показаниям — ЭКГ, содержание трансаминаз.
Стабильность гемодинамики, особенно в первые сутки послеоперационного периода, в значительной мере зависит от адекватного поддержания гемодинамики и гемогидробаланса во время операции. В этом плане важнейшее значение имеют: 1) учет и своевременное восполнение потерянной жидкости и крови; 2) своевременная и адекватная коррекция метаболического ацидоза после включения в кровоток ишемизированной конечности.
При длительных и больших по площади операционного поля хирургических вмешательствах, как например, по поводу окклюзии брюшной аорты, может быть значительная кро-вопотеря — медленная и быстрая в момент включения в кровоток синтетических протезов. С целью поддержания гемогидробаланса мы руководствуемся следующими основными положениями: 1) целесообразно, чтобы объем переливаемой крови был в целом несколько (на 10—15%) меньше кровопотери; 2) общее восполнение жидкости должно несколько (на 10— 15% от общего объема жидкости) поевышать ее потерю; 3) обязательна инфузия реополиглюкина, гемодеза или желатиноля в количестве 400— 800 мл; 4) поддержание выделительной функции почек при операциях на аорте — контроль диуреза путем катетеризации мочевого пузыря, введение низкомолекулярных декстра-нов, эуфиллина, маннита по показаниям.
Коррекцию нарушений кислотно-щелочного равновесия (КЩР) и водно-солевого обмена проводят во время операции и в первые 2—4 дня послеоперационного периода. При окклюзионных заболеваниях магистральных артерий развивается регионарная гипоксия тканей конечности, характеризующаяся уменьшением насыщения кислородом тканей, угнетением тканевых окислительных реакций, переходом клеточного метаболизма на анаэробный путь. Последнее обстоятельство является причиной развития метаболического ацидоза в пораженной конечности, так как при анаэробном окислении углеводов возникает избыток органических нелетучих кислот, в частности пиро-виноградной (ПВК) и молочной (МК), которые являются конечными продуктами анаэробного гликолиза.
Выраженный ацидоз развивается в тканях при тяжелой, остро прогрессирующей ишемии. Нарастание ацидоза наблюдается при дополнительном выключении путей кровоснабжения конечности в связи с пережатием сосудов во время реконструктивной операции. Нарушение КЩР тесно взаимосвязано с нарушением водно-солевого обмена. В условиях метаболического ацидоза ткани становятся гидрофильными, что приводит к задержке значительного количества воды во внеклеточном пространстве.
medwedi.ru
308
Изучение кислотно-щелочного го-меостаза крови с помощью современных методов исследования (метод мик-ро-Аструпа) подтвердило, как показали и наши наблюдения, известное положение, что после включения в кровоток нижних конечностей после реконструкции аорто-подвздошного сегмента у большей части больных развивается декомпенсированный метаболический ацидоз, обусловленный поступлением в общий кровоток не-доокисленных продуктов обмена из пораженной конечности. Об этом свидетельствует также увеличение содержания в крови ПВК и МК. Изменения со стороны показателей электролитов плазмы крови характеризовались увеличением содержания калия, в то время как содержание натрия существенно не изменялось. Коррекция метаболического ацидоза должна проводиться немедленно и адекватно. С этой целью применяют 4% раствор бикарбоната натрия, который вводят внутривенно обычно за 5—10 мин до снятия зажимов с сосудов и включения ишемизированной конечности в общий кровоток. Особенно опасный метаболический ацидоз развивается у больных со значительной кровопотерей, с нарушениями сердечно-сосудистой деятельности, в шоковом состоянии.
При несвоевременной и неадекватной коррекции метаболического ацидоза развиваются патологические симптомы, в первую очередь со стороны сердечно-сосудистой системы (падение артериального давления, нарушение сердечного ритма, остановка сердца), органов дыхания и почек.
Коррекцию нарушений КЩР и водно-электролитного баланса обычно осуществляют после реконструктивных операций на аорте, а также у больных с тяжелой, продолжительной ишемией тканей конечностей. Определение содержания электролитов (К+, Na+) в крови, показателей КЩР методом микро-Аструпа в динамике позволяет своевременно выявить нарушения.
Интенсивную инфузионную терапию — 10% раствор глюкозы с инсулином, раствор Рингера — Локка, низкомолекулярные декстраны, белковые кровезаменители и кровь — проводят при соответствующих показаниях в зависимости от характера реконструктивной операции и состояния больного в течение 2—4 дней. Одновременно осуществляют контроль диуреза. При нарушении мочевыде-лительной функции проводят стимуляцию ее с помощью осмотических диуретиков, эуфиллина.
Эффективным средством улучшения регионарной гемодинамики, микроциркуляции в конечности и профилактики раннего послеоперационного тромбоза является введение ни -комолекулярных декстранов, гемо-деза в количестве 800 мл в сутки в течение 2—3 дней, а затем по 400 мл 2—3 дня. Введение реополиглюкина позволяет отказаться у значительной части больных от применения антикоагулянтов в ранний послеоперационный период, уменьшить частоту опасных послеоперационных осложнений, особенно кровотечений, и улучшить исходы операций.
Вопрос о назначении антикоагулянтов решают индивидуально в зависимости от характера и особенностей реконструктивной операции, состояния сосудов притока и оттока, вида использованных сосудистых трансплантатов и других факторов.
Гепарин назначаем с первого дня после операции через 4 ч обычно по 5000 ЕД внутримышечно: 1) после тромбэндартериэктомии из аорто-подвздошного сегмента, особенно при включении в кровоток одной глубокой бедренной артерии, при малом ее диаметре в сочетании с профундопластикой; 2) после операций длинного обходного шунтирования к Отдельным сохранившим просвет арте-териям голени или к дистальной части подколенной артерии; 3) после тромбэндартериэктомии из артерий малого диаметра, например глубокой артерии бедра, области развилки подколенной, берцовых, плечевой артерий как самостоятельной операции или в сочетании с обходным шунтированием; 4) у больных с тяжелой ишемией конечности и резко выраженными расстройствами микроциркуляции, отеком стопы и голени, ишемическим поражением мышц; 5) при сопутствующем тромбофлебите или посттром-бофлебитическом синдроме; 6) после реконструктивных операций у больных, страдающих облитерирующим эндартериитом.
В остальных случаях мы обычно не применяем гепарин. Некоторым больным назначаем гепарин не с первых суток, а в последующие дни послеоперационного периода: в случае применения синтетических протезов при наличии некоторых вышеуказанных показаний к назначению гепарина; у больных сахарным диабетом; при появлении признаков тромбоэмболи-ческих осложнений или
резко выраженного гиперкоагуляционного синдрома по данным коагуло- и тромбо-эластографии. Всем больным при отсутствии противопоказаний к применению антикоагулянтов, как правило, назначали с 3-го дня после операции в течение 6—12 мес антикоагулянты непрямого действия под контролем протром-бинового индекса.
