
- •Введение
- •Тема 1 токсикология поваренной соли
- •Тема 2 токсикология нитритов и нитратов
- •Тема 3 токсикология карбамида
- •Тема 4 токсикология соединений цинка, меди, бария и свинца
- •Тема 5. Токсикология соединений ртути токсикологический анализ при отравлении
- •Тема 6 токсикология соединений мышьяка
- •Токсикологический анализ
- •При отравлении ядовитыми веществами, извлекаемыми после минерализации органических веществметоды обнаружения мышьяка и лечение отравлений
- •Работа1. Метод качественного определения мышьяка
- •Тема7 токсикология фосфорорганических соединений
- •Тема 8 токсикология хлорорганических соединений
- •Тема 9 токсикология производных карбаминовой кислоты токсикологический анализ при отравлении производными карбаминовой кислоты
МЕТОДЫ
ХИМИКО-ТОКСИКОЛОГИЧЕСКОГО АНАЛИЗА
Введение
Методические указания по химико-токсикологическому анализу предназначены для проведения лабораторно-практических занятий по курсу токсикологии. В методических указаниях подробно изложен порядок определения токсических веществ в объектах ветеринарного надзора. Приведены используемые в настоящее время методы качественного и количественного анализа. В конце каждой темы дано задание по фармакотерапии отравлений различными группами препаратов, что позволяет комплексно подойти к решению проблем токсикологии. Тестовое программированное задание по теме способствует закреплению знаний студентов. Знакомить студентов с методическими указаниями целесообразно после прослушивания лекций и изучения соответствующего материала по учебным пособиям. Используя методические указания, студенты выполняют практическую работу по токсикологии, а также закрепляют полученный на лекциях материал.
Перед проведением лабораторных исследований студенты должны изучить теоретический материал по каждой теме занятий, используя следующую схему:
1. Общая характеристика группы.
2. Основные соединения,применяемые в сельском хозяйстве, их физико-химические свойства, токсичность.
3. Условия, способствующие отравлению животных и птиц.
4. Пути проникновения яда в организм.
5. Всасывание, распределение, биотрансформация и выделение яда.
6. Механизм токсического действия.
7. Клинико-физиологические изменения у животных.
8. Патологоанатомические изменения.
9. Диагностика отравлений.
10. Первая помощь и лечение отравлений.
11. Профилактика отравлений.
12. Вопросы реализации продуктов и кормов, содержащих токсические соединения.
Тема 1 токсикология поваренной соли
Работа 1. Определение натрия хлорида в содержимом желудка (метод Фольгарда)
Принцип метода. Ионы хлора осаждаются избыточным количеством азотнокислого серебра. Затем избыток последнего, не вступивший в реакцию с хлоридом, оттитровывают раствором роданида аммония в присутствии железоаммонийных квасцов, взятых в качестве индикатора. По разности результатов двух титрований определяют объем раствора серебра нитрата, израсходованного на осаждение ионов хлора.
Материальное оснащение: 0,1 н. раствор серебра нитрата; 0,1 н. раствор роданида аммония; насыщенный (40%-ный) раствор железо-аммонийных квасцов; азотнаякислота, разбавленная поттолам с водой; мерная колба на 100 мл; водяная баня; бумажный фильтр.
Ход опыта. 10 г материала переносят в мерную колбу на 100 мл, доливают водой до метки, нагревают на водяной бане при 80 °С в течение 30 мин. После охлаждения смесь фильтруют. К 25 мл фильтрата добавляют 20-25 мл 0,1 н. раствора серебра нитрата, 1,5-2 мл раствора квасцов и 5 мл разбавленной азотной кислоты. Смесь титруют 0,1 н. раствором роданида аммония до слабо-оранжевого цвета до появления не исчезающего при энергичном взбалтывании коричнево-розового окрашивания. Рассчитывают по формуле:
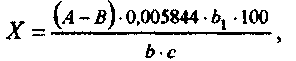
где X -содержание натрия хлорида, %;
А -количество прибавленного 0,1 н. раствора серебра
нитрата, мл;
В - количество 0,1 н. раствора роданида амония, пошедшего на титрование, мл;
b - объем водной вытяжки, взятой для анализа; Ьг- общий объем водной вытяжки, мл; с - навеска объекта,г;
0,005844 - количество натрия хлорида, г, соответствующее 1 мл 0,1 н. раствора серебра нитрата.
Работа 2. Определение натрия хлорида аргентометрическим методом (метод Мора)
Принцип метода основан на извлечении натрия хлорида из корма или патматериала дистиллированной водой с последующим титрова нием иона хлора раствором серебра нитрата в присутствии индикатора - калия хромата. После связывания иона хлора серебром избыток серебра нитрата реагирует с калия хроматом, образуя серебра хромат краснокирпичного цвета.
Материальное оснащение: 10 г патматериала, мерная колба на 100 мл, дистиллированная вода, термометр, бумажный фильтр, коническая колба, 10%-ный раствор калия хромата, ОД н. раствор серебра нитрата.
Ход опыта. Патматериал помещают в мерную колбу на 100 мл, заливают до 3/4 объема водой, хорошо встряхивают и нагревают на водяной бане до 80 °С. Через 30 мин охлаждают до комнатной температуры, периодически встряхивая, доводят водой до метки, встряхивают и фильтруют через бумажный фильтр в сухой стакан. 20 мл фильтрата переносят в коническую-колбу, приливают 1 мл 10%-ного раствора калия хромата и титруют 0,1 н. раствором серебра нитрата до появления неисчезающего кирпично-красного окрашивания. Содержание натрия хлорида вычисляют по формуле:
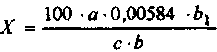
где X - содержание натрия хлорида, %;
а-количество раствора серебра нитрата, пошедшего на
титрование, мл;
Ъ - объем вытяжки, взятой для титрования, мл; Ь\— общий объем вытяжки, мл; с - навеска объекта, г;
0,00584 - количество натрия хлорида (г) связывающегося с 1 мл 0,1 н. раствора серебра нитрата.
Задание по фармакотерапии
Выписать в рецептах и объяснить действие препаратов:
1. Свинье - антидот при отравлении поваренной солью.
2. Двум коровам - 10%-ный раствор кальция хлорида для внутривенной инъекции.
3. Овце - кордиамин при сердечной слабости.
4. Свинье - слабительное средство при отравлении натрия хлоридом.
5. Собаке - слизь семян льна на два приема.
6. Рассчитать потребность в 10%-ном растворе кальция хлорида для 20 коров при отравлении поваренной солью.
Вопросы программированного контроля
I. Указать два вида животных и один вид птиц, наиболее чувствительных к избытку натрия хлорида.
1. Крупный рогатый скот. 2. Лошади. 3. Овцы. 4. Свиньи. 5. Собаки. 6. Куры. 7. Гуси. 8. Утки.
П. Отметите/основные биохимические изменения в крови при избыточном поступлении натрия хлорида в организм.
1. Увеличение количества ионов натрия в эритроцитах. 2. Увеличение количества ионов натрия в плазме. 3. Повышение содержания молочной кислоты. 4. Повышение содержания калия. 5. Понижение содержания калия. 6. Повышение содержания фосфора. 7. Понижение содержания фосфора.
III. Метод изоляции натрия хлорида из биологического материала.
1. Дистилляция с водяным паром. 2. Извлечение водой. 3. Экстракция органическими растворителями. 4. Минерализация. 5. Диализ.
IV. Отметить наиболее точный метод количественного определения натрия хлорида в биологическом материале.
1. Определение обратным титрованием. 2. Определение прямым титрованием. 3. Определение при помощи азотнокислой ртути.
V. С помощью каких методов можно обнаружить в моче хлориды.
1. Метод Мора. 2. Метод Воточека. 3. Метод Грисса.
VI. Какое количество хлоридов в содержимом желудка является токсичным для всех видов животных и птиц.
0,5%; 2) 1%; 3) 0,25%.
