
- •Министерство образования рф
- •Лекция 1 Заполнение зон электронами. Проводники, диэлектрики и полупроводники
- •Собственные полупроводники
- •Примесные полупроводники
- •Лекция 2 Принципы работы полупроводниковых приборов и их применение Диоды
- •Прямое включение: Обратное включение:
- •Стабилитроны
- •Варикапы
- •Светодиоды
- •Фоторезисторы
- •Люкс-амперная характеристика фоторезистора Фотоэлементы с p-n-переходом
- •Фотодиоды
- •Упрощенная структура фотодиода и его условное графическое обозначение
- •Термоэлектрогенераторы и термоэлектрохолодильники
- •Эффект Холла
- •Тензорезисторы
- •Лекция 3 Механические свойства материалов
- •Диаграмма растяжения
- •Пластичность и хрупкость. Твердость
- •Кривые растяжения материалов: а-хрупкого, б-пластичного
- •Способы измерения твёрдости
- •Для каждого материала существует установленная госТом сила вдавливания f
- •Твёрдость материала по Бринелю рассчитывают исходя из площади отпечатка.
- •Влияние энергии химических связей на свойства материалов
- •Теоретическая и реальная прочности кристаллов на сдвиг
- •Лекция 4 Кристаллизация металлов
- •Самопроизвольная кристаллизация
- •Кривые охлаждения металла
- •Изменение скорости образования зародышей (с. З.) и скорости роста кристаллов (с. Р.) в зависимости от степени переохлаждения
- •Несамопроизвольная кристаллизация
- •Получение монокристаллов
- •Схемы установок для выращивания монокристаллов
- •Аморфное состояние металлов
- •Термодинамическое обоснование диаграммы состояния сплавов, компоненты которых полностью растворимы в жидком и твердом состояниях Полиморфизм
- •Лекция 5 Влияние нагрева на структуру и свойства металлов
- •Холодная и горячая деформации
- •Термическая обработка металлов и сплавов Определения и классификация
- •Нагрев для снятия остаточных напряжений
- •Рекристаллизационный отжиг
- •Диффузионный отжиг (гомогенизация)
- •Лекция 6 Термохимическая обработка Назначение и виды химико-термической обработки
- •Цементация
- •Цианирование и нитроцементация
- •Азотирование
- •Диффузионная металлизация
- •Алитирование (Al)
- •Хромирование (Cr)
- •Борирование (b)
- •Силицирование (Si)
- •Поверхностно-пластическая деформация
- •Литье под давлением
- •Центробежное литье
- •Литье под низким давлением
- •Литье выжиманием
- •Лекция 8 Конструкционные материалы Общие требования, предъявляемые к конструкционным материалам
- •Прочность конструкционных материалов и критерии ее оценки
- •Классификация конструкционных материалов
- •Стали, обеспечивающие жесткость, статическую и циклическую прочности
- •Классификация конструкционных сталей
- •Влияние углерода и постоянных примесей на свойства стали
- •Диаграмма состояния железоуглеродистых сплавов
- •Превращения в сплавах системы железо-цементит
- •Диаграмма состояния Fe-Fe3c
- •Характерные точки диаграммы состояния железо-цементит
- •Углеродистые стали
- •Легированные стали
- •Лекция 9 Цветные сплавы Медные сплавы
- •Свойства промышленных латуней, обрабатываемых давлением
- •Сплавы на основе алюминия
- •Механические свойства алюминия
- •Сплавы на основе магния
- •Титан и сплавы на его основе
- •Механические свойства иодидного и технического титана
- •Лекция 10 Органические полимеры
- •Дополнительные компоненты полимерных композиций
- •Неполярные и слабополярные термопласты
- •Полярные термопласты
- •Термореактивные полимеры
- •Слоистые пластмассы
- •Металлопласты
- •Лекция 11 Неорганические материалы
- •Кристаллическая решетка графита
- •Неорганическое стекло
- •Ситаллы
- •Керамика
- •Лекция 12 Композиционные материалы Композиционные материалы с металлической матрицей
- •Композиционные материалы с неметаллической матрицей
- •Бороволокниты
- •Органоволокниты
- •Список литературы
Самопроизвольная кристаллизация
Самопроизвольная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние, характеризуемое уменьшением термодинамического потенциала G. С повышением температуры термодинамический потенциал вещества как в твердом, так и в жидком состоянии уменьшается, что показано на рисунке.
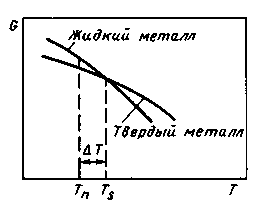
Изменение термодинамического потенциала в зависимости от температуры для металла в твердом и жидком состояниях
Температура, при которой термодинамические потенциалы вещества в твердом и жидком состояниях равны, называется равновесной температурой кристаллизации. Кристаллизация происходит в том случае, если термодинамический потенциал вещества в твердом состоянии будет меньше термодинамического потенциала вещества в жидком состоянии, т. е. при переохлаждении жидкого металла до температур ниже равновесной. Плавление - процесс, обратный кристаллизации, происходит при температуре выше равновесной, т. е. при перегреве. Разница между реальными температурами плавления и кристаллизации называется температурным гистерезисом.
Поскольку жидкий металл с присущим ему ближним порядком в расположении атомов обладает большей внутренней энергией, чем твердый со структурой дальнего порядка, при кристаллизации выделяется теплота. Между теплотой и температурой кристаллизации Тк существует определенная связь. Так как при равновесной температуре кристаллизации термодинамические потенциалы в жидком и твердом состояниях равны, то
![]()
![]() =>
=>
![]() =>
=>
Параметр ΔS = Q/TK характеризует упорядоченность в расположении атомов при кристаллизации. В зависимости от сил межатомной связи теплота кристаллизации для различных металлов изменяется от 2500 Дж/моль (Na, К и др.) до 20000 Дж/моль (W и др.).
Когда кристаллизуется чистый элемент, отвод теплоты, происходящий вследствие охлаждения, компенсируется теплотой кристаллизации. В связи с этим на кривой охлаждения, изображаемой в координатах температура-время, процессу кристаллизации соответствует горизонтальный участок:

Кривые охлаждения металла
При большом объеме жидкого металла выделяющаяся при кристаллизации теплота повышает температуру практически до равновесной (кривая а); при малом объеме металла выделяющейся теплоты недостаточно, вследствие чего кристаллизация происходит с переохлаждением по сравнению с равновесной температурой (кривая б).
Разница между равновесной (Ts) и реальной (Тn) температурой кристаллизации называется степенью переохлаждения ΔT. Степень переохлаждения зависит от природы металла. Она увеличивается с повышением чистоты металла и с ростом скорости охлаждения. Обычная степень переохлаждения металлов при кристаллизации в производственных условиях колеблется от 10 до 30 °С; при больших скоростях охлаждения она может достигать сотен градусов.
Степень перегрева при плавлении металлов, как правило, не превышает нескольких градусов.
В жидком состоянии атомы вещества вследствие теплового движения перемещаются беспорядочно. В то же время в жидкости имеются группировки атомов небольшого объема, в пределах которых расположение атомов вещества во многом аналогично их расположению в решетке кристалла. Эти группировки неустойчивы, они рассасываются и вновь появляются в жидкости. При переохлаждении жидкости некоторые из них, наиболее крупные, становятся устойчивыми и способными к росту. Эти устойчивые группировки атомов называют центрами кристаллизации (зародышами). Образованию зародышей способствуют флуктуации энергии, т. е. отклонения энергии группировок атомов в отдельных зонах жидкого металла от некоторого среднего значения. Размер образовавшегося зародыша зависит от величины зоны флуктуации.
Появление центров изменяет термодинамический потенциал системы ΔGобщ. С одной стороны, при переходе жидкости в кристаллическое состояние термодинамический потенциал уменьшается на VΔGυ (G1), с другой стороны, он увеличивается вследствие появления поверхности раздела между жидкостью и кристаллическим зародышем на величину, равную Sσ (G2):
ΔGобщ.
= -
VΔGυ
+ Sσ
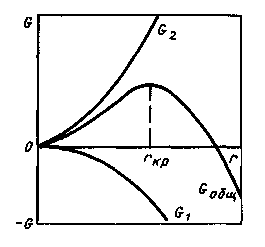
Изменение термодинамического потенциала при образовании зародышей в зависимости от их размера
Если принять, что зародыш имеет форму куба с ребром А, то общее изменение термодинамического потенциала
ΔGобщ.
= A3ΔGυ
+ 6A2
σ
Отсюда следует, что графическая зависимость изменения термодинамического потенциала от размера зародыша имеет максимум при некотором значении А, названном критическим. Зародыши с размером больше критического вызывают уменьшение ΔGобщ. и поэтому являются устойчивыми, способными к росту. Зародыши, имеющие размер меньше критического, нестабильны и растворяются в жидкости, поскольку вызывают увеличение ΔGобщ.
![]()
![]()
![]()
![]() =>
=> ![]() =>
=>
Скорость процесса и окончательный размер кристаллов при затвердевании определяются соотношением скоростей роста кристаллов и образования центров кристаллизации. Скорость образования зародышей измеряется числом зародышей, образующихся в единицу времени в единице объема; скорость роста - увеличением линейного размера растущего кристалла в единицу времени. Оба процесса связаны с перемещениями атомов и зависят от температуры. Графическая зависимость скорости образования зародышей и скорости их роста от степени переохлаждения представлена на рисунке.

