
- •1. Материальная точка. Система отсчета. Траектория, путь, перемещение. Скорость. Формулы пути и скорости.
- •2. Кинематика материальной точки. Путь, скорость, ускорение. Тангенциальное, нормальное, полное ускорение.
- •Модуль а полного ускорения в соответствии с теоремой Пифагора, равен:
- •3. Абсолютно твердое тело. Виды движения абсолютно твердого те-
- •4. Динамика материальной точки. Масса. Сила. Импульс (количест-
- •5. Система материальных точек. Силы внешние и внутренние. Им-
- •6. Система материальных точек. Центр масс. Движение центра масс
- •7. Работа. Мощность. Работа постоянной и переменной силы.
- •8. Энергия. Виды механической энергии. Кинетическая энергия.
- •9. Консервативные и неконсервативные силы. Связь между силой и
- •10. Работа и энергия упругих сил и сил тяготения. Потенциальная
- •11. Консервативные и неконсервативные силы. Закон сохранения
- •12. Момент инерции материальной точки. Момент инерции тела. При-
- •13. Момент силы. Момент импульса. Основной закон динамики враща-
- •14. Момент импульса материальной точки. Момент импульса тела.
- •15. Кинетическая энергия вращающегося тела. Работа при враща-
- •16. Сопоставление характеристик и уравнений для поступательного
- •17. Гармонический осциллятор. Дифференциальное уравнение соб-
- •18. Гармонический осциллятор. Кинетическая, потенциальная и
- •19. Физический и математический маятники. Уравнение движения ма-
- •20. Формула Эйлера. Запись гармонических колебаний в комплексной
- •21. Затухающие колебания. Дифференциальное уравнение затухающих
- •22. Вынужденные колебания. Дифференциальное уравнение вынужден-
- •23. Вынужденные колебания. Амплитуда вынужденных колебаний. Ре-
- •24. Общее определение волнового процесса. Уравнение плоской
- •25. Волновой процесс. Упругие волны. Скорость распространения
- •26. Динамика волнового процесса. Перенос энергии волной. Вектор
- •27. Сложение волн. Принцип суперпозиции. Стоячая волна. Узлы и
- •28. Графический метод изображения колебаний. Сложение колебаний
- •29. Сложение взаимно-перпендикулярных колебаний с одинаковыми и
- •30. Понятие идеального газа. Основные газовые законы. Уравнение
- •31. Молекулярно-кинетический и термодинамический подходы в мо-
- •38. Функция распределения молекул по координатам. Функция
- •39. Число столкновений и средняя длина свободного пробега моле-
- •40. Явления переноса в газах. Диффузия. Коэффициент диффузии.
- •41. Первое начало термодинамики. Количество теплоты. Работа и
- •42. Адиабатический процесс. Уравнение Пуассона. Работа газа при
- •43. Первое начало термодинамики и его применение к различным
- •44. Работа, совершаемая газом в различных изопроцессах.
- •45. Графическое изображение термодинамических процессов и рабо-
- •46. Приведенное количество теплоты. Неравенство Клаузиуса.
- •47. Энтропия и ее свойства. Физический смысл. Вычисление изме-
- •48. Второе начало термодинамики. Различные формулировки. Ста-
- •49. Реальные газы. Уравнение состояния реального газа. Внут-
- •50. Понятие о твердых телах. Тепловое движение в кристаллах.
- •51. Инерциальные системы отсчета. Преобразования и принцип от-
- •52. Основные постулаты специальной теории относительности. Ка-
- •53. Преобразования Лоренца-Эйнштейна и их некоторые кинемати-
- •54. Длина отрезка и длительность событий в различных системах
- •55. Релятивистская динамика. Релятивистские масса и импульс.
- •56. Закон взаимосвязи массы и энергии. Кинетическая энергия в
49. Реальные газы. Уравнение состояния реального газа. Внут-
ренняя энергия реального газа. Эффект Джоуля-Томсона.
Уравнение состояния идеального газа PVМ = RТ (для 1 моля газа) хорошо описывает лишь достаточно разреженные газы, где расстояния между соседними молекулами много больше их собственных размеров (радиуса действия межмолекулярных сил). Анализ свойств реальных газов должен учитывать межмолекулярные взаимодействия, которые, согласно Ван-дер-Ваальсу, проявляют себя в: 1/ уменьшении реального, т. е. доступного для движения молекул объёма газа, вследствие действия сил отталкивания между молекулами на малых расстояниях; 2/ увеличении давления, т. к. для молекул характерно превалирование сил притяжения, которые как бы стягивают молекулы газа, порождая некоторое внутреннее давление.
С учётом отмеченных двух поправок к параметрам газа (объёму VМ и давлению Р), связывающее эти параметры уравнение состояния применительно к реальному газу примет для одного моля следующий вид, называемый уравнением Ван-дер-Ваальса:
(Р + а/VМ2)(VM - b) = RT,
где а и b - эмпирические константы, зависящие от рода газа, но не от Р, Т, V; b - поправка к объёму, учитывающая фактически конечность объёма, занимаемого самими молекулами, т. е. действие сил межмолекулярного отталкивания при сближении молекул. Численно она равна учетверённому объёму, занимаемому самими молекулами: b = (23)d3А = 4Vо, где d - эффективный диаметр молекулы (d является табличной характеристикой молекул);
а/VМ2 - поправка к давлению, учитывающая его возрастание, связанное с взаимным притяжением молекул.
Т. к. действие сил межмолекулярного взаимодействия простирается на малые расстояния, то тонкий слой (приповерхностный) газа притягивается к нижележащему с силой (и давлением), пропорциональной квадрату концентрации газа n2 = 2/V2 или обратно пропорциональной квадрату объёма.
Для произвольного количества газа уравнение состояния реального газа примет вид:
(Р + 2a/V2)(V - b) = RT; = mМ; V = VМ.
Проанализируем некоторые особенности этого уравнения 3 - ей степени относительно объёма. Разрешив его относительно объёма, получим:
VМ3 - (RТР + b)VМ2 + аVМР - аbР = 0.
Анализ этого уравнения показывает, что для достаточно высоких температур оно имеет один вещественный корень (два корня – комплексные). При некоторой температуре, называемой критической, все три корня имеют одинаковое вещественное значение, а при более низкой температуре - три различающихся вещественных корня (мнимые значения физического смысла не имеют). Графически эти зависимости Р(VМ) при Т = const - изотермы Ван-дер-Ваальса - имеют следующий вид:
1
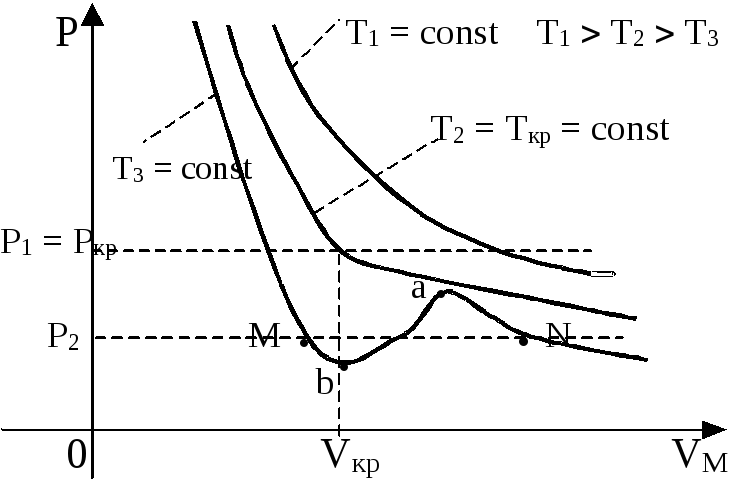
2. При Т < Ткр изотермы перегибаются, и для одного значения давления при фиксированной температуре имеет место три различных значения объёма. Вещество одновременно находится здесь в трех различных фазовых состояниях. Минимальный объём соответствует жидкому состоянию, максимальный - газообразному, среднее же значение объёма соответствует неустойчивому состоянию. В нем с ростом давления объём увеличивается. Таким образом, уравнение Ван-дер-Ваальса даёт изображение фазового перехода между жидким и газообразным состояниями вещества. Уравнение же состояния идеального газа такой возможности не содержало.
3. Т = Ткр. Изобара в точке перегиба касательна к изотерме. Соответствующие этой точке Р = Ркр и V = Vкр, называются критическими.
Внутренняя энергия реального газа. Эффект Джоуля-Томсона.
В
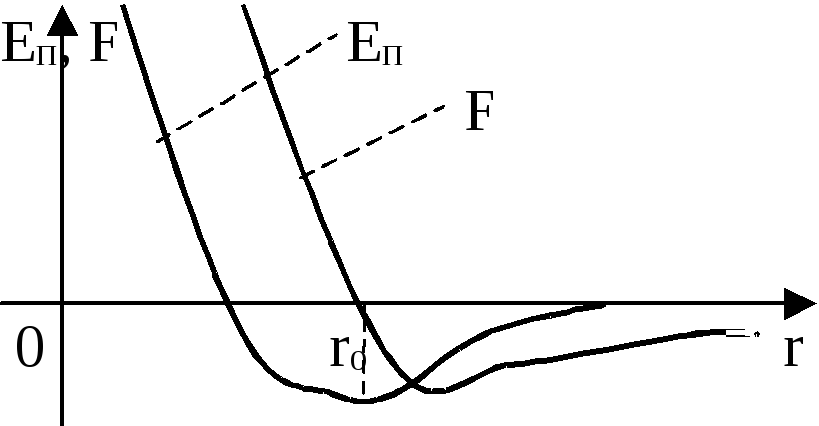
При расширении реального газа, т. е. при увеличении средних расстояний между молекулами, его потенциальная энергия может, как увеличиваться, так и убывать.
Если при этом газ изолирован (адиабатен) и не совершает работы, т. е. Q = 0 и А = 0, то и dU = 0 и в силу сохранения внутренней энергии, изменение её потенциальной компоненты должно сопровождаться компенсирующим изменением кинетической энергии (с обратным знаком). Изменение же кинетической энергии молекул связывается с соответствующим изменением температуры газа:
U (Т, V) = Ек + Еп = (СмV Т –аVм)Р = аVм2; Ам = РdVм = dЕп м = аdVмVм2
Еп м = -аVм и U = Ек + Еп = СмVТ- аVм.
Если газ адиабатно расширяется в пустоту, и его молекулы расходятся на достаточно большие расстояния, где потенциальная энергия их взаимодействия стремится к нулю, т. е. в итоге возрастает /ибо до этого она была отрицательной/, то газ всегда охлаждается. Если же газ адиабатно (медленно) проталкивается через пористую перегородку /для устранения турбулентности/ с перепадом давлений, то в зависимости от соотношения Р1, V1 и Р2, V2 и констант а и b газа, он может и понизить, и повысить, свою температуру. Соответственно имеем положительный и отрицательный эффект Джоуля - Томсона.
В
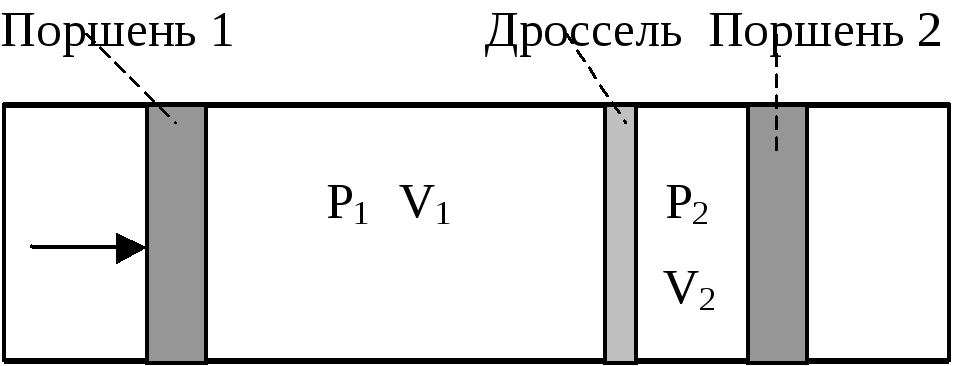
Дроссель (пористая перегородка) поддерживает постоянным перепад давлений Р1 – Р2.
Работа А1, совершаемая по вытеснению газа в объеме V1, равна А1 = Р1V1. После дросселирования газ займет (приобретет) объем V2 и совершит работу А2 = Р2V2. В условиях теплоизоляции изменение (приращение) внутренней энергии газа равно:
U = U2 – U1 = А1 – А2 = Р1V1 – Р2V2 Р1V1 + U1 = Р2V2 + U2 = const.
Для идеального газа Т = 0, эффект Джоуля – Томсона отсутствует.
