Взаимодействия между молекулами
![]()
Силы И.Ван-дер-Ваальса (голланд.ученый, 1873 г.) – силы межмолекулярного взаимодействия (взаимодействия между молекулами), проявляющиеся на расстояниях, превосходящих размеры частиц.
три
составляющие вандерваальсовых сил: (в
зависимости от природы системы)
1. ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ (эффект Кьезома) – электростатическое взаимодействие полярных молекул при сближении (рис.а)
Еориен увеличивается с увеличением мол и уменьшением расстояния между молекулами.
Ч электростатическое
взаимодействие полярной и неполярной
молекул (рис б). Диполи,
действуя на неполярные молекулы,
превращают их в индуцированные
(наведенные) диполи Еинд
увеличивается с увеличением мол
, уменьшением
расстояния между молекулами и увеличением
поляризуемости
неполярной молекулы..

2. Индукционная составляющая (Эффект Дебая) –
Еинд Еориен
дисперсионная составляющая (эффект Лондона)
-электростатическое взаимодействие мгновенных диполей, возникающих за счет флуктуации электрической плотности (рис.с). В результате взаимодействия мгновенных диполей энергия системы понижается.
Едисп пропорциональна поляризуемости молекул и обратно пропорциональна расстоянию между центрами частиц.
Для неполярных молекул - единственная составляющая вандерваальсовых сил.
вещество |
диполя |
Поляризуемость, М31030 |
Энергия взаимодействия, кДж/моль |
Ткип,К
|
|||
ориентационная |
Индукционная |
Дисперсионная |
Суммарная |
||||
H2 Ar Xe HCl HBr HI NH3 |
0 0 0 1,03 0,78 0,38 1,52 |
0,8 1,64 4,16 2,64 3,62 5,42 2,23 |
0 0 0 3,3 1,1 0,6 13,3 |
0 0 0 1,0 0,70 0,3 1,5 |
0,17 8,5 18,4 16,8 28,5 60,6 14,7 |
0,17 8,5 18,4 21,1 30,3 61,5 29,5 |
20,2 76 167 188 206 238 239,6 |
Минимальная энергия системы обеспечивается при расстояниях между центрами молекул 0,4 – 0,5 нм, т. е. существенно больше длины химической связи.
Как видно из табл., с увеличением размера молекул в ряду Аr – Хе и НСl – НI растет их поляризуемость и энергия дисперсионного притяжения. Ориентационное взаимодействие вносит значительный вклад в вандерваальсовы силы для молекул с большим дип. ]
С увеличением Е возрастет Ткип жидкостей, а также теплота их испарения.
![]()
связь, образованная
положительно поляризованным водородом
молекулы А – Н (или полярной группы –
А – Н) и электроотрицательным атомом
В другой или той же молекулы


м е ж м о л е к у л я р н а я внутримолекулярная
■ Межмолекулярная Н-связь
А – Н + В – R А – НВ – R
водород способен глубоко внедряться в электронную оболочку соседнего отрицательно поляризованного атома.
Атомы А и В могут быть одинаковыми
Н+-F- + Н+-F- H-F…H-F
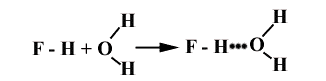 могут
быть разными
могут
быть разными
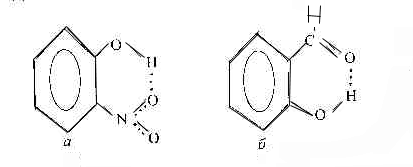
■ Внутримолекулярная Н-связь
о-нитрофенол (а) салициловый альдегид (б)
Е(н-связи) возрастает с увеличением ЭО и уменьшением размеров атомов В:
►
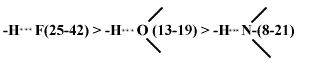 Несмотря
на высокую ЭО, у хлора Н- связь – Н…Сl-
относительно
слабая из-за большого размера атома
хлора.
Несмотря
на высокую ЭО, у хлора Н- связь – Н…Сl-
относительно
слабая из-за большого размера атома
хлора.
► Энергия водородной связи имеет промежуточное значение между энергией ковалентной связи и вандерваальсовых сил.
►У воды длина связи О–Н – 0,096 нм, а связи О…Н – 0,177 нм.
►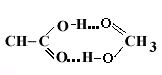 Возникновение
водородных связей приводит к образованию
димеров, тримеров и других полимерных
структур, например, зигзагообразных
структур (НF)n,
кольцевой димерной структуры низших
карбоновых кислот:
Возникновение
водородных связей приводит к образованию
димеров, тримеров и других полимерных
структур, например, зигзагообразных
структур (НF)n,
кольцевой димерной структуры низших
карбоновых кислот:
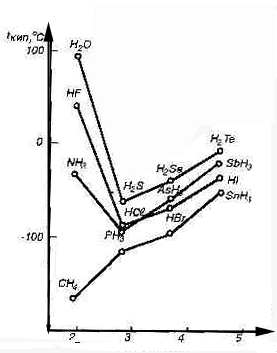
► Межмолекулярные Н-связи изменяют свойства веществ: повышают вязкость, диэлектрическую постоянную, температуру кипения и плавления, теплоту плавления и парообразования.
Н2О, НF и NН3 - аномально высокие Ткип и Тпл.