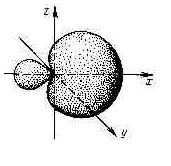
Связь
образована атомами с различным значением
ЭО; связывающая
электронная пара смещена к атому с
большим значением ЭО
Полярная связь
связывающая
электронная пара равномерно распределена
между ядрами взаимодействующих
атомов Связь
образована атомами с одинаковым
значением ЭО (ЭО
= 0): Н2,
О2
и т.д.
Неполярная связь

Молекула НСl:
ЭО(Cl) = 3,0 ЭО(Н) = 2,1
связывающая электронная пара смещена в сторону Cl: эффективный отрицательный заряд (-q) у атома Cl
эффективный положительный заряд (+q) у атома Н
электрический диполь.
д
расстояние
между центрами тяжести эффективных
зарядов (+q
и –q)

электрический момент диполя связи св
(
произведение
эффективного заряда
q
на
длину диполя lд
связи: св
= qlд.
(Клм)
![]()
![]() св
- векторная
величина, направленная от положительного
полюса к отрицательному.
св
- векторная
величина, направленная от положительного
полюса к отрицательному.
св некоторых связей
молекула |
ЭО |
св10-30,Клм |
Вывод |
Н – Сl |
0,90 |
1,03 |
Чем больше ЭО, тем больше св и, следовательно, связь более полярная |
Н – Br |
0,74 |
0,78 |
|
H I |
0,40 |
0,38 |
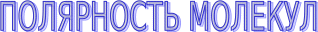
векторная сумма
электрических моментов диполей всех
связей и несвязывающих электронных
пар в молекуле
Электрический момент
диполя молекулы (м)
Полярность молекулы зависит от ее геометрической структуры.
2-х атомные молекулы линейная структура м =св
Если м
= св
= 0
молекула неполярная Если
м
= св
0
молекула полярная
Молекула Н2S
угловая структура ( 920)
ЭО(Н) = 2,1 и ЭО(S) = 2,5 связь полярная.

м = св 0 молекула в целом полярная.
Молекула SbН3
 Sb…5s25p3
Sb…5s25p3
Структура
– тригональная
пирамида Связь
полярная,
т.к.
Э.О.0
м
=
св
0.
молекула в целом полярная

Гибридизация:
смешение
АО с разными (но близкими) энергетическими
состояниями, вследствие которого
возникает такое же число одинаковых
по форме и энергии орбиталей, симметрично
расположенных в пространстве.
Если у атома в образовании химических связей участвуют разные по типу АО (s-, p-, d- или f-АО), то химические связи формируются электронами не «чистых», а «смешанных», или гибридных орбиталей.
Перекрывание гибридных АО происходит в большей степени, чем негибридных орбиталей
► химические связи прочнее
► молекула более устойчива.
Гибридная орбиталь: