
- •Лабораторный практикум по аналитичЕсКой химИи полимеров
- •240501 Химическая технология высокомолекулярных соединений,
- •240100 Химическая технология
- •Лабораторная работа № 1. Общие методы анализов мономеров и полимеров общие методы анализов мономеров и полимеров
- •1.1. Определение плотности
- •1.1.1. Определение плотности жидкости с помощью ареометра
- •1.1.2. Определение плотности с помощью пикнометра
- •1.1.3. Определение насыпной плотности
- •1.2. Определение вязкости
- •1.2.1. Определение абсолютной (динамической) вязкости
- •1.2.2. Определение условной вязкости на вискозиметр типа вз-246
- •1.3. Методы определения влажности
- •1.3.1. Определение содержания влаги высушиванием
- •1.3.2. Йодометрическое определение содержания влаги по Фишеру
- •1.3.3. Определение содержания влаги по Дину и Старку
- •Лабораторная работа № 2. Качественный анализ полимеров Качественный анализ полимеров
- •2.1. Проведение предварительных испытаний
- •2.1.1. Проба на горение
- •2.1.2. Пиролиз
- •2.1.3. Проба с серной кислотой
- •2.1.4. Проба на растворимость
- •2.2. Проведение качественного анализа полимера
- •2.2.1. Восстановительный способ разложения полимеров
- •2.2.2. Обнаружение присутствия азота
- •Лабораторная работа № 3. Анализ фенольно-альдегидных смол Анализ фенольно-альдегидных смол
- •3.1. Количественные определения
- •3.1.1. Определение содержания свободного фенола и формальдегида
- •3.1.1. Определение содержания свободного фенола
- •3.1.2. Определение содержания свободного формальдегида
- •3.2. Качественные определения
- •3.2.1. Определение фенола
- •3.2.2. Определение формальдегида
- •Лабораторная работа № 4. Анализ фенопластов анализ фенопластов
- •4.1. Определение массовой доли гексаметилентетрамина (гмта)
- •4.2. Определение массовой доли смолы и наполнителя
- •Лабораторная работа № 5. Анализ карбамидоформальдегидных смол анализ карбамидоформальдегидных смол
- •5.1. Определение содержания карбамида в составе карбамидоформальдегидных смол
- •5.2. Определение свободного формальдегида
- •5.3. Определение общего содержания формальдегида
- •Библиографический список
- •Лабораторный практикум по аналитичЕсКой химИи полимеров
- •240501 Химическая технология высокомолекулярных соединений,
- •240100 Химическая технология
- •170026, Тверь, наб. Афанасия Никитина, 22
5.2. Определение свободного формальдегида
Метод основан на реакции взаимодействия формальдегида с солянокислым гидроксиламином:
![]()
Выделяющаяся кислота может оказывать влияние на равновесие реакции образования и распада моно- и диметилолкарбамида

Как известно, этот каталитический эффект минимален при рН = 4–9 и увеличивается за пределами этого интервала.
В случае аналитических проб, особенно при малом содержании формальдегида, создаются очень благоприятные условия для диссоциации метилолкарбамидов, что вызывает образование больших количеств свободного формальдегида. В этой связи нейтрализацию выделяющейся соляной кислоты необходимо проводить сразу после добавления раствора солянокислого гидроксиламина.
Реактивы и оборудование:
Гидроксиламин солянокислый, 10%-ный раствор.
Гидроксид натрия ,0,1 н раствора.
Бромфеноловый голубой.
Бюкс для взятия навески.
Колба коническая на 250 мл.
Колба мерная на 100 мл.
Пипетка на 10 и 25 мл.
Цилиндр мерный на 50 мл.
Ход определения. Навеску тонко измельченной смолы (2 г), взятую с точностью до 0,0002 г или 5 мл сиропа смолы (пипеткой), помещают в коническую колбу емкостью 250 мл, приливают 50,0–75,0 мл воды и, если необходимо, спирта до полного растворения смолы и фильтруют в мерную колбу емкостью 100 мл, после чего раствор доводят дистиллированной водой до метки.
К 20 мл полученного раствора, взятого пипеткой, приливают 10 мл (пипеткой) 10%-ного раствора солянокислого гидроксиламина, несколько капель индикатора (бромфенолового голубого) и титруют 0,1 н раствором гидроксида натрия. Точку нейтрализации можно определить путем потенциометрического титрования с помощью рН-метра до величины рН = 4,01.
Параллельно проводят холостой опыт, используя 20 мл дистиллированной воды.
Расчет. Содержание формальдегида X рассчитывают по формуле
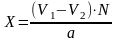 ,
%,
,
%,
где V1 – объем щелочи в контрольном опыте, мл; V2 – объем щелочи в холостом опыте, мл; N – нормальность щелочи; а – навеска, г.
5.3. Определение общего содержания формальдегида
Метод основан на разложении аминосмолы при кипячении с концентрированной фосфорной кислотой с последующим окислением выделяющегося формальдегида перекисью водорода в щелочной среде [20].
Реактивы и оборудование:
о-Фосфорная кислота, 85%-ная.
Гидроксид натрия, 0,5 н раствор.
Соляная кислота. 0,1 н раствор.
Перекись водорода, 3%-ный раствор.
Индикатор метиловый красный.
Круглодонная колба для перегонки емкостью 250 мл.
Коническая колба емкостью 500 мл.
Капельная воронка вместимостью 100 мл.
Холодильник прямой.
Холодильник обратный.
Пипетка на 50 и 25 мл.
Мерная колба на 250 мл.
Термометр ТЛ (0 +150).
Ход определения. Собирают перегонную установку (рис. 7), снабженную капельной воронкой, устанавливая аллонж таким образом, чтобы его конец был опущен ниже уровня раствора приемника. В коническую приемную колбу емкостью 500 мл наливают пипеткой 50 мл 0,5 н раствора едкого натра и 60 мл (мерный цилиндр) 3%-ного раствора перекиси водорода. Отвешивают 1 г смолы с точностью до 0,01 г и переносят в колбу Вюрца емкостью 250 мл, помещают в нее «кипелки» (кусочки пемзы или неглазурованного фарфора). Через капельную воронку добавляют 25 мл 85%-ной фосфорной кислоты и 25 мл воды. Содержимое колбы нагревают до точки кипения (110С). Отгоняют 200 мл жидкости, поддерживая в перегонной колбе постоянный объем путем добавления воды из капельной воронки.
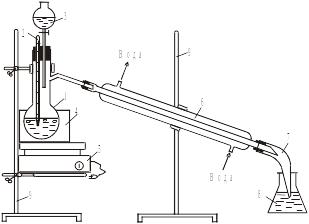
Рис. 7. Установка для перегонки:
1 – колба Вюрца, 2 – термометр, 3 – капельная воронка, 4 – баня воздушная, 5 – плитка электрическая, 6 – холодильник, 7– аллонж, 8 – приемник, 9 – штативы
По окончании перегонки холодильник и аллонж тщательно промывают водой (25 мл). Затем к приемной колбе присоединяют вертикальный холодильник и нагревают на водяной бане в течение 0,5 часа для расщепления ацеталей и полного окисления формальдегида. Раствор охлаждают и переносят в мерную колбу на 250 мл, доводят объем до метки дистиллированной водой. Избыток щелочи оттитровывают стандартным 0,1 н раствором соляной кислоты по метиловому красному, взяв аликвотную часть пипеткой на 25 мл. Одновременно проводят холостой опыт, титруя таким же способом 25 мл раствора, полученного в мерной колбе на 250 мл разбавлением дистиллированной водой до метки 50 мл 0,5 н раствора гидроксида натрия и 60 мл 3%-ного раствора перекиси водорода.
Расчет. Содержание формальдегида определяют по формуле
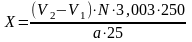 ,
%,
,
%,
где V2 – объем раствора HCl, израсходованного на титрование в холостом опыте, мл; V1 – объем раствора HCl , израсходованного на титрование образца, мл; N – нормальность раствора HCl; а – навеска, г.
