
- •Лабораторный практикум по аналитичЕсКой химИи полимеров
- •240501 Химическая технология высокомолекулярных соединений,
- •240100 Химическая технология
- •Лабораторная работа № 1. Общие методы анализов мономеров и полимеров общие методы анализов мономеров и полимеров
- •1.1. Определение плотности
- •1.1.1. Определение плотности жидкости с помощью ареометра
- •1.1.2. Определение плотности с помощью пикнометра
- •1.1.3. Определение насыпной плотности
- •1.2. Определение вязкости
- •1.2.1. Определение абсолютной (динамической) вязкости
- •1.2.2. Определение условной вязкости на вискозиметр типа вз-246
- •1.3. Методы определения влажности
- •1.3.1. Определение содержания влаги высушиванием
- •1.3.2. Йодометрическое определение содержания влаги по Фишеру
- •1.3.3. Определение содержания влаги по Дину и Старку
- •Лабораторная работа № 2. Качественный анализ полимеров Качественный анализ полимеров
- •2.1. Проведение предварительных испытаний
- •2.1.1. Проба на горение
- •2.1.2. Пиролиз
- •2.1.3. Проба с серной кислотой
- •2.1.4. Проба на растворимость
- •2.2. Проведение качественного анализа полимера
- •2.2.1. Восстановительный способ разложения полимеров
- •2.2.2. Обнаружение присутствия азота
- •Лабораторная работа № 3. Анализ фенольно-альдегидных смол Анализ фенольно-альдегидных смол
- •3.1. Количественные определения
- •3.1.1. Определение содержания свободного фенола и формальдегида
- •3.1.1. Определение содержания свободного фенола
- •3.1.2. Определение содержания свободного формальдегида
- •3.2. Качественные определения
- •3.2.1. Определение фенола
- •3.2.2. Определение формальдегида
- •Лабораторная работа № 4. Анализ фенопластов анализ фенопластов
- •4.1. Определение массовой доли гексаметилентетрамина (гмта)
- •4.2. Определение массовой доли смолы и наполнителя
- •Лабораторная работа № 5. Анализ карбамидоформальдегидных смол анализ карбамидоформальдегидных смол
- •5.1. Определение содержания карбамида в составе карбамидоформальдегидных смол
- •5.2. Определение свободного формальдегида
- •5.3. Определение общего содержания формальдегида
- •Библиографический список
- •Лабораторный практикум по аналитичЕсКой химИи полимеров
- •240501 Химическая технология высокомолекулярных соединений,
- •240100 Химическая технология
- •170026, Тверь, наб. Афанасия Никитина, 22
1.3. Методы определения влажности
Определение влаги производится на всех стадиях производства – при анализе сырья, вспомогательных материалов и готовой продукции.
Влага может быть частью анализируемого вещества, входящей в его состав в определенных постоянных соотношениях (кристаллизационная вода), а также присутствовать в виде примеси (гигроскопическая вода). Чтобы провести правильные расчеты результатов определения основного компонента анализируемого продукта, необходимо точно знать содержание влаги в этом продукте.
1.3.1. Определение содержания влаги высушиванием
Кристаллизационную и гигроскопическую влагу определяют обычно методом высушивания. Гигроскопическую влагу удаляют в сушильном шкафу при 100–105С, кристаллизационную – при 120–130С, а иногда и выше. Высушивание можно проводить также путем нагревания навески вещества лампой инфракрасного излучения.
Однако при высушивании масса вещества может уменьшаться не только за счет испарения влаги, но и вследствие удаления летучих составных частей вещества и продуктов его разложения или окисления. В этих случаях гигроскопическую влагу определяют путем высушивания в вакуум-эксикаторах над водопоглощающими веществами (серная кислота, фосфорный ангидрид, прокаленный хлорид кальция и др.) [8].
Ход определения. В предварительно вымытый и высушенный до постоянной массы бюкс помещают навеску вещества, закрывают крышкой и взвешивают на аналитических весах. Величину взятой навески определяют по разности массы бюкса с навеской и пустого бюкса. Приоткрыв крышку бюкса, помещают его в сушильный шкаф и сушат до постоянной массы. Если два последующих взвешивания после высушивания в течение 30 минут дают разницу, не превышающую 0,0002 г, то масса вещества считается постоянной. Вынимают бюкс из сушильного шкафа и помещают в эксикатор на 30 мин для того, чтобы он принял комнатную температуру, затем снова взвешивают. Продолжительность процесса определения влаги 2–3 часа.
Расчет. Содержание влаги Х вычисляют по формуле

где а1 – масса бюкса и исследуемого вещества, г; а2 – масса бюкса и сухого вещества, г; а3 – масса испытуемого вещества, г.
1.3.2. Йодометрическое определение содержания влаги по Фишеру
Сущность метода заключается во взаимодействии воды, содержащейся в пластмассе, с реактивом Фишера после ее растворения или экстракции воды растворителями.
Определение содержания воды полимеризационных и поликонденсационных пластмасс в виде гранул, бисера, порошка, латекса, дисперсии (за исключением полиамидных и карбамидных смол) проводят согласно ГОСТ 11736-78 [14].
Этот метод позволяет достаточно быстро и точно определять содержание свободной воды как в органических, так и неорганических соединениях. Относительная погрешность метода 5%. Диапазон определяемого содержания воды 0,005–80%. В основе определения лежит реакция окисления двуокиси серы йодом в присутствии воды:
I2 + SO2 + 2 H2O H2SO4 + 2 HI
Д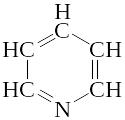 ля
связывания выделяющихся кислот реакцию
проводят в присутствии пиридина
ля
связывания выделяющихся кислот реакцию
проводят в присутствии пиридина
.
Реактив Фишера представляет собой раствор двуокиси серы, йода и пиридина в метаноле. Определение содержания влаги при помощи реактива Фишера сводится к титрованию точной навески испытуемого вещества. Конец титрования определяют визуально по изменению окраски раствора от желтой до красно-коричневой или электрохимически, проводя потенциометрическое титрование.
Реакция протекает в две стадии:
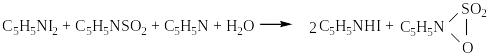
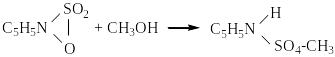
Суммарное уравнение реакции
С5H5NI2 + C5H5NSO2 + C5H5N + CH3OH + H2O 2 C5H5NHI + C5H5NHSO4CH3
Метод Фишера применим также для определения содержания влаги в газах. Для этого нужное количество газа пропускают через точный объем метанола, хорошо поглощающего влагу, а затем раствор титруют реактивом Фишера и определяют содержание влаги.
Для приготовления реактива Фишера в сухую колбу емкостью 1 л помещают 125 г йода и растворяют в 200 мл пиридина. Затем приливают 30 мл метанола, колбу закрывают пробкой и осторожно взбалтывают. Поместив колбу в ледяную воду, пропускают через раствор обезвоженную двуокись серы до тех пор, пока масса не увеличится на 65 г. Объем раствора доводят до 1 л метанолом, хорошо перемешивают и выдерживают сутки. Раствор хранят в темном месте в герметически закупоренной склянке. Рекомендуется пробку склянки залить парафином.
Для установки титра приготовленного раствора к точной навеске воды (приблизительно 0,03–0,05 г), взвешенной на аналитических весах в сухой колбе емкостью 50 мл, прибавляют 5 мл метанола и титруют реактивом Фишера, внося его в конце титрования по 0,1–0,05 мл. Одновременно проводят холостое титрование такого же объема растворителя.
Титр Т показывает количество граммов воды, эквивалентное 1 мл приготовленного реактива Фишера:

где g – навеска воды, г; V – объем реактива, израсходованный на титрование навески в метаноле, мл; V1 – объем реактива, израсходованный на титрование метанола, мл.
Ход определения. Для титрования применяют прибор для титрования реактивом Фишера. Навеску испытуемого вещества 1–5 г (в зависимости от предполагаемого содержания воды), взятую с точностью до 0,0002 г, помещают в колбу емкостью 100 мл, добавляют 30 мл сухого метанола, взбалтывают в течение 1–2 минут для извлечения воды, доводят объем метанолом до 100 мл, плотно закрывают пробкой и перемешивают. Отбирают пипеткой 10 мл раствора в колбу для титрования и титруют реактивом Фишера до появления красно-коричневого окрашивания. Параллельно титруют 10 мл метанола (холостой опыт).
Расчет. Содержание воды х вычисляют по формуле

где V1 – объем реактива Фишера, израсходованный на титрование пробы, мл; V2 – объем реактива Фишера, израсходованный на титрование холостой пробы, мл; Т – титр реактива Фишера; g – навеска вещества, г;
