
- •Курс лекций
- •По физико-химическим методам анализа
- •Раздел: «электрохимия»
- •Содержание
- •Тема I: «кондуктометрический метод анализа» лекция 17 план:
- •I. Титрование по методу осаждения.
- •II. Титрование по методу нейтрализации.
- •Лекция 18 план:
- •Тема II: «потенциометрический метод анализа» лекция 19 план:
- •Лекция 20 план:
- •Лекция 21 план:
- •Тема III: «электрогравиметрический и кулонометрический методы анализа» лекция 22 план:
- •Химические процессы при электролизе:
- •Лекция 23 план:
- •Лекция 24 план:
- •Тема IV: «полярографический метод анализа» лекция 25 план:
- •Лекция 26 план:
- •Лекция 27 план:
- •1) Расчетный метод
- •2) Метод градуировочного графика
- •3) Метод стандартных растворов
- •4) Метод добавок
- •1 ) Восходящая кривая:
- •2 ) Нисходящая кривая:
- •3) Комбинированная кривая:
Лекция 20 план:
Индикаторные электроды метода осаждения и комплексообразования.
Индикаторные электроды метода окисления - восстановления.
Ионоселективные электроды. Типы ионоселективных электродов.
Ионометрия. Реальный окислительно-восстановительный потенциал. Определение произведения растворимости плохо растворимых соединений.
1.
Для реакции осаждения и комплексообразования применяются металлические электроды, металлические электроды, покрытые их малорастворимой солью.
Металлические электроды: Нg│Нg2+ - ртутный, Аg│Аg+ - серебряный, Рt - платиновый. Ртутный и серебряный электроды обратимы относительно ионов ртути и серебра. При работе с платиновым электродом в раствор вводят ионы, какого - либо металла в двух различных степенях окисления. Рабочий раствор подбирают так, чтобы он реагировал с одним из ионов окислительно-восстановительной системы, но чтобы это взаимодействие происходили только после завершения основной реакции между определяемым веществом и раствором реагента.
Металлические электроды, покрытые пленкой малорастворимой соли того же металла:
Аg│AgCl│Cl- , Hg│Hg2Cl2│Cl-. Потенциалы этих электродов чувствительны к изменению концентрации Сl- ионов:
![]() ,
,
![]() .
.
Недостатки электродов:
Металлы на воздухе покрываются пассивирующей пленкой и не реагируют на изменение концентрации своих ионов.
Металлические электроды нельзя применять, если в растворе имеются ионы металла, расположенного в ряду напряжений за металлом индикаторного электрода.
2.
При окислительно-восстановительном титровании индикаторными электродами служат индифферентные металлы - платина, палладий, золото. Наиболее часто применяется гладкий платиновый электрод.
3.
Ионоселективные электроды - это электроды, чувствительные по отношению к одним ионам в растворе и не чувствительные к другим.
Все ионоселективные электроды можно разделить на четыре типа:
Ионоселективные электроды со стеклянной мембраной
Ионоселективные электроды с жидкой органической мембраной.
С твердой мембраной
С фермент - субстратной (гетерогенной) мембраной.
Применение ионоселективных электродов очень перспективно, определение концентраций веществ проводится за секунды, т.е. возможен автоматический контроль.
СТЕКЛЯННЫЕ ИОНОСЕЛЕКТИВНЫЕ ЭЛЕКТРОДЫ:
Изменяя
состав стекла можно получить электроды,
селективные по отношению к различным
ионам. Так, стекло с повышенным содержанием
Аl2О3
позволяет замерить ![]() .
Стекла различного состава имеют сродство
к
определенным катионам.
.
Стекла различного состава имеют сродство
к
определенным катионам.
Э
Ag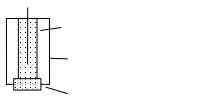 ЛЕКТРОДЫ
С ЖИДКОСТНЫМИ МЕМБРАНАМИ:
ЛЕКТРОДЫ
С ЖИДКОСТНЫМИ МЕМБРАНАМИ:
Э
AgCl
+ стандартный
раствор определяемого металла
органический
ионообменник
пористая
гидрофобная мембрана
На
границе раздела
мембраны с растворами возникает
потенциал, но т.к. состав внутреннего
водного раствора постоянен, потенциал
мембран меняется лишь с изменением
состава исследуемого раствора, влияющего
на потенциал внешней границы раздела:
![]() .
.
Такие электроды изготовлены для определения Сa2+; Cl-; NO3-; K+ и ряда других ионов.
Э
стандартный
раствор
эпоксидное
покрытие
твердый контакт
чувствительный
элемент
 ЛЕКТРОДЫ
С ТВЕРДЫМИ МЕМБРАНАМИ:
ЛЕКТРОДЫ
С ТВЕРДЫМИ МЕМБРАНАМИ:
Мембраной служит твердое вещество, обладающее свойствами проводника - монокристалл или таблетка, спрессованная из кристаллического материала. Возникновение электрического тока в кристаллической мембране обязано тем ионам кристаллической решетки, которые характеризуются наименьшим ионным радиолучом и наименьшим зарядом. Движение этих ионов обусловлено наличием дефектов решетки; ближайший к вакантному месту ион перемещается к этому месту. Требования к размеру, форме и заряду вакантных мест таковы, что подвижный ион кристаллической решетки является единственным ионом, который может перейти на это место (F-; Ag+).
ЭЛЕКТРОДЫ С ГЕТЕРОГЕННЫМИ МЕМБРАНАМИ:
В ионоселективных электродах этого типа твердое соединение, обладающее ионообменными свойствами, закрепляется в полимерной матрице мембраны.
Электрод для определения мочевины на основе уреазы:
Акриламидный гель, в котором фиксируется уреаза, наносится на поверхность стеклянной мембраны, чувствительной к ионам NH4+. Мочевина диффундирует в слой геля и под действием уреазы подвергается гидролизу:
![]()
Стеклянная мембрана реагирует на образующиеся ионы NH4+.
4.
Ионометрия или прямая потенциометрия основана на измерении потенциала электрода и расчете концентрации иона, по уравнению Нернста.
Для точных расчетов необходимо учитывать, что на электродный потенциал влияют различные факторы и поэтому электродный потенциал может отличаться от табличного.
Потенциал, замеренный в реальных условиях, называется реальным потенциалом.
На величину потенциала влияют:
1.
Посторонние комплексообразующие
ионы
Fe3+
/ Fe2+,
![]() В;
Fe(CN)63-
/ Fe(CN)64-,
В;
Fe(CN)63-
/ Fe(CN)64-,
![]() В.
В.
2. Ионная сила раствора, т.е. наличие всех примесей (индеферентных солей)
![]()
3.
Ионы
Н+,
принимающие участие в реакции
MnO4-
+ 5![]() + 8H+
→ Mn2+
+ 4H2O;
+ 8H+
→ Mn2+
+ 4H2O;
![]()
![]()
4. Ионы Н+, не принимающие участие в реакции Fe3+ + HOH → Fe(OH)2+ + H+; Fe2+ + HOH → FeOH+ + H+
Чаще всего величина реального электродного потенциала может быть определена только экспериментально.
ОПРЕДЕЛЕНИЕ
![]() :
:
I. Берем стандартный раствор ВаSO4.
![]()
![]()
![]()
II. Берем насыщенный раствор ВаSO4.
![]()
![]()
![]()
