
- •Курс лекций
- •По физико-химическим методам анализа
- •Раздел: «электрохимия»
- •Содержание
- •Тема I: «кондуктометрический метод анализа» лекция 17 план:
- •I. Титрование по методу осаждения.
- •II. Титрование по методу нейтрализации.
- •Лекция 18 план:
- •Тема II: «потенциометрический метод анализа» лекция 19 план:
- •Лекция 20 план:
- •Лекция 21 план:
- •Тема III: «электрогравиметрический и кулонометрический методы анализа» лекция 22 план:
- •Химические процессы при электролизе:
- •Лекция 23 план:
- •Лекция 24 план:
- •Тема IV: «полярографический метод анализа» лекция 25 план:
- •Лекция 26 план:
- •Лекция 27 план:
- •1) Расчетный метод
- •2) Метод градуировочного графика
- •3) Метод стандартных растворов
- •4) Метод добавок
- •1 ) Восходящая кривая:
- •2 ) Нисходящая кривая:
- •3) Комбинированная кривая:
Тема II: «потенциометрический метод анализа» лекция 19 план:
Сущность метода и область применения. Классификация: ионометрия (прямая потенциометрия), потенциометрическое титрование.
Электроды. Электроды первого и второго рода.
Электроды сравнения. Требования, предъявляемые к электродам сравнения. Водородный нуль - электрод, каломельный, хлорсеребряный электроды.
Индикаторные электроды. Электроды, применяемые в кислотно-основном методе. Устройство водородного, хингидронного, стеклянного электродов. Преимущества и недостатки этих электродов.
Определение рН растворов с помощью цепей, состоящих из двух водородных электродов, хингидронного и каломельного электродов, стеклянного и каломельного электродов.
1.
Потенциометрический метод анализа основан на изменении величины потенциала электрода в зависимости от физических или физико-химических процессов, протекающих в системе.
При
погружении металлической пластины в
раствор на границе металл - раствор
возникает электродный потенциал.
![]()
П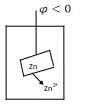 ри
t
= 25
ри
t
= 25
Величина и знак заряда зависят от энергии решетки металла при данной концентрации ионов в растворе.
Если энергия гидратации велика, происходит образование катионов, металл заряжается отрицательно за счет избытка электронов. Электростатическое поле притягивает к себе катионы из раствора. Возникает двойной электрический слой. Нейтрализации ионов не происходит, т.к. ионы удерживаются молекулами воды. Внутри двойного электрического слоя создается некоторая разность потенциалов.
Величина и знак потенциала зависят от:
природы металла
растворителя
концентрации ионов в растворе
и выражается уравнением Нернста:
![]()
Д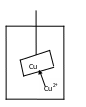 ля
разбавленных растворов при t
= 25°С
:
ля
разбавленных растворов при t
= 25°С
:
![]()
Энергия
гидратации мала, медь оседает на
пластинке, потенциал ![]() >0.
>0.
Металлические пластинки бывают двух типов:
1) Металл - проводник, находящийся в контакте с раствором своих ионов.
![]()
![]()
2) Инертный металл (Рt), находящийся в контакте с раствором ионов, составляющих окислительно-восстановительную пару.
Например: платиновая проволока, опущенная в раствор с Fе2+ и Fе 3+.
При этом на электроде протекает полуреакция восстановления: Fe3+ + e = Fe2+
и полуреакция окисления: Fe2+ - e = Fe3+.
Мерой окислительно-восстановительной способности служит электродный редокспотенциал:
![]()
![]()
![]() -
стандартный электродный потенциал
– это потенциал, замеренный относительно
водородного электрода при t=25
и концентрации определяемого иона = 1
моль/дм3.
-
стандартный электродный потенциал
– это потенциал, замеренный относительно
водородного электрода при t=25
и концентрации определяемого иона = 1
моль/дм3.
Измерить потенциал одного электрода нельзя, но можно измерить ЭДС гальванического элемента, составленного из двух электродов, потенциал одного из которых есть величина постоянная, а потенциал второго меняется с изменением концентрации определяемого иона в растворе (такой электрод выступает в роли индикатора).
Если
![]() ,
то
,
то ![]() будет
зависеть только
от потенциала анода, который является
индикатором.
будет
зависеть только
от потенциала анода, который является
индикатором.
Электрод, потенциал которого изменяется с изменением концентрации определяемого иона, называется индикаторным электродом.
Электрод, потенциал которого остается постоянным, называется стандартным электродом или электродом сравнения.
Потенциометрический метод анализа применяется:
для нахождения точки эквивалентности в титриметрии
для определения концентрации ионов в растворе
для изучения химических реакций
Потенциометрический метод анализа делится на прямую потенциометрию и потенциометрическое титрование.
Прямая потенциометрия - определяет значение электродного потенциала, и вычисляют по уравнению Нернста концентрацию определяемого иона.
Потенциометрическое титрование - конец реакции определяют по резкому изменению электродного потенциала в эквивалентной точке индикатор - электрод.
2.
Все электроды можно разделить на электроды I и II рода.
Электроды I рода – это, электроды, обратимые относительно катионов, т.е. чувствительны к тем катионам, с которыми они могут образовывать окислительно-восстановительную систему.
Например: Аg(электрод) │ АgNO3 (раствор)
Аg + е = Аg(тв)
Такой электрод чувствителен только к катионам серебра.
К электродам первого рода можно отнести и водородный электрод. Газообразный водород, адсорбированный на металле, образует с ионами водорода в растворе окислительно-восстановительную систему: 2Н++2е = Н2 .
Электроды, чувствительные к анионам, которые образуют малорастворимые осадки с катионами металла электрода, относятся к электродам второго рода. Электроды второго рода чувствительны также к изменению концентрации ионов, которые не участвуют непосредственно в окислительно -восстановительном процессе.
Например: Аg│АgСl (насыщенный раствор)
АgСl(тв) + е = Аg(тв) + Сl-
Потенциал электрода зависит от концентрации Сl-, т.к. раствор АgСl насыщенный ПР=[Аg+][Сl-], отсюда [Аg+]=ПР/[Сl-].
![]()
Можно определить как концентрацию Сl- и Аg+ - ионов.
К электродам второго рода относятся хлорсеребряный и каломельный электроды.
3.
Электроды сравнения могут быть электроды второго рода при условии сохранения условия постоянной концентрации ионов, определяющих электродный процесс.
Например: Hg│Нg2Сl2│КСl - каломельный;
Нg│Нg2SO4│Н2SO4 - сульфатнортутный;
Аg│АgСl│КСl - хлорсеребряный.
Требования к электродам сравнения:
п
 отенциал
должен быть постоянен во времени и по
температуре
отенциал
должен быть постоянен во времени и по
температуреп
Ag
рост в изготовлении
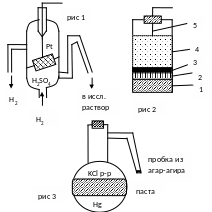
ВОДОРОДНЫЙ ЭЛЕКТРОД (рис 1)
Платину покрывают чернью для лучшей воспроизводимости опытов и для уменьшения влияния загрязнений.
![]()
![]()
Водород
должен быть абсолютно чистым (обычно
получают электролитическим путем).
Потенциал такого электрода условно
принят
равным нулю. ![]()
ХЛОРСЕРЕБРЯННЫЙ ЭЛЕКТРОД (РИС 2)
Серебряный электрод, погруженный в раствор хлорида калия, насыщенный хлоридом серебра.
пористая пробка (через пробку идет контакт с исследуемым раствором)
пробка из агар - агара
твердый КСl
раствор насыщенный КСl + 1 капля 1М АgNO3
серебряная проволочка
Иногда электрод изготавливают проще: серебряную проволоку окунают в расплав АgСl, который хорошо проводит электрический ток, а затем погружают в раствор КСl.
Аg│АgСl│КС1 (АgСlтв + е = Аg++Сl-)
Постоянство электродного потенциала поддерживается избытком хлорида калия, а именно избытком Сl-, который входит в состав АgСl, малорастворимой соли.
Преимущества: прост и удобен в работе.
КАЛОМЕЛЬНЫЙ ЭЛЕКТРОД (РИС З)
Нg│Нg2Сl2│КСl Нg2Cl2 + 2е = 2Нg+ + 2Сl-
Потенциал каломельного электрода зависит от концентрации хлорид ионов, она должна быть фиксированной для каждого электрода.
Электроды различают по концентрации КСl: насыщенные, 1Н; 0,1Н.
Недостаток: имеет высокое сопротивление, легко поляризуется.
4.
Индикаторный электрод - это электрод, изменяющий свой потенциал с изменением концентрации определяемого иона.
Индикаторный электрод выбирают в зависимости от типа реакции.
Требования к индикаторному электроду:
обратимость электрода
потенциал устанавливается мгновенно
не должен реагировать на примеси
Метод нейтрализации: в основе метода лежит реакция
H+ + ОН-=Н2O. Индикаторный электрод должен реагировать на изменение концентрации ионов водорода.
ХИНГИНДРОННЫЙ ЭЛЕКТРОД
Хингиндрон С6Н402 *C6H4(OH)2 - эквимолекулярное соединение хинона и гидрохинона. В водном растворе существует равновесие:
C6H4O2 + 2H+ + 2e = C6H4(OH)2.
В исследуемый раствор насыпают хингидрон и отпускают туда платиновую пластинку; создается окислительно-восстановительная система:
![]()
![]()
![]()
В присутствии сильных окислителей (соли железа, титана, HNO3 и других) хингидронный электрод применять нельзя.
Применяется электрод для измерения рН = 0-8.
ВОДОРОДНЫЙ ЭЛЕКТРОД Если в водородный электрод залить исследуемый раствор с неизвестным рН, то этот электрод будет работать как индикаторный; рН = 1-13,электрод сильно реагирует на примеси.
СТЕКЛЯННЫЙ ЭЛЕКТРОД
Н аиболее
часто применяющийся электрод. Это
стеклянный шарик диаметром до 15-20
мм и толщиной стенок 0,05-0,1 мм изготовленный
из рН -чувствительного
стекла. В трубку с шариком залит раствор
НСl,
насыщенный АgСl
и помещена серебряная проволока. Раствор
имеет постоянную
концентрацию ионов водорода. При
погружении шарика в раствор
между внутренней и внешней поверхностями
стеклянной мембраны возникает
разность потенциалов
аиболее
часто применяющийся электрод. Это
стеклянный шарик диаметром до 15-20
мм и толщиной стенок 0,05-0,1 мм изготовленный
из рН -чувствительного
стекла. В трубку с шариком залит раствор
НСl,
насыщенный АgСl
и помещена серебряная проволока. Раствор
имеет постоянную
концентрацию ионов водорода. При
погружении шарика в раствор
между внутренней и внешней поверхностями
стеклянной мембраны возникает
разность потенциалов ![]() и
и ![]() связано с ионообменным взаимодействием
ионов водорода и щелочных металлов,
находящихся в стекле.
связано с ионообменным взаимодействием
ионов водорода и щелочных металлов,
находящихся в стекле.
R-SiONa + H+ = R-SiOH + Na+
стекло р-р стекло р-р
Ионный обмен происходит только при участии гидритированной мембраны. Сухой стеклянный электрод теряет свою активность. Во внутреннем слое в результате ионного обмена устанавливается потенциал , величина которого постоянна, т.к. концентрация Н+ постоянна. Во внешнем слое устанавливается потенциал , величина которого меняется с изменением концентрации исследуемого раствора. Работает стеклянный электрод обычно в паре с каломельным электродом. Гальваническую пару можно записать следующим образом:
И.К.Э. |
Внешний анализируемый раствор |
Стеклянная мембрана (шарик) |
Внутренний раствор |
Стеклянный электрод Ag│AgCl |
![]()
![]()
Потенциалы и не зависят от изменения рН анализируемого раствора.
Изменение
рН определяется только разностью ![]() , а так как
, а так как ![]() ,
то изменение рН определяется изменением
,
то есть чувствительностью внешней
мембраны.
,
то изменение рН определяется изменением
,
то есть чувствительностью внешней
мембраны.
В
схеме два электрода сравнения – внешний
и внутренний – это обеспечивает
возможность замера ![]() .
.
Недостатки:
Высокое омическое сопротивление
Потенциал асимметрии. Если концентрация ионов водорода одинакова внутри и снаружи, то на внутренней и внешней поверхностях электрода возникают разные потенциалы, что является результатом строения и природы стеклянной мембраны.
Уменьшают этот потенциал путем подбора стекла (тонкое и легкоплавкое) и периодическим вымачиванием его в буферном растворе с рН внутреннего раствора.
Преимущества:
На него не действуют окислители и восстановители
Область применения рН=0-14, то есть кислые и щелочные среды
5.
Определение рН растворов с помощью индикаторных электродов: 1) Два водородных электрода (-) Рt(Н2) │2Н+ ∫исследуемый раствор∫ 2Н+│(Н2)Рt (+) индикаторный стандартный
![]()
![]()
Р = 1атм. t = 25
![]()
![]()
![]()
![]()
![]()
2)
Каломельный
электрод - хингидронный электрод
(-) Нg│Нg2Cl2│КС1
∫ исследуемый раствор ∫ ХГ (+)
![]()
![]()
![]()
![]()
3) Стеклянный электрод - каломельный электрод
(-) стандартный ∫станд. р-р или ∫ КСl│каломельный (+)
электрод иссл. р-р насыщ. электрод
Прибор градуируется в единицах рН.
