
- •51. Статистический и термодинамический методы исследования вещества.
- •52. Основные положения молскулярно-кинетичсской теории.
- •53. Максвелловский закон распределения молекул газа по их скоростям.
- •54. Больцмановский закон распосделсния молекул газа по их энергиям.
- •55. Закон равномерного распределения энергии по степеням свободы молекул газа.
- •56. Молекулярно-кинстическое толкование абсолютной температуры
- •57. Первое начало термодинамики.
- •58. Адиабатический процесс.
- •59. Политропические процессы
- •60. Второе начало термодинамики.
- •61. Изопроцессы. Запишите уравнения состояния идеального газа для этих процессов и начертите их графики в координатах р и V, р и t, t и V.
- •62. Дайте определение полной, молярной и удельной тсплоемкостей газа.
- •63Дайте определение равновесного и неравновесного состояния системы.
- •64. Дайте определение обратимого и необратимого процесса.
- •65. Дайте определение кругового процесса (цикла). Объясните принцип действия тепловых машин.
- •66. Начертите цикл Карно в координатах р и V
- •67. Дайте определение энтропии. Чему равно изменение энтропии для обратимых и необратимых процессов.
- •Энтропия и второе начало термодинамики
- •73. Приведите барометрическую формулу. Для чего она служит?
- •74. Получите формулу для средней длины свободного пробега молекул газа.
- •75. Какое явление переноса в идеальном газе описывается выражением
- •78. Получите выражения для молярных теплоемкостей всех изопроцессов в идеальном газе. 79Получите соотношение Манера
- •Соотношение Майера
- •Соотношение Майера
- •94. Начертите изотерму Ван-дер-Ваальса и сравните ее с экспериментальной изотермой реального газа.
- •95. Дайте определение критического состояния газа. Получите выражения для параметров критического состояния газа.
- •96. Получите формулу для внутренней энергия реального газа.
- •97. В чем заключается эффект Джоуля-Томсона?
- •98. Получите уравнение Клапейрона-Клаузиуса для фазового превращения реального газа.
- •99. Нарисуйте диаграмму равновесных давлений и температур для двухфазной системы "жидкость - пар".
- •100Нарисуйте обобщенную диаграмму состояний для трехфазной системы "твердое тело - жидкость - газ". Дайте определение тройной точки.
- •Фазовые превращения реального газа
- •Уравнение Клапейрона-Клаузиуса и фазовая диаграмма для превращения жг
- •Уравнение Клайперона-Клаузиуса и Рис. 6 фазовая диаграмма для превращения тж
- •Уравнение Клайперона-Клаузиуса и фазовая диаграмма для превращения тг. Тройная точка. Диаграмма состояния.
73. Приведите барометрическую формулу. Для чего она служит?
74. Получите формулу для средней длины свободного пробега молекул газа.
Средняя длина свободного пробега молекул газа

На рисунке показана кривая, изображающая взаимную потенциальную энергию двух молекул как функцию расстояния r между их центрами. Рассмотрим с помощью этой кривой процесс сближения (соударения) молекул. Поместим мысленно центр одной из молекул в начало координат, а центр второй молекулы представим перемещающимся по оси r. Пусть вторая молекула летит по направлению к первой из бесконечности, имея начальный запас кинетической энергии к=1. Приближаясь к первой молекуле, вторая молекула под действием силы притяжения движется со всёвозрастающей скоростью. В результате кинетическая энергия к молекулы растёт, а потенциальная п одновременно уменьшается, но их сумма = к+п = const остаётся неизменной. При прохождении молекулой точки с координатой ro силы притяжения сменяются силами отталкивания, вследствие чего молекула начнёт быстро терять скорость (в области отталкивания кривая п идёт круто вверх). В момент, когда потенциальная энергия п становится равной полной энергии системы 1, скорость молекулы обращается в нуль. В этот момент имеет место наибольшее сближение молекул друг с другом. После остановки молекулы все явления протекают в обратной последовательности.
Минимальное расстояние, на которое сближаются центры двух молекул, называется эффективным диаметром молекулы d. Величина
= d2
называется эффективным сечением молекулы. Как видно из рисунка, эффективный диаметр молекул зависит от их энергии, а следовательно, и от температуры. С повышением температуры эффективный диаметр молекул уменьшается.
Длина свободного пробега молекулы – это путь l, который молекула проходит между двумя последовательными соударениями. Длина свободного пробега – случайная величина. Иной раз молекуле удаётся пролететь между соударениями довольно большой путь, в другой раз этот путь может оказаться весьма малым. Поэтому вводится понятие среднего значения длины свободного пробега = < l >.
За секунду молекула проходит в среднем путь, равный средней скорости < >. Если за секунду она претерпевает в среднем z столкновений, то средняя длина свободного пробега будет равна
 .
.
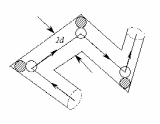
За секунду молекула проходит путь, равный < >. Число происходящих за это время соударений с неподвижными молекулами равно количеству молекул, центры которых попадают внутрь коленчатого цилиндра длины <> и радиуса d.
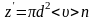 ,
,
где n – число молекул в единице объёма.
В действительности все молекулы движутся, вследствие чего число соударений определяется средней скоростью движения молекул по отношению друг к другу, а не средней скоростью < > молекул относительно стенок сосуда. Относительная скорость движения двух произвольно взятых молекул равна
 .
.
Возведя в квадрат это выражение, получим
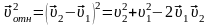 .
.
Средние значения суммы нескольких величин равно сумме средних значений складываемых величин. Поэтому
 .
.
События,
заключающиеся в том, что первая молекула
имеет скорость
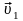 ,
а вторая – скорость
,
а вторая – скорость
 являются статистически независимыми,
поэтому
являются статистически независимыми,
поэтому
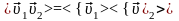 .
Для газа, находящегося в равновесии,
каждый из сомножителей равен нулю. Таким
образом
.
Для газа, находящегося в равновесии,
каждый из сомножителей равен нулю. Таким
образом
 .
.
Полученный результат означает, что
 .
.
Средне квадратичные скорости пропорциональны средним арифметическим. Следовательно
 .
.
Тогда, для среднего числа столкновений за секунду получим выражение
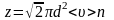 ,
,
а для средней длины свободного пробега следующую формулу
 .
.
Если концентрацию газа определить из соотношения P = nkT, получим другую формулу для средней длины свободного пробега
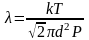 .
.
Для оценки порядка величины и z, рассмотрим следующий пример:
О2 – кислород, Т=300 К, Р=105 Па, эффективный диаметр молекулы кислорода возьмём из таблицы, d=0,3610-9 м. Тогда, для средней длины свободного пробега получим значение порядка ~10-7 м, а число столкновений за секунду z~1010 c-1.
