
- •Закладка
- •2. Взаимодействие лекарственных веществ с рецепторами
- •3. Всасывание, распределение и выведение лекарственных веществ
- •4. Метаболизм лекарственных веществ в организме
- •5. Местные анестетики
- •6. Лекарственные средства, действующие на нервно-мышечную передачу
- •7. Вегетативная нервная система
- •8. Холинергические средства
- •1) Холиномиметики прямого действия (агонисты м- и н-холи-норецепторов);
- •9. Адренергические средства
- •10. Лекарственные средства, действующие на глаза
- •11. Лекарственные средства, применяемые при бронхиальной астме, поллинозе и анафилаксии
- •12. Лекарственные средства, действующие
- •Секреция соляной кислоты
- •13. Лекарственные средства, действующие на жедудочно-кишечный тракт. II. Средства, влияющие на моторику и секрецию
- •14. Лекарственные средства, специфически влияющие на почки:
- •15. Лекарственные средства, применяемые при артериальной гипертензии
- •17. Противоаритмические средства
- •18. Лекарственные средства,
- •19. Лекарственные средства, влияющие на свёртывание крови
- •20. Гиполипидемические средства
- •21. Лекарственные средства, стимулирующие эритропоэз
- •22. Медиаторы центральной системы
- •24. Транквилизаторы и снотворные средства
- •24. Транквилизаторы и снотворные средства
- •25. Противоэпилептические средства
- •26. Препараты, применяемые при паркинсонизме
- •27. Антипсихотические средства — нейролептики
- •28. Средства, применяемые при аффективных состояниях. Антидепрессанты
- •29. Опиоидные (наркотические) анальгетики
- •30. Противорвотные средства. Антиэметики
- •31. Лекарственная зависимость и злоупотребление лекарствами
- •32. Нестероидные противовоспалительные средства
- •33. Препараты гормонов коры надпочечников (кортикостероиды)
- •34. Половые гормоны и их препараты
- •36. Средства, применяемые при сахарном диабете (антидиабетические средства)
- •37. Противомикробные средства,
- •38. Противомикробные средства,
- •39. Противомикробные средства,
- •40. Противогрибковые и противовирусные средства
- •41. Противопаразитарные средства. I. Противоглистные препараты
- •42. Противопаразитарные средства. II. Противопротозойные препараты
- •44. Отравления лекарственными веществами
- •45. Побочное действие лекарств
34. Половые гормоны и их препараты
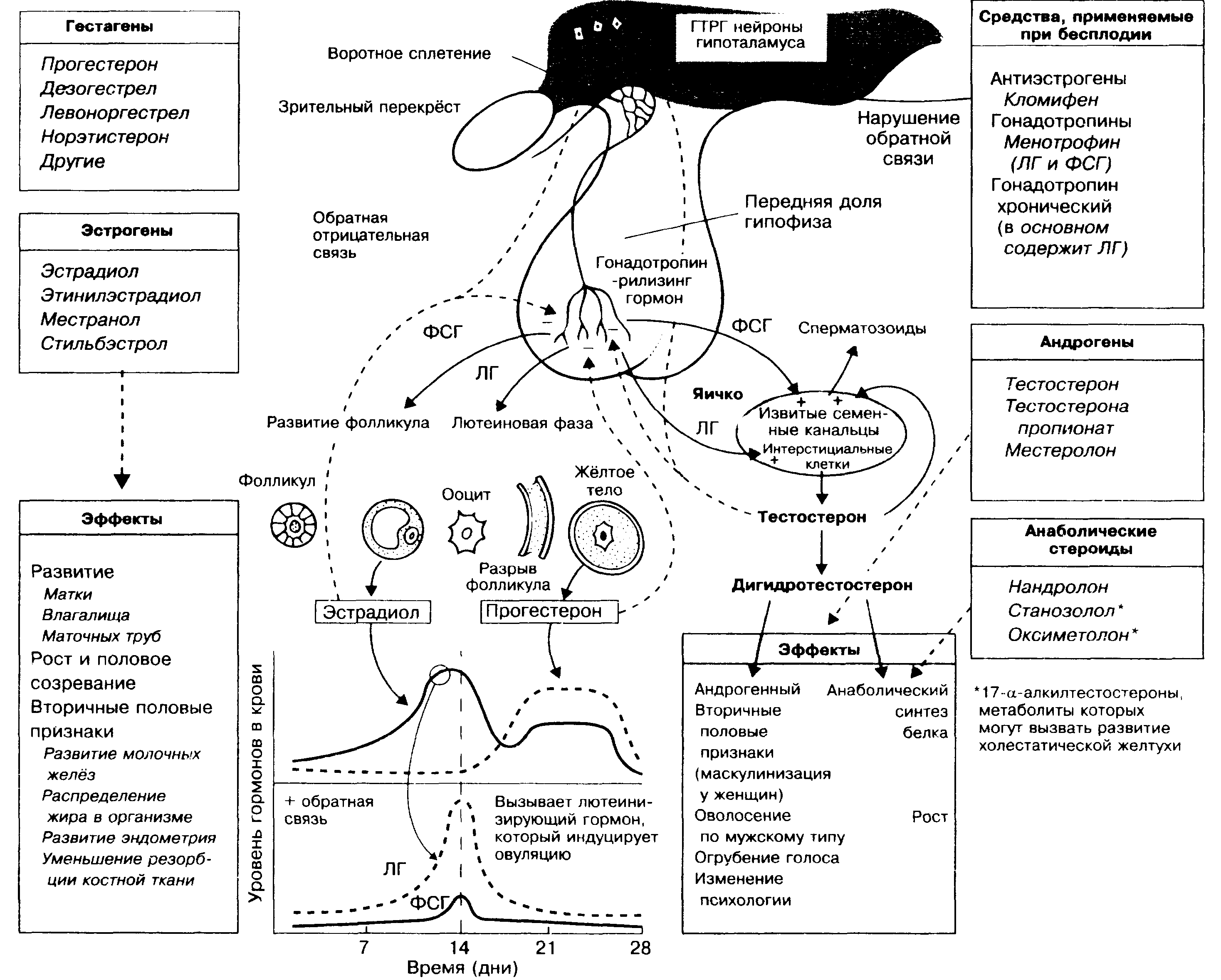
В половых железах (яичниках и яичках) кроме созревания половых клеток (гамет) происходит синтез половых гормонов (эстрогенов и андрогенов соответственно). Секрецию эстроге-нов (в основном эстрадиола) и андрогенов (в основном тестос-терона) стимулируют гонадотропные гормоны передней доли гипофиза (лютеинизирующий — ЛГ и фолликулостимулирую-щий — ФСГ) (в центре рисунка). В свою очередь высвобождение ЛГ и ФСГ регулируется гонадотропин-рилизинг гормонами (фоллиберином и люлиберином) гипоталамуса (ГТРГ; в верхней части рисунка).
В извитых семенных канальцах яичек (на рисунке справа) происходит созревание сперматозоидов. Этот процесс регулируют ФСГ и тестостерон, образующийся в интерстициальных клетках (клетки Лейдига, гландулоциты) мужских половых желез под влиянием Л Г. Тестостерон способствует формированию мужского фенотипа (показано в нижней части рисунка справа). Андрогены (в правой части рисунка в середине) применяют в основном для заместительной терапии после кастрации, при гипогонадизме, развивающемся при некоторых заболеваниях гипофиза или яичек. Тестостерон при пероральном применении быстро инактивируется в печени, тогда как синтетические андрогены (например, местеролон) при приёме внутрь сохраняют свою активность. Анаболические стероиды (в нижней части рисунка справа) обладают слабой андрогенной активностью, их используют в основном в качестве средств, усиливающих синтез белка (например, после тяжёлых хирургических операций, а также при различных хронических заболеваниях). Основными побочными эффектами андрогенов и анаболичсских стероидов (в меньшей степени) являются развитие маскулинизации у женщин и у детей препубертатного возраста, угнетение выработки ФСГ и Л Г.
ФСГ (и ЛГ) стимулирует созревание фолликула в яичниках (в верхней части рисунка слева), а также синтез эстрадиола гранулёзными клетками фолликула. В ранней стадии фоллику-линовой фазы менструального цикла низкий уровень эстрадиола в крови (в середине рисунка слева) способствует усилению высвобождения ФСГ (по принципу обратной связи), который в свою очередь стимулирует созревание фолликула. В середине менструального цикла уровень эстрадиола в крови повышается, что усиливает секрецию ЛГ (по принципу положительной обратной связи), способствуя овуляции. Таким образом, изменение концентрации эстрадиола в крови в различные фазы менструального цикла по принципу обратной связи влияет на выработку ГТРГ в гипоталамусе и гонадотропных гормонов в аденогипофизе. На месте лопнувшего фолликула образуется жёлтое тело, где синтезируются гестагены и эстрогены (в середине рисунка слева) во второй (лютеиновой) фазе менструального цикла. В фолликулиновой фазе менструального цикла под влиянием эстрогенов происходит пролиферация эндометрия (фаза пролиферации). В лютеиновой фазе под влиянием про-гестерона отмечается развитие желез эндометрия (фаза секреции), в дальнейшем в фазе десквамации (менструации) происходит отторжение всего функционального слоя эндометрия.
Эстрогены оказывают много различных эффектов (показаны в нижней части рисунка слева). Эти гормоны используют для заместительной терапии при первичном гипогонадизме и в постменопаузе у женщин (для предупреждения возникновения чувства приливов, атрофического вагинита и остеопороза). Эстрогены применяют при нарушениях менструального цикла (дис-менорее), а в комбинации с гестагенами в качестве контрацептивов. Гестагены (в верхней части рисунка слева) в основном используют для гормональной контрацепции. Половые гормоны и их антагонисты применяют при некоторых видах гормо-нозависимых опухолей (см. главу 43).
ГТРГ (гонадорелин) является декапептидом, стимулирующим высвобождение ФСГ и ЛГ в аденогипофизе. ГТРГ применяют внутривенно при гипоталамическом гипогонадизме.
ФСГ и ЛГ — это гормоны передней доли гипофиза, являющиеся гликопротеинами и регулирующие функционирование половых желез.
Бесплодие
Для лечения ановуляторного бесплодия используют средства, стимулирующие овуляцию в яичниках.
Антиэстрогенные средства кломифен и тамоксифен блокируют рецепторы эстрогенов, нарушая обратную отрицательную связь, что приводит к увеличению высвобождения гипотала-мических рилизинг-факторов лютеинизирующего и фоллику-лостимулирующего гормонов и соответственно ФСГ и ЛГ в аденогипофизе.
При женском бесплодии, связанном с гипофункцией гипофиза, а также при неэффективности кломифена применяют препараты гонадотропииов. В первую фазу менструального цикла для стимуляции созревания фолликула внутримышечно вводят менотрофин (содержит поровну ФСГ и ЛГ) или урофоллитро-фин (ФСГ), затем используют хорионический гонадотропин (в основном содержит ЛГ) в высоких дозах для стимуляции овуляции. После лечения развитие беременности отмечается в среднем у 20—30% женщин. Гонадотропины применяют также для стимуляции сперматогенеза и повышения продукции андроге-нов у мужчин.
Андрогены
Основным андрогеном является тестостерон. Около 2% тес-тостерона циркулирует в плазме крови в свободном состоянии, остальная часть гормона в различных тканях организма (в коже, предстательной железе, в семенных пузырьках и в придатках яичка) превращается в дигидротестостерон. При андрогенной недостаточности внутримышечно вводят пролонгированные препараты тестостерона пропионата.
Эффекты андрогенов. Андрогены вызывают развитие вторичных половых признаков у мужчин. Применение андрогенов в высоких дозах у мужчин угнетает высвобождение гонадотроп-ных гормонов и приводит к атрофии интерстициальной ткани и извитых канальцев яичек. У женщин андрогены вызывают маскулинизирующий эффект (вирилизм).
Эстрогены
Основным эстрогеном, высвобождающимся из яичников, является эстрадиол. Однако для перорального применения более эффективными являются синтетические эстрогены.
Побочные эффекты (см. также в разделе: пероральные контрацептивы). Длительное применение эстрогенов вызывает гиперплазию эндометрия, способствует появлению маточных кровотечений и увеличивает частоту возникновения карциномы эндометрия. При комбинированном применении эстрогенов с гестагенами частота развития рака яичников и эндометрия снижается.
Гестагены
Гестагены применяют для гормональной контрацепции, при гипофункции яичников, а также при различных гинекологических заболеваниях (например, при дисменорее, эндометрио-зе. гирсутизме, маточных кровотечениях).
Пероральные контрацептивы
Комбинированные гестаген-эстрогенные контрацептивы применяют ежедневно в течение 21-го дня (с 5-го дня менструального цикла), затем следует 7-дневный перерыв, когда появляется менструальноподобная реакция.
Контрацептивы, содержащие малые дозы гестагенов (мини-пили) применяют постоянно (без перерывов).
Для гормональной контрацепции используют два эстроге-на — этинилэстрадиол и местранол. Следует отметить, что одновременный приём пероральных контрацептивов со средствами, вызывающими индукцию микросомальных ферментов печени (например, фенобарбитал, карбамазепин, дифенин и особенно рифампицин) снижает эффективность гормональной контрацепции.
Механизм действия. Комбинированные гестаген-эстрогенные контрацептивы по принципу обратной связи угнетают высвобождение гипоталамических рилизинг-факторов гонадотропных гормонов и соответственно гонадотропных гормонов аденоги-пофиза, что приводит к нарушению процессов овуляции (возникновению ановуляторных циклов). Вместе с тем гормональные контрацептивы вызывают изменения эндометрия, препятствующие имплантации оплодотворенной яйцеклетки, изменяют состав и количество цервикальной слизи и нарушают транспорт яйцеклетки по фаллопиевым (маточным) трубам. Эти механизмы контрацептивного действия имеют особое значение при применении препаратов гестагенов (мини-пили), так как при этом овуляция отсутствует только у 25% женщин. При использовании мини-пили отмечается развитие нерегулярного менструального цикла.
Побочные эффекты. Основными осложнениями гормональной контрацепции (как комбинированных гестаген-эстрогенных препаратов, так и мини-пили) являются: маточные кровотечения, увеличение массы тела, изменение либидо, «нагрубание» грудных желез, головная боль и тошнота. Комбинированные контрацептивы могут вызвать развитие депрессии, появление гир-сутизма и грибковой инфекции влагалища. Нежелательные эффекты гормональной контрацепции отмечаются в среднем у 20—30% женщин (10—15% женщин из-за появления побочных эффектов прекращают приём контрацептивов). При применении только гестагенов (мини-пили) осложнения наблюдаются реже. Основными побочными эффектами этих препаратов являются маточные кровотечения и нарушения менструального цикла.
Серьёзные побочные эффекты гормональной контрацепции отмечаются редко. К ним относятся развитие холестатической желтухи и тромбоэмболических осложнений, которые, вероятно, связаны с действием эстрогенов. Вместе с тем отмечено, что тромбоэмболические осложнения отмечаются чаще при использовании комбинированных препаратов, содержащих ге-стоден и дезогестрел. Курение, артериальная гипертензия, наличие тромбоэмболий в анамнезе, сахарный диабет повышают риск развития тромбоэмболических осложнений при перораль-ной контрацепции.
Средства, обладающие абортивным действием
Прогестерон способствует сохранению беременности, тогда как антагонисты прогестерона (например, мифепристон) обладают способностью прерывать беременность в основном на её ранних стадиях, особенно при комбинированном применении с простагландинами. Основными побочными эффектами химического аборта являются болевые ощущения и маточные кровотечения.

В щитовидной железе синтезируются йодсодержащие гормоны: трийодтиронин (Тз) и тироксин (тетрайодтиронин, Т^), регулирующие процессы роста, развития, дифференцировки тканей и активирующие обмен веществ в организме. В пара-фолликулярных клетках щитовидной железы образуется каль-цитонин, участвующий в регуляции обмена кальция.
Для синтеза трийодтиронина и тироксина необходимы йо-диды, которые обычно поступают в организм с пищей. Йодиды (1~) поглощаются фолликулярными клетками (тироцитами) (в центре рисунка) за счёт активного транспорта (на рисунке показано в виде t=>). Этот процесс контролируется тиреотропным гормоном (ТТГ). В субапикальной зоне цитоплазмы тироцитов при участии пероксидазы происходит быстрое окисление иоди-дов в более активный атомарный йод (1°). Йодирование тире-оглобулина (содержит в своём составе тирозин и его производные — тиронины) приводит к образованию тиреоидных гормонов: тироксина (Т4 показан на рисунке в виде ^) и трийодтиронина (Тз показан на рисунке в виде (У). Эти йодтиронины содержатся в коллоиде фолликулов щитовидной железы в составе молекул тиреоглобулина.
Высвобождение Тз и Т4 фолликулами щитовидной железы регулируется по принципу обратной связи (показано в верхней части рисунка). При снижении уровня Тз и Т4 в крови увеличивается выделение тиреотропина (тиреотропного гормона, ТТГ) из передней доли гипофиза, что приводит к усилению реабсор-бции коллоида (путём эндоцитоза) в клетки фолликулов. В цитоплазме тироцитов капли коллоида сливаются с лизосомами, в результате чего протеолитические ферменты лизосом расщепляют тиреоглобулины, высвобождая Тз и Т4 в кровь. Тиреоид-ные гормоны (Тз и Т4) взаимодействуют с рецепторами (Р) на мембранах клеток и внутриклеточными рецепторами (в нижней части рисунка), вызывая различные эффекты (показаны на рисунке справа).
Нарушения функции щитовидной железы (гипер- и гипоти-реоз) являются наиболее частой эндокринной патологией, они отмечается у 2% населения (в 2—3% случаев эти нарушения сочетаются с сахарным диабетом). При Базедовой болезни (ги-пертиреоидизме) повышение функции щитовидной железы связано с выработкой специфических антител (LATS — длительно действующих тиреоидных стимуляторов), которые стимулируют ТТГ-рецепторы, что приводит к избыточной продукции тиреоидных гормонов (Тз и Т4). При повышенной функции щитовидной железы используют антитиреоидные средства, радиотерапию (I131) и хирургическое лечение. Для уменьшения повышенного тонуса симпатической нервной системы при гипертиреоидизме используют р-адреноблокаторы (например, пропранолол). При Базедовой болезни часто развивается офтальмопатия аутоиммунного генеза, трудно поддающаяся лечению.
Первичный гипотиреоидизм (микседема) в большинстве случаев возникает вследствие клеточного иммунного ответа против фолликулярных клеток щитовидной железы. Препаратом выбора для проведения заместительной терапии при гипотире-озе является гироксин.
Тиреотропин-рилизинг гормон (ТТРГ) является трипептидом. Этот гормон синтезируется в гипоталамусе и транспортируется по капиллярам гипофизарной портальной венозной системы в гипофиз, где стимулирует синтез и высвобождение ТТГ.
ТТГ. Тиреотропный гормон является гликопротеином, высвобождающимся из передней доли гипофиза (аденогипофиза). ТТГ активирует аденилатциклазу, которая стимулирует синтез и высвобождение Тз и Т4 из щитовидной железы. Повышение уровня ТТГ при гипотиреоидизме или при недостаточном поступлении йода в организм (реже) приводит к увеличению размеров щитовидной железы (формированию зоба).
Циркулирующие в крови тиреоидные гормоны (Тз и Т4) почти полностью связаны с белками плазмы крови (99,5% и 99,95% соответственно). В фолликулах щитовидной железы синтезируется только около 20% Тз, остальное количество этого гормона образуется в периферических тканях из Т4 (путём отщепления йода от его молекулы). Таким образом, Т4 является основным предшественником Тз.
Механизм действия. Механизм действия тиреоидных гормонов полностью не изучен. Известно, что гормоны щитовидной железы обладают высоким сродством к рецепторам ядра клеток, митохондрий и цитоплазматических мембран. Взаимодействие тиреоидных гормонов с рецепторами приводит к развитию различных эффектов (в том числе к усилению синтеза белка и повышению обмена веществ). Большинство тиреоидных рецепторов являются внутриклеточными. Ядерные рецепторы для Тз (так же как и стероидные рецепторы и рецепторы витамина D) кодируются семейством генов, родственных цис-он-когенам. Свободные тиреоидные гормоны (Тз и Т4) проникают в клетку с помощью специального механизма переноса. В цитоплазме клеток большая часть Т4 превращается в Тз (или рТз — реверсивный Тз), который связывается с С-терминалями тиреоидных рецепторов и вызывает конформационные изменения в их ДНК-связывающем участке. Активированные тиреоидные рецепторы взаимодействуют с молекулами ДНК. В результате изменяются процессы транскрипции генов, а синтез белка стимулируется или угнетается.
Гипертиреоидизм (тиреотоксикоз)
При гипертиреоидизме отмечается усиление основного обмена, повышение температуры тела, развитие сердечной аритмии и повышение аппетита. Кожные покровы становятся тёплыми и влажными. Увеличивается нервная возбудимость и возникает гиперкинезия. Повышение активности симпатической нервной системы способствует развитию тахикардии, повышенной потливости и тремора. Может развиваться стенокардия и сердечная недостаточность. Отмечается появление ретракции верхнего века (симптом Кохера) и развитие экзофтальма.
При гипертиреоидизме у лиц молодого возраста применяют антитиреоидные средства, при рецидивах тиреотоксикоза выполняют субтотальную резекцию щитовидной железы. Пациентам старше 40 лет проводят радиоактивную терапию йодом (I131). При гипертиреозе у пациентов молодого возраста можно применять длительную радиотерапию (I131) в сочетании с приёмом карбимазола.
Антитиреоидные средства
Тионамиды содержат активную тиокарбамидную группу (S = С—Н). Эти соединения угнетают синтез тиреодных гормонов, подавляя катализируемые каталазой процессы образования активной формы йода. В результате отмечается нарушение процессов йодирования тирозина и превращения йодтиро-зина в дийодтиронин. Вместе с тем, возможно, что тионамиды оказывают иммуносупрессорное действие (снижают уровень LATS в крови). Антитиреоидные средства применяют перораль-но. Препараты накапливаются в щитовидной железе, однако их действие проявляется не сразу, а после истощения запасов тиреоидных гормонов в организме (в среднем через 3—4 недели).
Карбимазол в организме быстро превращается в метимазол (метилмеркаптоимидазол — мерказолил). Препарат используют с целью создания у больного эутиреоидного состояния, а затем уменьшенные дозы карбимазола применяют для поддерживающей терапии. Часто возникает возможность прекратить лечение через 1—2 года. Побочные эффекты карбимазола включают появление кожной сыпи, редко развитие агранулоцитоза (у некоторых пациентов отмечается болезненность при глотании).
При непереносимости пациентами карбимазола используют пропилтиоурацил. Этот препарат вызывает развитие агранулоцитоза чаще (0,4%), чем карбимазол (0,1%). Пропилтиоурацил не только угнетает синтез тиреоидных гормонов, но также тормозит превращение Т4 в Тз в периферических тканях и, возможно, оказывает иммуносупрессорное действие.
Препараты йода. Механизм действия препаратов йода при гипертиреозе изучен недостаточно. Йодиды угнетают синтез и высвобождение тиреоидных гормонов (возможно, нарушая процессы протеолитического расщепления тиреоглобулинов). Вместе с тем йодиды уменьшают объём и васкуляризацию гиперп-лазированной щитовидной железы. Препараты йода применяют для предоперационной подготовки пациентов к тиреоидэк-томии, а в комбинации с другими средствами — для купирования тиреотоксического криза (при этом исчезновение тирео-токсических симптомов наблюдается в течение 2—7 дней). Препараты йода при гипертиреоидизме нельзя использовать длительное время, так как в этом случае снижается их антити-реоидная активность.
Бета-адреноблокаторы пропранолол (анаприлин) и атенолол уменьшают частоту сердечных сокращений и выраженность других проявлений гипертиреоидизма (до их полного устранения мерказолилом). Их применяют в процессе предоперационной подготовки к тиреоидэктомии. При тиреотоксическом кризе пропранолол используют в комбинации с гидрокортизоном, мерказолилом и препаратами йода.
Гипотиреоидизм
Наиболее частыми симптомами гипотиреоза являются чувство усталости и сонливость. К другим проявлениям заболевания относятся угнетение основного обмена, понижение аппетита, уменьшение сердечного выброса вплоть до развития сердечной недостаточности. Характерным признаком гипотиреоза является сухость кожных покровов. Недостаточность тиреоидных гормонов в раннем детском возрасте приводит к задержке умственного и физического развития (кретинизм). Возникающие изменения носят необратимый характер, поэтому гипоти-реоз необходимо диагностировать как можно раньше и назначать заместительную терапию тиреоидными гормонами с самого рождения ребенка.
Заместительная терапия
Препаратом выбора для проведения заместительной терапии при гипотиреозе является тироксин. Наиболее часто применяют синтетический тироксин 04), который представляет собой натриевую соль L-тироксина. При его применении отмечается латентный период, продолжительность которого определяется временем насыщения тироксином белков плазмы крови и тканевых рецепторов. Фармакотерапия тиреоидными гормонами должна проводиться под контролем уровня ТТГ в плазме крови, так как его содержание в крови нормализуется при достижении оптимальных доз тироксина.
Лиотиронин является натриевой солью трийодтиронина. Препарат меньше связывается с белками плазмы крови, поэтому действует быстрее, чем тироксин. Лиотиронин в основном применяют внутривенно в комбинации с гидрокортизоном при ги-потиреоидной (микседематозной) коме.
