
- •1 Траектория, путь, перемещение. Скорость движения точки по прямой. Нахождение координаты по известной зависимости скорости от времени.
- •2. Векторный и координатный способы описания движения точки в пространстве. Скорость (средняя, линейная, мгновенная) и ускорение. Вычисление пройденного пути и перемещения.
- •3. Движение материальной точки по окружности (равномерное и произвольное). Баллистическое движение. Криволинейное движение точки в пространстве.
- •4. 3Акон инерции. Инерциальные системы отсчета. Второй закон Ньютона. Третий закон Ньютона и область его применимости.
- •5. Сила упругости. Закон Гука
- •7. Закон сохранения импульса в изолированной системе из двух материальных точек. Изменение импульса системы материальных точек. Импульс силы.
- •8. Теорема о движении центра масс.
- •9. Движение тел с переменной массой. Уравнение Мещерского, уравнение Циолковского.
- •10. Работа силы. Мощность. Геометрическая форма представления работы.
- •11. Кинетическая энергия материальной точки. Связь кинетической энергии с работой сил. Теорема Кенига.
- •14. Вращение твердого тела вокруг неподвижной оси. Угловая скорость и угловое ускорение как векторные величины. Связь между векторами скорости и угловой скорости.
- •15. Момент инерции. Уравнение динамики вращательного движения твердого тела. Момент инерции твердого тела
- •16. Работа при вращении тела. Условия равновесия твердого тела.
- •19. Система отсчета равномерно вращается (материальная точка покоится в нисо, материальная точка движется в нисо). Теорема Кориолиса.
- •20. Законы Кеплера и обобщение Ньютона (закон всемирного тяготения). Сила тяжести. Поле тяготения. Космические скорости.
- •22. Гармонический осциллятор. Превращения энергии при колебаниях осциллятора. Примеры гармонических осцилляторов (физический маятник, математический маятник).
- •23. Плотность среды и давление в гидростатике. Основные законы гидростатики. Барометрическая формула.
- •24. Понятие потока жидкости (газа) и уравнение непрерывности. Вывод уравнения Бернулли. Теорема Торричелли. Течение в горизонтальной трубе.
- •26. Параметры, определяющие состояние вещества. Идеальный газ. Вывод основного уравнения кинетической теории газов. Вывод основных газовых законов. Уравнение состояния идеальных газов.
- •27. Универсальная газовая постоянная. Средняя квадратичная скорость молекул. Постоянная Больцмана и средняя кинетическая энергия одной молекулы.
- •30. Теплоемкость, закон Джоуля, уравнение Роберта Майера.
- •31. Первый закон термодинамики. Работа газа при изменении объема.
- •32. 0Братимые и необратимые процессы. Равновесные и неравновесные процессы. Изопроцессы в газах.
- •34. Адиабатный процесс. Уравнение Пуассона, адиабата. Политропный процесс, уравнение политропы.
- •35. Круговые процессы или циклы. Идеальная тепловая машина и цикл Карно. К.П.Д. Идеальной тепловой машины. К.П.Д. Реальной тепловой машины.
- •36. Содержание второго закона термодинамики.
- •37. Неравенство Клаузиуса. Энтропия. Изменение энтропии при обратимых и необратимых процессах. Изменение энтропии в процессах идеального газа.
- •9.14 Теорема Клаузиуса
- •38. Энтропия и вероятность. Статистический характер второго закона термодинамики. Третье начало термодинамики.
- •39. Реальные газы. Межмолекулярные силы.
- •40. Уравнение Ван - дер - Ваальса. График уравнения Ван - дер - Ваальса.
36. Содержание второго закона термодинамики.
Второе начало термодинамики:
Невозможно построить периодически действующую тепловую машину, которая бы всю подводимую к ней теплоту превращала в работу, т.е. всегда .
Энтропия и второе начало термодинамики
Понятие
энтропии имеет статистическое толкование.
Состояние макроскопического тела (т.е.
тела, образованного огромным количеством
молекул) может быть задано с помощью
объёма, давления, температуры, внутренней
энергии и других макроскопических
величин. Охарактеризованное таким
способом состояние называется
макросостоянием. Состояние
макроскопического тела, охарактеризованное
настолько подробно, что оказываются
заданными состояния всех образующих
тело молекул, называется микросостоянием.
Всякое макросостояние может быть
осуществлено различными способами,
каждому из которых соответствует
некоторое микросостояние тела. Число
различных микросостояний, соответствующих
данному макросостоянию, называется
статистическим весом
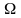 или термодинамической вероятностью
макросостояния. В статистической
физике существует теорема, которая
утверждает о равновероятности всех
микросостояний данной системы. В
качестве характеристики вероятности
состояния можно было бы выбрать
статистический вес
,
однако такая характеристика не обладала
бы свойствами аддитивности. Поэтому в
качестве характеристики состояния
принимается величина S,
пропорциональная логарифму статистического
веса
.
или термодинамической вероятностью
макросостояния. В статистической
физике существует теорема, которая
утверждает о равновероятности всех
микросостояний данной системы. В
качестве характеристики вероятности
состояния можно было бы выбрать
статистический вес
,
однако такая характеристика не обладала
бы свойствами аддитивности. Поэтому в
качестве характеристики состояния
принимается величина S,
пропорциональная логарифму статистического
веса
.
 (4). где
(4). где
 - постоянная Больцмана. Такую величину
называют энтропией. Определённая
таким образом энтропия обладает
следующими свойствами:
- постоянная Больцмана. Такую величину
называют энтропией. Определённая
таким образом энтропия обладает
следующими свойствами:
Энтропия изолированной системы при протекании необратимого процесса возрастает. Действительно, изолированная, т.е. предоставленная самой себе, система переходит из менее вероятных в более вероятные состояния, что сопровождается ростом величины (4).
Энтропия системы, находящейся в равновесном состоянии, максимальна.
Эти
утверждения и составляют содержание
второго начала термодинамики:
Энтропия изолированной системы может
только возрастать, (либо по достижении
максимального значения оставаться
неизменной), т.е.
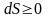 .
.
37. Неравенство Клаузиуса. Энтропия. Изменение энтропии при обратимых и необратимых процессах. Изменение энтропии в процессах идеального газа.
9.14 Теорема Клаузиуса
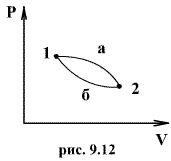
Рассмотрим
обратимый процесс по пути 1а2 и 2б1. Т.к.
процессе 1а2б1 обратимый, то для него
справедливо равенство Клаузиуса
![]()
 Разобьем этот интеграл на два: по пути
1а2 и 2б1
Разобьем этот интеграл на два: по пути
1а2 и 2б1
![]() Поменяем пределы интегрирования второго
интеграла
Поменяем пределы интегрирования второго
интеграла
![]() или
или
![]() Таким образом, сумма приведенных теплот
при переходе из одного состояния в
другое не зависит от формы (пути) перехода
в случае обратимых процессов. Последнее
утверждение носит название теоремы
Клаузиуса.
Таким образом, сумма приведенных теплот
при переходе из одного состояния в
другое не зависит от формы (пути) перехода
в случае обратимых процессов. Последнее
утверждение носит название теоремы
Клаузиуса.
Если же 2б1 я-ся необратимым неравновесным способом то ΔS≥0 (интеграл 1а2 больше) неравенство клаузиуса. Изменение энтропии замкнутой системы может либо равняться улю или возрастать для необратимого процесса.
9.15
Энтропия Из теоремы
Клаузиуса следует, что приведенная
теплота подобно энергии (потенциальной,
внутренней) является функцией состояния
(не зависит от пути перехода и зависит
только от состояния системы). Независимость
интеграла
от пути перехода означает, что этот
интеграл выражает собой изменение
некоторой функции состояния системы,
она называется энтропия и обозначается
буквой S. Изменение энтропии системы,
очевидно, равно![]() .
Мы говорим только об изменении энтропии
(подобно изменению потенциальной
энергии
.
Мы говорим только об изменении энтропии
(подобно изменению потенциальной
энергии
![]() ,
для которой не важно где начало отсчета).
Из уравнения что выше вытекает основное
количественное выражение второго
начала термодинамики
,
для которой не важно где начало отсчета).
Из уравнения что выше вытекает основное
количественное выражение второго
начала термодинамики
Энтропия
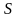 – это такая функция состояния,
дифференциал которой определяется
отношением:
– это такая функция состояния,
дифференциал которой определяется
отношением:
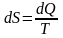 .
В СИ энтропия
измеряется в Дж/К. Приведём формулы для
подсчёта изменения энтропии в случае
изопроцессов для идеального газа:
.
В СИ энтропия
измеряется в Дж/К. Приведём формулы для
подсчёта изменения энтропии в случае
изопроцессов для идеального газа:
а)
Изохорический процесс:
 ,
,
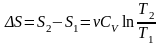 .
.
б)
Изобарический процесс:
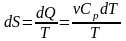 ,
,
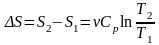 .
.
в)
Изотермический процесс:
 ,
,
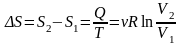 .
.
г)
Адиабатический процесс:
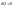 ,
,
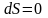 ,
,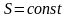 .
.
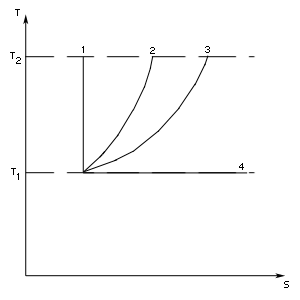
 - адиабатический
процесс,
- адиабатический
процесс,
 - изохорический
процесс,
- изохорический
процесс,
 - изобарический
процесс,
- изобарический
процесс,
 - изотермический
процесс.
- изотермический
процесс.
