
- •Федеральное агентство по образованию
- •Содержание:
- •Введение
- •1.Литературный обзор.
- •1.1. Углерод – углеродные материалы на основе ту.
- •1.1.1. Заполнение пористого пространства пироуглеродом (зауглероживание).
- •Константы скорости образования пу, при различных температурах с использованием метана и ацетилена.
- •1.1.2. Формирование пористой структуры в процессе активации уплотненной матрицы.
- •1.1.3. Модифицирование поверхностных свойств углеродных носителей
- •1.1.4. Свойства пористых уукм, типа “Сибунит”.
- •Свойства пористых углеродных материалов типа сибунита
- •1.2. Углеродные нановолокна
- •1.2.2. Морфология унв
- •2. Экспериментальная часть.
- •2.1. Определение адсорбционной активности по метиловому оранжевому
- •2.1.1. Построение градуировочного графика
- •2.1.2. Проведение анализа
- •2.2. Метод КомпАс.
- •2.2.1. Определение удельной адсорбционной поверхности углеродных материалов по методу КомпАс
- •2.2.2 Определение структурности и дисперсности углеродных материалов по методу КомпАс
- •Формулы расчета характеристик дисперсного материала
- •2.3. Отработка методики определения окислительной стабильности углеродных материалов
- •2.3.1. Неизотермический режим.
- •Расчет линеаризации температурной зависимости для 1 участка сажи n234
- •Кинетические параметры для саж n234 и n234gr
- •2.3.2. Изотермический режим.
- •Скорости реакции на расчетных участках
- •Значения констант скоростей для саж n234 и n234 gr.
- •Энергия активации саж n234 и n234gr, при окислении в изотермическом режиме.
- •2.4.Результаты исследований и их обсуждение
- •2.4.1.Изучение свойств исходных материалов
- •Значения энергий активации и констант скоростей окисления исходных образцов
- •2.4.2. Изучение закономерностей уплотнения пиролитическим углеродом исходных материалов и свойств образующегося продукта
- •Сорбционная активность уплотненных (степень заполнения 100 %) материалов
- •2.4.3. Изучение закономерностей активации уплотненных материалов и свойств образующегося продукта
- •Значения энергий активации и констант скорости при окислении удунв, уунв, уn234
- •2.5. Сравнение сорбционных характеристик полученных уукм с характеристиками существующих сорбентов такого типа.
- •Сорбционные характеристики углеродных материалов
- •Список литературы:
Скорости реакции на расчетных участках
Сажа N234gr |
|||
Скорость: |
Температура, оС |
||
1020 |
1040 |
1070 |
|
На стабильных участках, г/мин •107 |
2,63 |
4,6 |
7,15 |
90 % окислен., г/мин • 107 |
1,38 |
2,13 |
4,1 |
Сажа N234 |
|||
Скорость: |
Температура, оС |
||
1020 |
1055 |
1085 |
|
На стабильных участках, г/мин •107 |
5,56 |
9,4 |
12,4 |
90 % окислен., г/мин • 107 |
3,67 |
6,22 |
8,53 |
4. Расчет константы скорости.
В таблице 7 представлены константы скоростей для испытуемых саж.
Таблица 7
Значения констант скоростей для саж n234 и n234 gr.
N234 |
Температура, oC |
||
1020 |
1055 |
1085 |
|
Константа скорости на стабильных (участок 1) участках, мин-1 • 107 |
1,68 |
2,80 |
3,99 |
Константа скорости 90 % окислен. (участок 2), мин-1• 107 |
0,93 |
2,00 |
5,00 |
N234gr |
Температура, oC |
||
1020 |
1040 |
1070 |
|
Константа скорости на стабильных (участок 1) участках, мин-1 • 107 |
0,84 |
1,48 |
2,30 |
Константа скорости 90 % окислен. (участок 2), мин-1 • 107 |
0,24 |
6,86 |
2,98 |
Логарифм константы скорости будет:
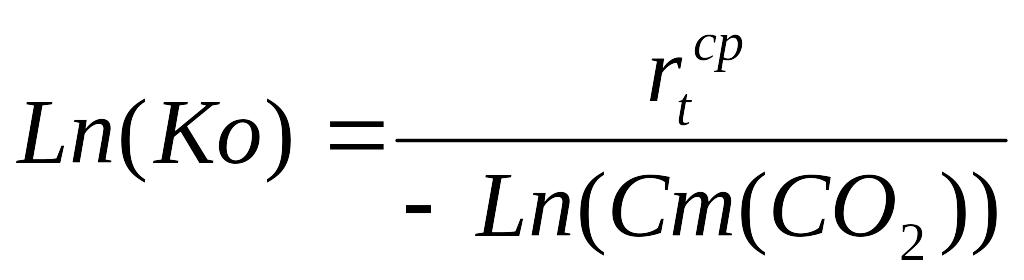 (18)
(18)
Где: Ко – константа скорости, [мин-1]
![]() –
средняя скорость
реакции, при температуре t, [г/мин]
–
средняя скорость
реакции, при температуре t, [г/мин]
Сm (СО2) – мольная концентрация СО2, [моль-1]
Константа скорости равна:
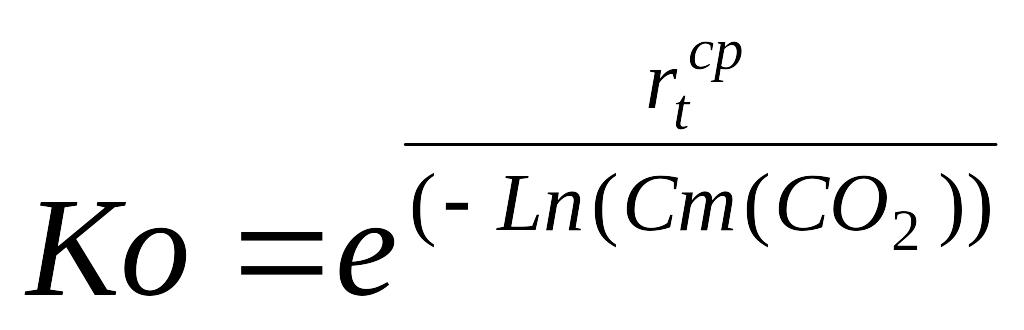 (19)
(19)
Константа скорости для средней скорости стабильного участка кривой окисления сажи N234 при 1085 оС:
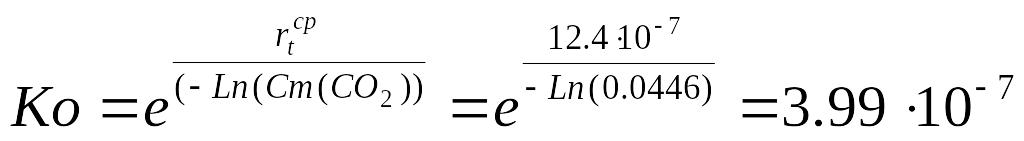 ,
мин-1
,
мин-1
5. Расчет энергии активации.
Строится зависимость константы скорости от обратной температуры.
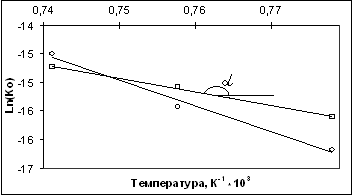
Рис 26. Зависимость логарифма константы скорости от обратной температуры для сажи марки N234
![]() - 1 участок,
- 1 участок,
![]() - 2 участок, α – угол наклона прямой.
- 2 участок, α – угол наклона прямой.
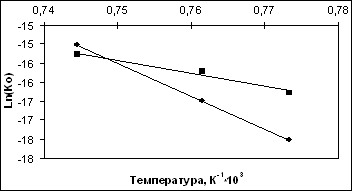
Рис 27. Зависимость логарифма константы скорости от обратной температуры для сажи марки N234gr
![]() - 1 участок,
- 1 участок,
![]() - 2 участок.
- 2 участок.
В таблице 8 представлена информация по энергиям активации испытуемых саж.
Таблица 8
Энергия активации саж n234 и n234gr, при окислении в изотермическом режиме.
N234 |
||
|
Участок 1 |
Участок 2 |
Ea, кДЖ |
215 |
446 |
N234rg |
||
|
Участок 1 |
Участок 2 |
Ea, кДЖ |
282 |
719 |
Энергия активации Ea:
![]() (20)
(20)
Где: Еa – энергия активации, [кДж]
R – универсальная газовая постоянная, 8,314 [Дж/(К·моль)]
Проанализировав таблицы 8 и 6, относящиеся к рассматриваемым нами режимам окисления видно, что средняя ошибка по значениям активации не превышает 10 % (для кинетических исследований допустимое расхождение составляет 20 %) Таким образом, предложенный нами режим кинетических исследований (неизотермический) дает объективную информацию. Но, хотелось бы отметить, что изотермический режим более трудоемок и требует гораздо большего времени, поэтому все дальнейшие исследования кинетических параметров проводились в соответствии с методом анализа в неизотермическом режиме окисления.
