
- •1. Вид Государственной итоговой аттестации:
- •Объем времени на подготовку итоговой аттестации:
- •Сроки проведения итоговой аттестации:
- •Необходимые экзаменационные материалы:
- •5.Условия подготовки и процедура проведения Государственной итоговой аттестации (далее гиа).
- •6.Формы проведения Государственной итоговой аттестации
- •7.Критерии оценки уровня и качества подготовки выпускника.
- •Перечень теоретических вопросов и практических задач, выносимых на 1этап итогового междисциплинарного экзамена по специальности Дисциплина «Аналитическая химия»
- •Дисциплина «Аналитический контроль объектов окружающей среды»
- •Дисциплина «Спектральный анализ»
- •Дисциплина «Физико-химические методы анализа»
- •Перечень заданий на выполнение практических (лабораторных) задач, выносимых на 2 этап итогового междисциплинарного экзамена по специальности (демонстрация профессиональных умений и навыков)
- •Перечень профессиональных задач на 3 этапе итогового междисциплинарного экзамена по специальности
- •Перечень приборов, оборудования и материалов для решения профессиональных задач на 2 этапе имдэ
- •Приложение 5 Список учебной литературы
- •Перечень справочной литературы
Дисциплина «Спектральный анализ»
1.Атомно-эмиссионный спектральный анализ, (АЭСА).
1.1.Периодическая система Д.И Менделеева и атомные спектры. Изменение спектральных свойств элементов по группам и периодам. Классификация элементов по энергиям возбуждения и ионизации; по сложности спектра. Особенности спектральных свойств d и f элементов. Рассмотрите на примере элементов: калий, алюминий, бром, марганец. Укажите элементы с самой высокой и самой низкой энергией ионизации. В спектре какого элемента самое большое число линий?
1.2.Назначение источника света в АЭСА. Классификация источников и области их применения. Процессы, происходящие в источнике света. Интенсивность спектральной линии атомов и ионов. Аналитические и спектральные характеристики дуговых и искровых источников света.
1.3.Индуктивно связанная плазма (ИСП)- источник света в АЭСА. Конструкция и принцип действия. Основные достоинства ИСП по сравнению с традиционными источниками.
1.4.Принципиальная схема спектрального прибора. Классификация приборов. Основные характеристики спектральных приборов, области их применения. Современные приборы. Многоканальные спектрометры.
1.5.Выбор условий количественного АЭСА: выбор аналитических пар линий, стандартных образцов, источника света и спектрального прибора. Отбор и подготовка проб к анализу.
1.6.Методы количественного АЭСА: метод 3-х стандартных образцов, метод постоянного градуировочного графика, метод добавок. Координаты градуировочных графиков при различных методах регистрации.
1.7.Погрешности в количественном АЭСА. Причины их возникновения и способы уменьшения и учета.
1.8.Способы уменьшения систематической погрешности в АЭСА, связанной с влиянием 3-х элементов на интенсивность аналитической линии:
а) метод добавок; б) введение спектроскопического буфера.
1.9.Содержание калия в воде установили методом пламенной атомно-эмиссионной спектрометрии (ПАЭС). Данные для определения даны в таблице.
Параметр |
Градуировочные растворы 1 2 3 4 |
Исследуемый раствор |
|||
Концентрация мг/мл |
50 |
40 |
30 |
10 |
|
Аналитический сигнал (I. A) |
0,10 |
0,079 |
0,062 |
0,020 |
0,048; 0,051,0,048, 0,053, 0,052 |
Рассчитайте:
Среднеарифметическую концентрацию
Стандартное отклонение (S)
Доверительный интервал погрешностей (ΔС)
Доверительный интервал концентраций (С ± ΔС)
Для расчетов воспользуйтесь ПК.
1.10.Определите концентрацию олова в медном сплаве по данным, полученным спектрографическим методом 3-х стандартных образцов
№ обр. |
СSn |
SSn |
SCu |
1 |
0,12 |
0,81 |
1,61 |
0,85 |
1.63 |
||
0,78 |
1,58 |
||
2 |
0,36 |
1,24 |
1,58 |
1,17 |
1,52 |
||
1,21 |
1,56 |
||
3 |
1,25 |
1,67 |
1,58 |
1,56 |
1,49 |
||
1,72 |
1,66 |
||
4 |
|
1,00 |
1,58 |
1,05 |
1,64 |
||
1,15 |
1,50 |
||
|
|
1,20 |
1,78 |
Проверьте данные на «выбросы» по Q критерию.
Постройте градуировочный график и определите концентрацию олова в сплаве
Для расчета используйте ПК.
1.11.Содержание меди в серебреном сплаве определили атомно-эмиссионным методом. Получили следующие данные:
№ обр. |
С Cu % |
S Cu |
S Ag |
1 |
0,35 |
0,28 |
0,62 |
2 |
0,42 |
0,32 |
0,62 |
3 |
0,54 |
0,35 |
0,61 |
4 |
C x |
0,38 |
0,62 |
Определить концентрацию меди в сплаве.
Назовите другие методы спектрального анализа, с помощью которых можно провести аналогичный анализ.
2. Атомно-абсорбционный спектральный анализ ААСА
2.1.Теоретические основы атомно-абсорбционного анализа. Причины отклонения от закона Бугера-Ламберта-Бера.
2.2. Количественный ААСА. Погрешности ААСА.
2.3.Примеры применения атомно-абсорбционного анализа.
2.4. Атомно-абсорбционные спектрометры. Принципиальная схема.
2.5.Основные узлы атомно-абсорбционного спектрометра (спектрофотометра): источник света, атомизатор, монохроматор, приемник света (детектор) и регистрирующий прибор.
3.2.Методом атомно-абсорбционного анализа определили концентрацию никеля в воде после промывки никелированных деталей. Для анализа использовали метод добавок. Определите концентрацию никеля в пробе воды. Данные для определения смотрите в таблице
Концентрация добавки мг/мл |
0 |
0,015 |
0,032 |
0,058 |
Абсорбционность |
0,71 |
0,60 |
0,75 |
0,92 |
1.Постройте градуировочный график
2.Рассчитайте коэффициент корреляции и удостоверьтесь, что наблюдается линейная зависимость между абсорбционностью и концентрацией
Рассчитайте коэффициенты линейного уравнения и определите концентрацию никеля в воде.
Для ответа на вопросы воспользуйтесь ПК.
3.Рентгено-флуоресцентный анализ. (РФСА).
3.1. Теоретические основы РФСА.
3.2. Рентгеновская трубка – разборная и неразборная. Конструкция, принцип действия, применение
3.3. Качественный РФСА. Основы метода. Закон Мозли. Выбор условий для надежного обнаружения элементов: источник возбуждения, напряжение на трубке, аналитические линии. Рассмотрите на примере обнаружения Mn, Co, V, Fe. (Спектрометр «Спектроскан»).
3.4. Количественный РФСА. Стандартные образцы.
3.5. Способы выражения зависимости аналитического сигнала от концентрации. Компьютеризация (ПО) количественного анализа.
3.6.Пользуясь таблицами, расшифруйте РФ спектр, изображенный на рисунке. Объясните все надписи.

3.7.В ИК спектре п-нитротолула имеются полосы поглощения , см-1: 2960,2870,1520,1465, 1360, 850, 750.В результате некоторой химической реакции в спектре исчезли полосы 1520, 1360, 850 и 750 и появились две полосы в диапазоне 3500 – 3300см-1, 1280 см-1. Какая химическая реакция прошла?
4. Молекулярный спектральный анализ.
4.1.Основные закономерности в колебательных спектрах молекул: число полос поглощения в спектре сложного органического соединения, интенсивность полос и их характеристичность.
4.2. Связь колебательных спектров со структурой молекул поглощающего вещества. Рассмотрите на примере ИК спектра сложного эфира:
CH3-CH2-COOС2Н5
4.3.Происхождение и основные закономерности электронных спектров молекул. Типы электронных переходов.
4.4.Хромофоры и ауксохромы. На примере соединений: фенол, метил-этил кетон, гексан, п-дихлорбензол – покажите типы электронных переходов и укажите расположение полос в спектре.
4.5.Теоретические основы анализа по спектрам КР (комбинационного рассеяния). Какие различия наблюдаются в КР и ИК спектрах тетрахлорэтилена?
4.6.Принципиальная схема КР спектрометра. Основные детали и принцип их действия.
4.7.Идентификация органических соединений. Перечислите известные Вам методы идентификации. Как по УФ и ИК спектрам отличить соединения
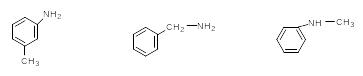
1 2 3
4.8. В УФ спектре соединения С8Н11О имеется полоса поглощения с максимумом -265 нм.
В ИК спектре этого соединения, наряду с другими, обнаружены полосы поглощения, см-1: 3300(широкая), 3050 (несколько полос), 2930(с), 2855(с), 1600, 1500, 1450, 1300 (с), 1050(широкая), 750(с), 700.ЯМР-Н спектр содержит четыре синглетных сигнала, м.д: 2.4, 4,6; 5,1(шир); 7,2. Отношение площадей 3:2:1:4.Определите структуру молекул соединения.
4.9.Для спектрофотометрического определения концентрации метилэтилкетона в водном растворе приготовили три градуировочных раствора и измерили их абсорбционность. В тех же условиях шесть раз измерили абсорбционность исследуемого раствора. Данные занесли в таблицу.
Параметр |
Градуировочные растворы |
Исследуемый раствор |
||
№ раствора |
1 |
2 |
3 |
|
Концентрация М/л |
0,05 |
0,08 |
0,1 |
|
Абсорбционность |
0,230 |
0,365 |
0,460 |
0,248; 0,250; 0,250; 0,238; 0,450; 0,240. |
Пользуясь ПК,
1. Проверьте, нет ли среди результатов анализа «выбросов»
,2. Рассчитайте коэффициент корреляции и удостоверьтесь, в том, что наблюдается линейная зависимость между концентрацией и абсорбционностью.
.3. Рассчитайте градуировочные коэффициенты линейного уравнения (y=ax+b)
.4 Определите концентрацию метилэтилкетона в водном растворе.
4.10 Сопоставьте спектр ЯМР-Н со структурой соединения (C6H5CH2CH2NHCOCH3)


4.11.Соединение имеет брутто-формулу С15Н14О. В ИК- спектре соединения обнаружена интенсивная полоса при 1710 см-1, в УФ- полоса 260 нм. Спектр ЯМР-Н дан на рисунке. Определите структуру молекул соединения.

5. ЯМР спектрометрия.
5.1.Основные закономерности в ЯМР-Н спектре: количество сигналов, химический сдвиг, мультиплетность, соотношение площадей сигналов. Рассмотрите на примере спектра н-пропанола и изопропанола.
5.2. Информативность спектров ЯМР-Н.
