
- •Основные положения теории химического
- •Углеводороды. Классификация.
- •3.Реакции полимеризации
- •1.Реакции присоединения:
- •2.Реакции окисления
- •Реакции полимеризации и сополимеризации олефинов. Натуральный и синтетический каучукипонятие о высокомолекулярных соединениях.
- •1.Реакции замещения
- •2.Реакции присоединения
- •3.Реакции окисления
- •1. Замещение атомов водорода гидроксильных групп
- •2. Замещение гидроксильных групп
- •1.Реакции с участием гидроксильной группы
- •2.Реакции с участием бензольного кольца
- •2.Реакции окисления
- •2.Образование солей:
- •Непредельные одноосновные кислоты. Понятие о двухосновных кислотах и кислотах с несколькими двойными связями.
- •Важнейшие представители: муравьиная, уксусная, капроновая, энантовая, акриловая, щавелевая, олеиновая, стеариновая, сорбиновая кислоты. Реакция поликонденсации.
- •Жиры и масла. Получение, гидролиз и гидрогенизация жиров. Саломас, маргарин.
- •Карбоновые кислоты ароматического ряда. Бензойная кислота. Фталевые кислоты. Понятие об окси-кислотах (молочная, лимонная, винная кислоты).
- •Амины. Классификация, изомерия, номенклатура, получение. Физические и химические свойства (основность, алкилирование, ацилирование, действие азотистой кислоты). Понятие о диаминах.
- •2. Взаимодействие внутри молекулы — образование внутренних солей:
- •3. Взаимодействие аминокислот друг с другом — образование пептидов.
- •3. Цветные (качественные) реакции на белки:
3.Реакции полимеризации
Полимеризацией называется процесс соединения одинаковых молекул (мономеров), протекающий за счет разрыва кратных связей, с образованием высокомолекулярного соединения (полимера).
nСН2 = СН2 → (—СН2-СН2—)n, где n — степень полимеризации (число молекул мономера)
Нахождение в природе: В природе ациклические алкены практически не встречаются. Простейший представитель этого класса органических соединений — этилен (C2H4) — является гормоном для растений и в незначительном количестве в них синтезируется.
АЛКАДИЕНЫ (диеновые УВ) — это УВ, в молекулах которых между атомами углерода имеются две двойные связи. Общая формула:CnH2n-2, n≥3
Изомерия и номенклатура:
Структурная изомерия цепи, структурная изомерия взаимного положения двойных связей, пространственная изомерия,межклассовая изомерия
Химические свойства
1. Реакции присоединения: например, присоединение галогенов:
2.Реакция полимеризации
Нахождение в природе:
АЛКИНЫ (ацетиленовые УВ) CnH2n-2, n≥2
Алкины — это углеводороды, в молекулах которых два атома углерода находятся в состоянии sp-гибридизации и связаны друг с другом тройной связью.
Изомерия н номенклатура
Существует 2 типа изомерии алкинов: изомерия положения тройной связи и изомерия цепи. Первые два члена гомологического ряда — этин и пропин — изомеров не имеют. По номенклатуре IUPAC названия алкинов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ин»; положение тройной связи указывается арабскими цифрами. Углеводородные радикалы, образованные от алкинов имеют суффикс «-инил», так CH≡C- называется «этинил».
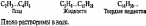 Физические
свойства
Физические
свойства
Химические свойства
Алкины во многих реакциях обладают большей реакционной способностью, чем алкены.
1.Реакции присоединения:
—Присоединение водорода (гидрирование). На I ступени образуются алкены, на II ступени — алканы
—Присоединение галогенов (галогенирование). На I ступени образуются дигалогеналкены, на II — тетрагалогеналканы.
Реакция алкинов с бромной водой — качественная реакция на алкины. Бромная вода обесцвечивается.
—Присоединение галогеноводородов (гидрогалогенирование). На I ступени образуются моногалогеналкены, на II —дигалогеналканы.
—Присоединение воды (гидратация).Происходит по правилу Марковникова. Ацетилен образует альдегид, его гомологи — кетоны (реакция М.Г.Кучерова):
2.Реакции окисления
—Горение (полное окисление)
2С2Н2 + 5О2→4СО2 + 2Н2О
—Неполное окисление (под действием окислителей типа КМnO4, К2Сг2O7)
При действии сильных окислителей (КМnO4 в нейтральной среде, К2Сг2O7 в кислой среде) алкины окисляются с разрывом молекулы по тройной связи (кроме ацетилена). Конечным продуктом реакции являются карбоновые кислоты.
Реакция с КМnO4 является качественной реакцией на алкины.Раствор КМnO4 обесцвечивается.
3.Реакции полимеризации
Алкины могут образовывать линейные димеры, тримеры и полимеры, циклические тримеры.
4.Реакции замещения атомов «Н», связанных с sp-гибридизованными атомами углерода
Атомы водорода, связанные с sp-гибридизованными атомами углерода в молекулах алкинов, обладают значительной подвижностью, что объясняется поляризацией связи ≡С—Н. В связи с этим данные атомы водорода могут замешаться атомами металлов, в результате чего образуются ацетилениды. Способность к таким реакциям отличает алкины от других непредельных углеводородов.
Нахождение в природе: В природе алкины практически не встречаются. В некоторых видах грибов Basidiomycetes были обнаружены в крайне малом количестве соединения содержащие полиацетиленовые структуры.Ацетилен обнаружен в атмосфере Урана, Юпитера и Сатурна.
