
- •Введение
- •Лекция 1 кристаллическое строение металлов
- •Металлический тип связи в кристаллах
- •1.2. Кристаллизация
- •1.3. Модифицирование сплавов
- •1.4. Форма кристаллических образований
- •1.5. Строение металлического слитка
- •1.6. Пластическая деформация и рекристаллизация
- •1.6.1 Упругая и пластическая деформация металлов
- •1.6.2 Наклеп (нагартовка) металлов.
- •1.6.3 Влияние нагрева на структуру и свойства деформированного металла
- •1.6.4 Холодная и горячая деформации
- •Вопросы для самоконтроля
- •Лекция 2. Теория сплавов
- •2.1 Виды взаимодействия компонентов в сплавах
- •2.2 Простейшие типы диаграмм состояния сплавов
- •1 Вариант (рис. 2.9).
- •2 Вариант диаграммы 3 типа
- •2.3 Связь между свойствами сплавов и типом диаграммы состояния.
- •Вопросы для самоконтроля
- •Лекция 3 железо и его сплавы.
- •3.1 Аллотропия железа.
- •3.2 Фазы в железо-углеродистых сплавах.
- •3.3 Структурные составляющие железо-углеродистых сплавов
- •3.4 Структура сталей в равновесном состоянии
- •3.5 Чугун.
- •3.5.1 Белый чугун.
- •3.5.2 Процесс графитизации
- •3.5..3 Серый чугун
- •3.5.4 Высокопрочный чугун (с шаровидным графитом)
- •3.5.5 Ковкий чугун
- •Вопросы для самоконтроля
- •Лекция 4 теория термической обработки стали
- •4.1 Превращения в стали при нагреве
- •4.2 Измельчение и рост аустенитного зерна при нагреве
- •4.3 Превращения в стали при охлаждении.
- •4.4 Перлитное превращение
- •4.5 Мартенситное превращение
- •4.6 Превращение мартенсита и остаточного аустенита при нагреве (отпуск стали)
- •4.7 Технология термической обработки стали
- •4.7.1 Отжиг
- •4.7.1.1 Отжиг I рода
- •4.7.1.2 Отжиг II-го рода (с фазовой перекристаллизацией)
- •4.7.2 Закалка
- •4.7.2.1 Выбор температуры закалки
- •4.7.2.2 Охлаждающие среды при закалке
- •4.7.2.3 Закаливаемость и прокаливаемость стали
- •4.7.2.4 Способы закалки
- •4.7.2.5 Закалка с обработкой стали холодом
- •4.7.3 Отпуск
- •4.7.4 Нормализация
- •4.8 Термомеханическая обработка (тмо)
- •Вопросы для самоконтроля
- •Лекция 5 Химико-термическая обработка
- •5.1 Цементация стали
- •5.2 Азотирование
- •5.3 Цианирование (нитроцементация)
- •5.4 Диффузионная металлизация и диффузионное насыщение другими элементами
- •5.5 Поверхностный наклеп
- •Вопросы для самоконтроля
- •Лекция 6 поверхностное упрочнение стали
- •6.1 Поверхностная закалка
- •6.2 Закалка твч
- •6.3 Закалка с газопламенным нагревом
- •Вопросы для самоконтроля
- •Содержание
2.2 Простейшие типы диаграмм состояния сплавов
Диаграмма – это графическое изображение состояния сплавов в зависимости от состава и температуры. Диаграммы строятся для условий равновесия, которые создаются при очень медленном охлаждении или нагревании сплавов, когда ни один процесс не затормаживается, все превращения идут до конца.
Диаграммы строятся экспериментально по критическим точкам. Критические точки – это температуры, при которых в сплаве происходит какое-то превращение (например, затвердевание – расплавление, аллотропическое превращение, распад твердого раствора и т.д.). Критические точки находят термическим или каким-либо другим методом. При термическом анализе для каждого сплава данной системы строят кривую охлаждения. Все превращения сопровождаются тепловым эффектом (выделение или поглощение тепла) что приводит или к температурным остановкам, или перегибам кривой охлаждения сплава из жидкого состояния (см. рис. 2.4): 1 и 2 – критические точки.

Рис. 2.4 Кривая охлаждения сплава, где компоненты дают твердый раствор (20% В, 80% А – см. рис. 2.5)
Полученные критические точки наносятся в координатах состав-температура. Соединяя однотипные точки, получаем диаграмму состояния (см. рис. 5.5).
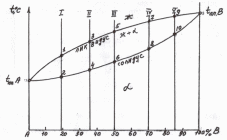
Рис.2.5 Линии диаграммы, построенные по критическим точкам (ликвидус и солидус)
Например, в сплавах 1, 2, 3, 4, 5 были найдены критические точки (рис. 2.5). Соединяя точки начала кристаллизации (1, 3, 5, 7, 9), получаем линию ликвидус. Соединяя точки конца кристаллизации, получаем линию солидус. Таким образом, зная температуры плавления чистых компонентов А и В, получаем диаграмму для случая неограниченной растворимости.
Рассмотрим 4 типа простейших диаграмм.
Диаграмма 1 типа (случай образования механической смеси с эвтектикой, рис. 2.6).
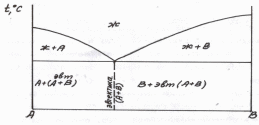
Рис. 2.6,а Диаграмма состояния 1 типа
Диаграмма состояния 2 типа (случай неограниченной растворимости компонентов в друг друге – рис. 5.9).
Неограниченная растворимость будет иметь место при следующих условиях:
1)Компоненты имеют один тип кристаллической решетки (изоморфны) с небольшим различием в параметрах.
2)Компоненты находятся близко в таблице Менделеева и имеют близкие атомные размеры.
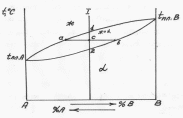
Рис. 2.7 Диаграмма состояния 2 типа
В этом случае атомы как бы взаимозаменяемы
в кристаллической решетке. Заменяя
атомы одного компонента на атомы другого
компонента в кристаллической решетке
получают непрерывный ряд твердых
растворов. Когда будут заменены все
атомы, получается чистый второй компонент.
Твердые растворы, как уже упоминалось,
обозначают
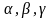 и т.д., рис. 2.7. Выше линии ликвидус –
жидкость, ниже линии солидус – твердый
раствор
.
Между линией ликвидус и солидус –
двухфазная область, состоящая из ж+
(см. концы коноды аб). Количество жидкой
фазы в сплаве 1 при температуре т.С
соответствует отрезку «сб». При снижении
температуры до т.2 отрезок «сб» обращается
в ноль, следовательно. При подходе к
линии солидус затвердевают остатки
жидкости. Кривая кристаллизации твердого
раствора не имеет ступеньки (рис. 2.8).
и т.д., рис. 2.7. Выше линии ликвидус –
жидкость, ниже линии солидус – твердый
раствор
.
Между линией ликвидус и солидус –
двухфазная область, состоящая из ж+
(см. концы коноды аб). Количество жидкой
фазы в сплаве 1 при температуре т.С
соответствует отрезку «сб». При снижении
температуры до т.2 отрезок «сб» обращается
в ноль, следовательно. При подходе к
линии солидус затвердевают остатки
жидкости. Кривая кристаллизации твердого
раствора не имеет ступеньки (рис. 2.8).
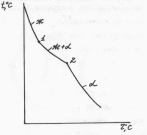
Рис. 2.8 Кривая охлаждения сплава 1 на диаграмме 2 типа.
Диаграмма состояния 3 типа (случай ограниченной растворимости компонентов).
Случаи неограниченной растворимости очень редки, чаще встречается ограниченная растворимость, будет участок диаграммы 2 типа.
Существует несколько вариантов диаграмм 3 типа.
