
- •Аминокислоты Аминокислотный состав белков
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Н езаменимые аминокислоты
- •Пищевая ценность белков
- •Биологические функции белков
- •Структурная организация белковых молекул
- •Классификация белков по растворимости
- •Физико-химические свойства белков
- •Первичная структура белков
- •Конформация пептидных цепей в белках
- •Третичная структура белков
- •Силы, стабилизирующие третичную структуру белка.
- •Четвертичная структура белка.
- •Ферменты
- •Особенности ферментов как биокатализаторов
- •Классификация ферментов по типу катализируемой реакции и номенклатура ферментов
- •Активный центр ферментов
- •Причины высокой каталитической активности.
- •Субстратная специфичность
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Влияние активаторов и ингибиторов на активность ферментов
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Единицы ферментативной активности ферментов
- •Регуляция ферментативной активности
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •Углеводы Общая характеристика и классификация.
- •Моносахариды
- •Цикло-оксо-таутомерия
- •Химические свойства
- •Дисахариды
- •Полисахариды
- •Классификация и основные структурные компоненты омыляемых липидов.
- •Высшие жирные кислоты – это карбоновые кислоты, насыщенные или ненасыщенные, выделенные из жиров путем гидролиза. Для их строения характерны следующие основные особенности:
- •Нейтральные липиды
- •Триацилглицериды
- •Неомыляемые липиды
- •Витамины
- •Водорастворимые витамины Тиамин (витамин в1)
- •Рибофлавин (витамин в2)
- •Ниацин (никотинамид, никотиновая кислота, витамин рр)
- •Пантотеновая кислота
- •Пиридоксин (пиридоксаль, пиридоксамин, витамин в6)
- •Биотин (витамин н)
- •Фолиевая кислота
- •Витамин в12
- •Аскорбиновая кислота (витамин с)
- •Жирорастворимые витамины Витамин а
- •Биохимические функции витамина а Регуляция экспрессии генов
- •Витамин а и акт зрения
- •Гипервитаминоз и гиповитаминоз
- •Витамин д (кальциферол)
- •Витамин е (токоферолы)
- •Витамин к (нафтохиноны)
- •Биоэнергетика. Основные понятия и определения Особенности живых организмов как объектов для термодинамических исследований
- •Сопряжение экзергонических процессов с эндергоническими
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Клеточное дыхание
- •Биосинтез вжк в тканях
- •Гниение аминокислот, обезвреживание продуктов гниения
- •Метаболизм аминокислот
- •Пути обезвреживания аммиака
- •Глюконеогенез
Биосинтез вжк в тканях
Биосинтез ВЖК происходит в эндоплазматической сети клеток. Заменимые ВЖК (все предельные и непредельные, имеющих одну двойную связь) синтезируются в клетках из АЦЁТИЛ-КоА. Условиями для биосинтеза ВЖК являются:
1.Наличие АЦЕТИЛ-КоА, АТФ, СО2, Н2О, НАДФ*Н2,
2.Наличие специальных белков-переносчиков (HS -АПБ). 3.Наличие ферментов синтеза.
Процесс биосинтеза циклический. Каждый цикл включает в себя 6 этапов:
1этап- образование 3-углеродного соединения - МАЛОНИЛ-КОА;2 этап- перенос МАЛОНИЛА и АЦЕТИЛА на специальные белки ( HS-АПБ);3. этап- конденсация МАЛОНИЛА-АПБ и АЦЕТИЛА-АПБ с участием СИНТАЗЫ;4. этап- восстановление бета -КЕТОАЦИЛ-АПБ;5.этап- дегидратация бета-ГИДРОКСИАЦИЛ-АПБ;6.этап- восстановление ЕНОИЛАЦИЛ-АПБ.
 Т.о.
завершается 1 цикл синтеза ВЖК образованием
масляной кислоты (БУТИРИЛ-АПБ). В
дальнейшем последовательно и циклично
к ней будут присоединяться молекулы
МАЛОНИЛ-КоА. Завершается биосинтез
любой ВЖК в тканях ДЕАЦИЛАЗНОЙ реакцией.
Т.о.
завершается 1 цикл синтеза ВЖК образованием
масляной кислоты (БУТИРИЛ-АПБ). В
дальнейшем последовательно и циклично
к ней будут присоединяться молекулы
МАЛОНИЛ-КоА. Завершается биосинтез
любой ВЖК в тканях ДЕАЦИЛАЗНОЙ реакцией.
Гниение аминокислот, обезвреживание продуктов гниения
ГНИЕНИЕ АМИНОКИСЛОТ
Аминокислоты, которые не подверглись всасыванию, поступают в толстую кишку, где подвергаются гниению. ГНИЕНИЕ АМИНОКИСЛОТ - это процесс распада аминокислот под действием ферментов, вырабатывающихся микрофлорой толстого отдела кишечника. Аминокислоты при гниении подвергаются следующим превращениям:
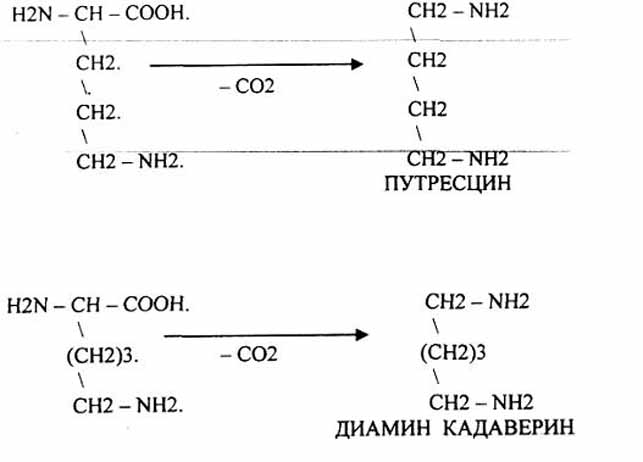
РЕАКЦИИ ДЕКАРБОКСИЛИРОВАНИЯ:
Подвергаются
орнитин и лизин. ОРНИТИН в состав белков
не входит, но обязательно содержится
в организме. Проукты декарбоксилирования
- ПУТРЕСЦИН и КАДАВЕРИН - являются
токсическими веществами. Они входят в
состав трупных ядов.
 ВОССТАНОВИТЕЛЬНОЕ
ДЕЗАМИНИРОВАНИЕ: (на примере аланина)
ВОССТАНОВИТЕЛЬНОЕ
ДЕЗАМИНИРОВАНИЕ: (на примере аланина)
![]() ДЕСУЛЬФИРОВАНИЕ
ДЕСУЛЬФИРОВАНИЕ
Десульфированию подвергаются серосодержащие аминокислоты (метионин, цистеин). В результате образуются сероводород, метилмеркаптан.
РАСПАД ЦИКЛИЧЕСКИХ АМИНОКИСЛОТ
При распаде тирозина, фенилаланина, триптофана образуются метан, углекислый газ, аммиак, фенол, крезол, индол.
Все эти вещества токсические. Они поступают в печень, где и происходит их обезвреживание. В печени имеется две системы, участвующие в обезвреживании этих веществ:
1.УДФГК - УРИДИНДИФОСФОГЛЮКУРОНОВАЯ К-ТА.
2.ФАФС-ФОСФОАДЕНОЗИНФОСФОСУЛЬФАТ.
Процесс обезвреживания - это процесс конъюгации токсических веществ с компонентами одной из этих систем, и образования конъюгатов, которые являются уже нетоксичными веществами.
ИНДОКСИЛСУЛЬФАТ нейтрализуется и превращается в натриевую или калиевую соль.
Все эти вещества выводятся из организма с мочой.
В норме реакция на индол должна быть отрицательна. При положительной реакции на индол - нарушена обезвреживающая функция печени. Положительная реакция на ИНДИКАН наблюдается при очень активном гниении белков в толстом кишечнике.
Метаболизм аминокислот
Метаболизм аминокислот
Источниками аминокислот в клетке являются:
1.белки пищи после их гидролиза в органах пищеварения;
2.синтез заменимых аминокислот;
3.распад тканевых белков.
Тканевые белки подвергаются гидролитическому расщеплению при участии тканевых ПРОТЕАЗ - КАТЕПСИНОВ, которые в основном находятся в ЛИЗОСОМАХ. Выделяют разные КАТЕПСИНЫ, которые отличаются оптимумом рН и специфичностью действия. Распад тканевых белков необходим для обновления белков, а также для устранения дефектных молекул белка.
Несмотря на то, что почти для каждой аминокислоты выяснены индивидуальные пути обмена, известен ряд превращений, общих для многих аминокислот:
ТРАНСАМИНИРОВАНИЕ; ДЕКАРБОКСИЛИРОВАНИЕ; ДЕЗАМИНИРОВАНИЕ.
ТРАНСАМИНИРОВАНИЕ – реакции межмолекулярного переноса аминогруппы от аминокислоты на кетокислоту без промежуточного образования аммиака.
Особенности реакций трансаминирования:
протекают при участии ферментов - аминотрансфераз;
для реакций необходим кофермент – пиридоксальфосфат (ПФ);
реакции обратимы;
могут подвергаться все аминокислоты кроме лиз, тре;
в результате реакции образуются новая аминокислота и новая кетокислота.
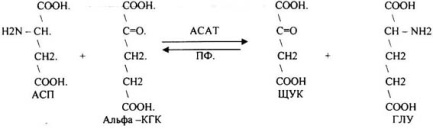 Роль реакций
ТРАНСАМИНИРОВАНИЯ:
Роль реакций
ТРАНСАМИНИРОВАНИЯ:
1.Синтез заменимых аминокислот. При этом происходит перераспределение азота в органах и тканях;
2.Являются начальным этапом катаболизма аминокислот.
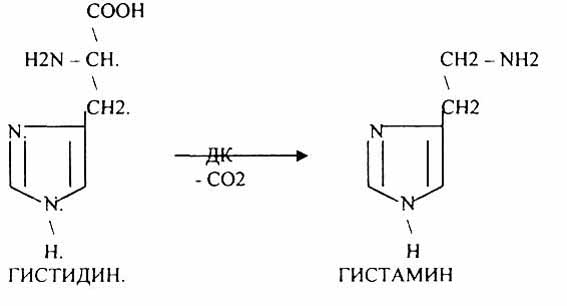
Реакции ДЕКАРБОКСИЛИРОВАНИЯ – отщепление альфа – карбоксильной группы аминокислот в виде углекислого газа.
При этом аминокислоты в тканях образуют биогенные амины, которые являются биологически активными веществами (БАВ). Среди них могут быть соединения, которые выполняют функции:
1.НЕЙРОМЕДИАТОРОВ (СЕРОТОНИН, ДОФАМИН, ГАМК),
2. Гормоны (АДРЕНАЛИН, НОРАДРЕНАЛИН),
3. Регуляторы местного действия (ГИСТАМИН).
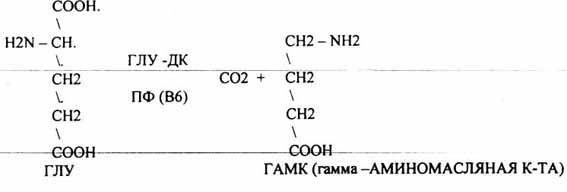 ГАМК является
НЕЙРОМЕДИАТОРОМ тормозного действия,
поэтому препараты на основе ГАМК
используются в клинике для лечения
некоторых заболеваний ЦНС. Эта реакция
используется в педиатрической практике:
детям при сильном возбуждении используют
раствор витамина В6, который стимулирует
процесс образования ГАМК.
ГАМК является
НЕЙРОМЕДИАТОРОМ тормозного действия,
поэтому препараты на основе ГАМК
используются в клинике для лечения
некоторых заболеваний ЦНС. Эта реакция
используется в педиатрической практике:
детям при сильном возбуждении используют
раствор витамина В6, который стимулирует
процесс образования ГАМК.
ДОФАМИН является НЕЙРОМЕДИАТОРОМ возбуждающего действия. Он является основой для синтеза АДРЕНАЛИНА и НОРАДРЕНАЛИНА.
 Реакции
ДЕЗАМИНИРОВАНИЯ - отщепление NН2-группы
в виде аммиака. ОКИСЛИТЕЛЬНОЕ
ДЕЗАМИНИРОВАНИЕ.
Непосредственно,
ОКИСЛИТЕЛЬНОМУ ДЕЗАМИНИРОВАНИЮ
подвергается только ГЛУ.
Реакции
ДЕЗАМИНИРОВАНИЯ - отщепление NН2-группы
в виде аммиака. ОКИСЛИТЕЛЬНОЕ
ДЕЗАМИНИРОВАНИЕ.
Непосредственно,
ОКИСЛИТЕЛЬНОМУ ДЕЗАМИНИРОВАНИЮ
подвергается только ГЛУ.
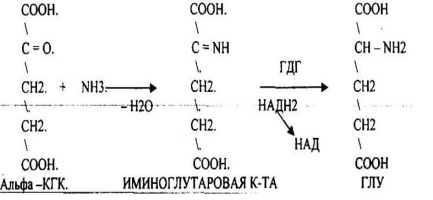 НЕПРЯМОЕ
ДЕЗАМИНИРОВАНИЕ
НЕПРЯМОЕ
ДЕЗАМИНИРОВАНИЕ
Этому виду дезаминирования подвергаются остальные аминокислоты, но через стадию трансаминирования с альфа-кетоглутаровой кислотой. Затем глутаминовая кислота (продукт этой реакции) подвергается окислительному дезаминированию.
