
- •Аминокислоты Аминокислотный состав белков
- •Строение и классификация аминокислот
- •Стереоизомерия.
- •Н езаменимые аминокислоты
- •Пищевая ценность белков
- •Биологические функции белков
- •Структурная организация белковых молекул
- •Классификация белков по растворимости
- •Физико-химические свойства белков
- •Первичная структура белков
- •Конформация пептидных цепей в белках
- •Третичная структура белков
- •Силы, стабилизирующие третичную структуру белка.
- •Четвертичная структура белка.
- •Ферменты
- •Особенности ферментов как биокатализаторов
- •Классификация ферментов по типу катализируемой реакции и номенклатура ферментов
- •Активный центр ферментов
- •Причины высокой каталитической активности.
- •Субстратная специфичность
- •Зависимость скорости ферментативной реакции от температуры
- •Зависимость скорости ферментативной реакции от рН
- •Влияние активаторов и ингибиторов на активность ферментов
- •Обратимое конкурентное ингибирование аналогами субстрата
- •Обратимое неконкурентное ингибирование
- •Необратимое ингибирование
- •Единицы ферментативной активности ферментов
- •Регуляция ферментативной активности
- •Регуляция количества фермента путем регуляции скорости его синтеза и распада
- •Превращение ферментов в активные формы
- •Регуляция активности ферментов путем их ковалентной модификации
- •Аллостерическая регуляция
- •Ингибирование по принципу обратной связи
- •Углеводы Общая характеристика и классификация.
- •Моносахариды
- •Цикло-оксо-таутомерия
- •Химические свойства
- •Дисахариды
- •Полисахариды
- •Классификация и основные структурные компоненты омыляемых липидов.
- •Высшие жирные кислоты – это карбоновые кислоты, насыщенные или ненасыщенные, выделенные из жиров путем гидролиза. Для их строения характерны следующие основные особенности:
- •Нейтральные липиды
- •Триацилглицериды
- •Неомыляемые липиды
- •Витамины
- •Водорастворимые витамины Тиамин (витамин в1)
- •Рибофлавин (витамин в2)
- •Ниацин (никотинамид, никотиновая кислота, витамин рр)
- •Пантотеновая кислота
- •Пиридоксин (пиридоксаль, пиридоксамин, витамин в6)
- •Биотин (витамин н)
- •Фолиевая кислота
- •Витамин в12
- •Аскорбиновая кислота (витамин с)
- •Жирорастворимые витамины Витамин а
- •Биохимические функции витамина а Регуляция экспрессии генов
- •Витамин а и акт зрения
- •Гипервитаминоз и гиповитаминоз
- •Витамин д (кальциферол)
- •Витамин е (токоферолы)
- •Витамин к (нафтохиноны)
- •Биоэнергетика. Основные понятия и определения Особенности живых организмов как объектов для термодинамических исследований
- •Сопряжение экзергонических процессов с эндергоническими
- •Макроэргические соединения
- •Фазы освобождения энергии из питательных веществ
- •Роль высокоэнергетических фосфатов в улавливании энергии. Клеточное дыхание
- •Биосинтез вжк в тканях
- •Гниение аминокислот, обезвреживание продуктов гниения
- •Метаболизм аминокислот
- •Пути обезвреживания аммиака
- •Глюконеогенез
Макроэргические соединения
Энергия, освобождающаяся при реакциях гидролиза разных веществ, обычно невелика. Если она превышает 30 кДж/моль, то такую связь называют высокоэнергетической. Макроэргические соединения можно разделить на две группы:1)Соединения, образующиеся в ходе процессов катаболизма и служащие для превращения энергии в качестве передаточного звена (1,3-дифосфоглицерат, фосфоенолпируват - промежуточные метаболиты катаболизма углеводов). 2) Соединения, которые могут быть использованы тканями в качестве "аварийного" источника энергии (креатинфосфат локализован в основном в мышцах и служит дополнительным источником энергии при стремительных кратковременных нагрузках).
Фазы освобождения энергии из питательных веществ
Характер
метаболизма в тканях во многом
определяется питанием. У человека
метаболическим превращениям подвергаются,
главным образом, глюкоза, жиры и
аминокислоты. Глюкоза и аминокислоты
- структурные компоненты белков и
углеводов. Таким образом, необходимыми
компонентами пищи являются белки
углеводы и жиры.В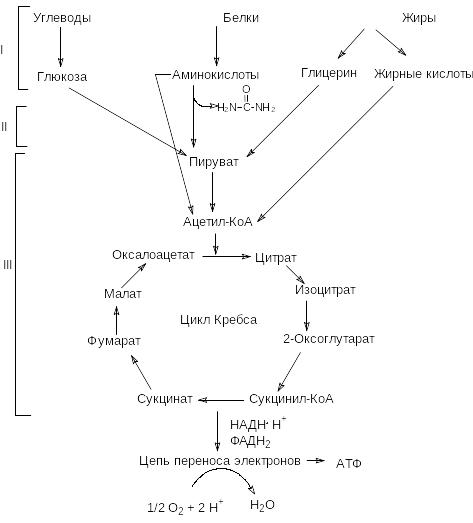 ходе извлечения энергии из различных
субстратов можно условно выделить три
фазы катаболизма питательных веществ.
ходе извлечения энергии из различных
субстратов можно условно выделить три
фазы катаболизма питательных веществ.
Первая фаза - подготовительная. Она необходима для превращения полимеров, поступающих с пищей или находящихся внутри клетки, в удобную для извлечения энергии форму - мономеры. На этом этапе освобождается около 1% всей энергии, запасенной в питательных веществах. Эта энергия рассеивается в форме теплоты.
Вторая фаза - частичный распад мономеров до ключевых промежуточных продуктов: пирувата, ацетил-КоА и некоторых метаболитов цикла Кребса. На этом этапе освобождается около 20% энергии. Эта стадия называется промежуточный обмен. Реакции промежуточного обмена протекают в цитоплазме.
Третья фаза - окончательный распад всех веществ до CO2 и H2O. Этот этап включает реакции общего пути катаболизма (окислительное декарбоксилирование пирувата, цикл Кребса) и цепь переноса электронов. Примерно 80% всей энергии химических связей освобождается в данной фазе. Все реакции этой фазы локализуются в митохондриях.
Роль высокоэнергетических фосфатов в улавливании энергии. Клеточное дыхание
Главный путь синтеза АТФ из АДФ - окислительное фосфорилирование. При этом АДФ фосфорилируется неорганическим фосфатом:
АДФ + H3PO4 + энергия АТФ + H2O
Реакция энергетически сопряжена с переносом водорода с восстановительных эквивалентов на кислород. Восстановительные эквиваленты образуются при окислении органических молекул. Последовательность реакций, с помощью которых организм использует энергию связей органических молекул для синтеза АТФ, и при этом углерод органических молекул превращается в углекислый газ, а водород (Н+ и е-) переносится на молекулярный кислород с образованием молекулы воды, называется клеточным дыханием.
Другой путь синтеза АТФ из АДФ - субстратное фосфорилирование. В этом случае макроэргическая связь в молекуле АТФ может образоваться за счет энергии макроэргической связи в другом субстрате (например, креатинфосфате).
Таким образом, энергия пищевых веществ в клетке трансформируется сначала в энергию АТФ, а затем АТФ служит непосредственным источником энергии для совершения работы в биохимических и физиологических процессах.
Нуклеиновые кислоты. Нуклеиновые кислоты – это высокомолекулярные соединения, состоящие из мононуклеотидов, т.е. их структурной единицей является мононуклеотид (нуклеотид). Каждый нуклеотид включает 3 химически различных компонента: моносахарид, азотистое основание, остаток фосфорной кислоты. Нуклеотиды, входящие в РНК и ДНК, отличаются друг от друга по составу. Соединение основания и пентозы называют нуклеозидом, связь между пентозой и азотистым основанием (b - гликозидная) образована - первым атомом углерода пентозы с первым атомом азота в пиримидиновых нуклеозидах и девятым атомом азота в пуриновых нуклеозидах. Нуклеотиды представляют собой соединения нуклеозидов с фосфорной кислотой (связь сложно – эфирная). В составе РНК и ДНК по 4 нуклеозидмонофосфата (нуклеотида).
Номенклатура наиболее распространенных нуклеотидов.
РИБОНУКЛЕОЗИДМОНОФОСФАТЫ:
1. Аденозинмонофосфат ( АМФ ), адениловая кислота.
2.Гуанозинмонофосфат ( ГМФ ), гуаниловая кислота.
3.Цитидинмонофосфат ( ЦМФ ), цитидиловая кислота.
4.Уридинмонофосфат (УМФ), уридиловая кислота
ДЕЗОКСИРИБОНУКЛЕОЗИДМОНОФОСФАТЫ:
1. д.Аденозинмонофосфат ( д.АМФ ).
2.д.Гуанозинмонофосфат ( д.ГМФ ).
3 д.Цитидинмонофосфат ( д.ЦМФ ).
4.Тимидинмонофосфат ( д.ТМФ ).
Структура нуклеиновых кислот.
Первичные структуры РНК и ДНК построены однотипно, они представляют собой линейные полимеры – полинуклеотиды, состоящие из мононуклеотидов, соединенных 3',5' – фосфодиэфирными связями. При этом сложноэфирная связь образована фосфатным остатком одного мононуклеотида и 3' – гидроксильной группой пентозного остатка другого мононуклеотида (3',5' – фосфодиэфирная связь). Концы полинуклеотидов различаются по структуре: на одном конце имеется свободная 5' – фосфатная группа (5' – конец), на другом – свободная 3' – ОН - группа (3' – конец). Уникальность структуры и функциональная индивидуальность молекул ДНК и РНК определяется их первичной структурой.
Вторичная структура ДНК.
Особенностью нуклеотидного состава ДНК является то, что число адениловых нуклеотидов равно числу цитидиловых: А=Т, Г=Ц, следовательно, А+Г=Т+Ц, т.е. число пуриновых нуклеотидов равно числу пиримидиновых (правила Чаргаффа). Такие соотношения не свойственны РНК. Исходя из правил Чаргоффа о нуклеотидном составе ДНК и из рентгеноструктурных исследований, Дж. Уотсон и Ф. Крик (Великобритания) предложили модель строения ДНК (1953) Согласно этой модели молекула ДНК представляет собой двойную спираль, образованную двумя полинуклеотидными цепями, закрученными относительно друг друга и вокруг общей оси. Двойная спираль правозакрученная, полинуклеотидные цепи в ней антипараллельны, т.е. если одна из них ориентирована в направлении 3' a 5' , то вторая – в направлении 5' a 3'. Поэтому на каждом из концов молекулы ДНК расположены 5' – конец одной цепи и 3' – конец другой цепи. Все основания цепей ДНК (гидрофобные по свойствам) расположены внутри двойной спирали, а пентозы и остатки фосфорной кислоты – снаружи. Полинуклеотидные цепи удерживаются относительно друг друга за счет водородных связей, образующихся за счет специфического взаимодействия между парами комплементарных оснований. Комплементарными являются А и Т, они образуют две водородные связи, а также Г и Ц образуют три водородные связи. Кроме водородных связей в стабилизации вторичной структуры ДНК участвуют гидрофобные взаимодействия возникающие за счет гидрофобных азотистых оснований, обращенных внутрь спирали. Гидрофобные взаимодействия вносят основной вклад в стабилизацию двойной спирали, больший чем водородные связи между цепями. Рибозофосфатные связи располагаются по периферии, образуя ковалентный остов спирали
Особенности структуры РНК.
Первичная структура РНК аналогична первичной структуре ДНК и представляет полинуклеотидную цепь, состоящую из мононуклеотидов, соединенных 3' a 5' – фосфодиэфирными связями.
Вторичная структура РНК.Молекулы РНК построены из одной полинуклеотидной цепи. Отдельные участки цепи РНК образуют спирализованные петли "шпильки", за счет водородных связей между комплементарными азотистыми основаниями А-У и Г-Ц. Участки цепи РНК в таких спирализованных участках антипараллельны, но не всегда полностью комплементарны. Наличие спирализованных участков характерно для всех типов РНК. Такие спирализованные участки содержат небольшое число нуклеотидных пар (до 20-30) и чередуются с неспирализованными участками.
Основные типы РНК.
По особенностям структуры и функциям различают 3 типа рибонуклеиновых кислот – транспортные РНК (тРНК), матричные РНК (мРНК) и рибосомальные РНК (рРНК). Они различаются по первичной структуре, молекулярной массе, конформации, продолжительности жизни и по функциональной активности.
1.Транспортные РНК (тРНК)Пространственную структуру тРНК, независимо от различий в последовательности нуклеотидов, описывают универсальной моделью "клеверного листа". В каждой молекуле тРНК есть участки цепи, не участвующие в образовании водородных связей между нуклеотидными остатками. К ним в частности, относят участок, ответственный за связывание с аминокислотой на 3'-конце молекулы и антикодон – специфический триплет нуклеотидов, взаимодействующий комплементарно с кодоном мРНК. Транспортные РНК составляют около 15% всей РНК клетки, они участвуют в транспорте аминокислот.
Строение транспортных РНК.
1. Рибосомные РНК (рРНК) – компоненты рибосом. На долю рРНК приходится около 80% всей РНК клетки.
2. Матричные РНК (мРНК) составляют около 2% от всей РНК клетки. Матричные РНК называются также информационными РНК (иРНК).
Третичная структура нуклеиновых кислот.
Одноцепочные РНК характеризуются компактной и упорядоченной третичной структурой, возникающей путем взаимодействия спирализованных участков вторичной структуры. Третичная структура РНК стабилизируется ионами двухвалентных металлов, например ионами Mg2+. Исследование некоторых ДНК вирусов митохондрий, хлоропластов при помощи физических, физико-химических методов показало, что двойная спираль ДНК на некоторых участках может подвергаться дальнейшей спирализации с образованием суперспирали или открытой кольцевой формы.
Суперспиральная структура (суперскрученная) обеспечивает экономную упаковку огромной молекулы ДНК в хромосоме вместо 8 см длины, которую она могла бы иметь в вытянутой форме, в хромосоме человека молекула ДНК настолько плотно упакована, что ее длина укладывается в 5 нм.
Имеющиеся данные о структуре тРНК свидетельствуют о том, что нативные молекулы тРНК имеют примерно одинаковую третичную структуру, которая отличается от плоской структуры «клеверного листа» большей компактностью, образованной за счет складывания различных частей молекулы.
ФОСФОПРОТЕИНЫ.
Фосфопротеины – это сложные белки, содержащие в своем составе в качестве простетической части фосфорную кислоту. Фосфорная кислота связана сложно – эфирной связью с белковой частью молекулы через гидроксильные группы оксиаминокислот (серин, треонин). Установлено, что фосфопротеины в клетках синтезируются в результате фосфорилирования при участии протеинкиназ. К фосфопротеинам относится казеиноген молока, который представляет собой белок с сильно выраженными гидрофильными свойствами. Казеиноген в молоке находится в виде кальциевой соли. Поэтому организм получает с молоком необходимые аминокислоты, кальций, лабильно связанный фосфор, находящиеся в казеиногене.
ОБМЕН УГЛЕВОДОВ
Углеводы - это полиоксикарбонильные соединения и их производные.
Основными углеводами организма человека являются:
1.Моносахариды (глицеральдегид, диоксиацетон,эритроза, рибоза, дезоксирибоза, рибулоза, ксилулоза,глюкоза, галактоза, фруктоза, манноза, арабиноза и др.);
2.Олигосахариды (мальтоза, лактоза, сахароза);
3.Гомополисахариды (крахмал, гликоген, клетчатка);
4.Гетерополисариды (гиалуроновая кислота, хондроитинсульфат, дерматансульфат, кератансульфат, гепарин).
Окисление высших жирных кислот
Жировая ткань, состоящая из адипозоцитов, выполняет специфическую роль в липидном обмене. Около 65% массы жировой ткани приходится на долю отложенных в ней триацилглицеролов (ТАГ) - они представляют собой форму запасания энергии и выполняют в обмене жиров такую же функцию, как гликоген печени в обмене углеводов. Отложенные жиры в жировой ткани служит источником эндогенной воды и энергетическим резервом для организма человека. ТАГ используется в организме после предварительного расщепления (липолиза), в ходе которого освобождаются глицерин и свободные жирные кислоты. В клетках жировой ткани при участии липаз происходит распад ТАГ. Липаза находится в неактивной форме, она активируется гормонами (адреналином, норадреналином, глюкагоном, тироксином, глюкокортикоидами, СТГ, АКТГ) в ответ на стресс, голодание, охлаждение продуктами реакции являются моноацилглицерин и ВЖК. ВЖК с помощью альбуминов переносятся кровью к клеткам тканей, органов, где происходит их окисление.
Окисление высших жирных кислот.
Источники ВЖК:
- липиды жировой ткани
- липопротеины
-триацилглицерины
-фосфолипиды клеточных биомембран
Окисление ВЖК происходят в митохондриях клеток, и называется бетта окислением. Доставка их к тканям и органам происходит при участии альбумина, а транспорт из цитоплазмы в митохондрии при участии карнитина. Процесс бета-окисления ВЖК складывается из следующих этапов:
-активация ВЖК на наружной поверхности мембраны митохондрий при участии АТФ, конзима А и ионов магния с образованием активной формы ВЖК (ацил - КоА).
-транспорт жирных кислот внутрь митохондрий возможен при присоединении активной формы жирной кислоты к карантину, находящемуся на наружной поверхности внутренней мембраны митохондрий. Образуется ацил-карнитин, обладающий способностью проходить через мембрану. На внутренней поверхности комплекс распадается и карнитин возвращается на наружную поверхность мембраны.
-внутримитохондриальное
окисление жирных кислот состоит из
последовательных ферментативных
реакций. В результате одного завершенного
цикла окисления происходит отщепление
от жирой кислоты одной молекулы
ацетил-КоА, т.е. укорочение жирнокислотной
цепи на два углеродных атома.Приэтом
в результате двух дегидрогеназных
реакций восстанавливается ФАД до ФАДН2
и НАД+
до НАДН2.
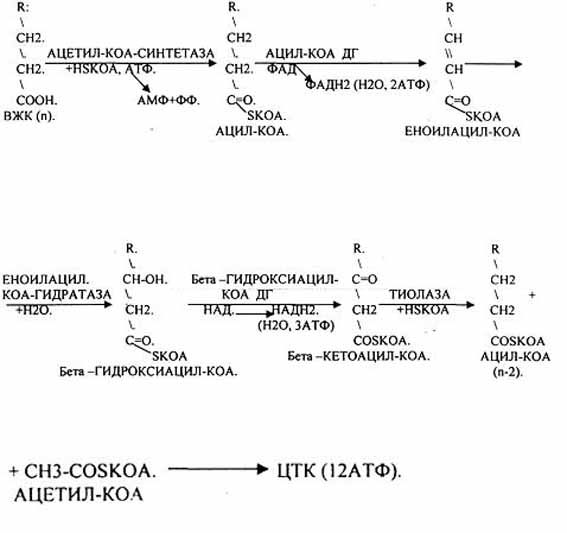 Т.о. завершая 1 цикл бега - окисления
ВЖК, в результате которого ВЖК укоротилось
на 2 углеродных звена. При бета -окислении
выделилось 5АТФ и 12АТФ выделилось при
окислении АЦЕТИЛ-КОА в ЦТК и сопряженных
с ним ферментов дыхательной цепи.
Окисление ВЖК будет происходить
циклически одинаково, но только до
последней стадии - стадии превращения
масляной кислоты (БУТИРИЛ-КОА), которая
имеет свои особенности, которые
необходимо учитывать при подсчёте
суммарного энергетического эффекта
окисления ВЖК, когда в результате одного
цикла образуется 2 молекулы АЦЕТИЛ-КОА,
одна из них проходила бета -окисление
с выделением 5АТФ, а другая нет.
Т.о. завершая 1 цикл бега - окисления
ВЖК, в результате которого ВЖК укоротилось
на 2 углеродных звена. При бета -окислении
выделилось 5АТФ и 12АТФ выделилось при
окислении АЦЕТИЛ-КОА в ЦТК и сопряженных
с ним ферментов дыхательной цепи.
Окисление ВЖК будет происходить
циклически одинаково, но только до
последней стадии - стадии превращения
масляной кислоты (БУТИРИЛ-КОА), которая
имеет свои особенности, которые
необходимо учитывать при подсчёте
суммарного энергетического эффекта
окисления ВЖК, когда в результате одного
цикла образуется 2 молекулы АЦЕТИЛ-КОА,
одна из них проходила бета -окисление
с выделением 5АТФ, а другая нет.
ОКИСЛЕНИЕ ВЖК, ИМЕЮЩИХ НЕЧЕТНОЕ КОЛИЧЕСТВО УГЛЕРОДНЫХ ЗВЕНЬЕВ В ЦЕПИ
Такие ВЖК поступают в организм человека в составе пищи с мясом жвачных животных, растений, морских организмов. Окисление таких ВЖК происходит также как и ВЖК, имеющих чётное количество углеродных звеньев в цепи, но только до последней стадии - стадии превращения ПРОПИОНИЛ-КОА. которая имеет свои особенности.
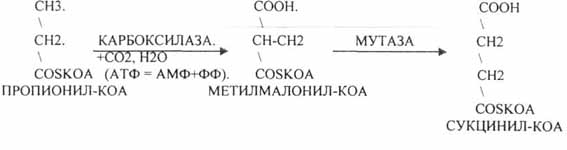 Т.о.
образуется СУКЦИНИЛ-КОА, который в
дальнейшем окисляется в МИТОХОНДРИЯХ
с участием ферментов ЦТК КРЕБСА и
сопряженных с ним ферментов дыхательной
цепи.
Т.о.
образуется СУКЦИНИЛ-КОА, который в
дальнейшем окисляется в МИТОХОНДРИЯХ
с участием ферментов ЦТК КРЕБСА и
сопряженных с ним ферментов дыхательной
цепи.
Окисление глицерина
Окисление глицерина в тканях тесно связано с ГЛИКОЛИЗОМ, в который вовлекаются метаболиты обмена глицерина по следующей схеме:
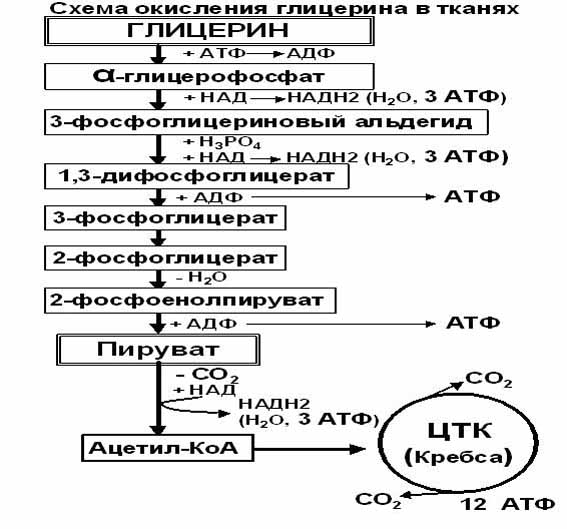 При окислении
глицерина образовались конечные
продукты:
При окислении
глицерина образовались конечные
продукты:
СО2 на этапе превращения:
1. ПИРУВАТА
2.ИЗОЦИТРАТА
3.Альфа-КЕТОГЛУТАРАТА
Н2О на этапе превращения:
1 .альфа -ГЛИЦЕРОФОСФАТА
2. ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТА
3. 2-ФОСФОГЛИЦЕРАТА
4.ПИРУВАТА
5.ИЗОЦИТРАТА
6.Альфа-КЕТОГЛУТАРАТА
7. СУКЦИНАТА
8. МАЛАТА
АТФ выделилось за счёт реакций
А) Субстратного фосфорилиования на этапах превращения:
1. 1,3-дифосфоглицерата
2.2-фосфоенолпирувата
3.Сукцинил-КоА
Б) Окислительного фосфорилирования на этапах превращения:
1.Альфа-глицерафосфата
2.Глицеральдегид-3 фосфата
3.Пирувата
4.Изоцитрата
5. Альфа-КЕТОГЛУТАРАТА
6.Сукцината
7.Малата
Суммарный энергетический эффект окисления одной молекулы глицерина равен 22 АТФ.
