
- •15 Динамика механика
- •Глава 1. Кинематика
- •1.1. Закон движения материальной точки
- •1.2. Скорость определяет быстроту движения.
- •Чтобы определить скорость изменения функции, надо взять производную этой функции по времени.
- •1.3. Ускорение
- •1.4. Кинематика вращательного движения
- •Глава 2. Динамика
- •2.1.Первый закон Ньютона (закон инерции)
- •2.2. Второй закон Ньютона
- •Изменение импульса (количества движения) за время равно импульсу силы за это же время.
- •2.3. Третий закон Ньютона
- •2.4. Сохраняющиеся величины
- •2.5. Основной закон динамики для системы материальных точек. Закон сохранения импульса.
- •Скорость изменения импульса системы материальных точек равна векторной сумме внешних сил.
- •2.6. Центр инерции
- •Глава 3. Работа и энергия
- •3.1.Работа силы и ее выражение через криволинейный интеграл
- •3.2.Мощность
- •3.3. Кинетическая энергия
- •3.4. Потенциальная энергия
- •3.5. Потенциальные кривые
- •3.6.Закон сохранения механической энергии
- •3.7. Соударения
- •Глава 4. Механика вращательного движения
- •4.1. Кинетическая энергия вращательного движения. Момент инерции.
- •4.3. Второй закон Ньютона вращательного движения.
- •4.4. Момент импульса. Закон сохранения момента импульса.
- •4.5. Таблица соответствия поступательного и вращательного движений
- •Работа и энергия
- •Глава 5 механические колебания и волны
- •5.1.Основные понятия
- •5.2.Дифференциальное уравнение свободных гармонических колебаний
- •5.3. Примеры свободных гармонических колебаний
- •5.4. Затухающие колебания.
- •5.5. Вынужденные колебания
- •5.6. Автоколебания.
- •5.7.Сложение колебаний.
- •Глава 6. Механические (упругие ) волны. Звук
- •6.1. Характеристики упругих волн
- •6.2. Уравнение бегущей волны
- •Основы молекулярной физики и термодинамики
- •Глава 7. Основы молекулярно–кинетической теории
- •7.1. Основные понятия и определения
- •7.2. Уравнение состояния идеального газа
- •7.3. Основное уравнение молекулярно–кинетической теории идеального газа (основное уравнение мкт)
- •Абсолютная температура является мерой средней кинетической энергии поступательного движения молекулы.
- •7.4. Закон распределения молекул по скоростям
- •7.5. Барометрическая формула #
- •Глава 8 основы термодинамики
- •8.1. Первый закон термодинамики
- •6.2. Простейшие процессы в идеальных газах
- •8.3. Второй закон термодинамики
- •8.4. Цикл Карно
- •Глава 9 реальные газы
- •9.1. Уравнение состояния реальных газов (уравнение Ван–дер–Ваальса).
- •9.2.Изотермы реальных газов
7.4. Закон распределения молекул по скоростям
Распределение молекул по скоростям (Максвелл). В § 7.3. мы ввели понятие средней квадратичной скорости молекул как средней характеристики всех молекул газа, справедливо считая, что скорости конкретных молекул отличаются друг от друга даже в состоянии термодинамического равновесия.
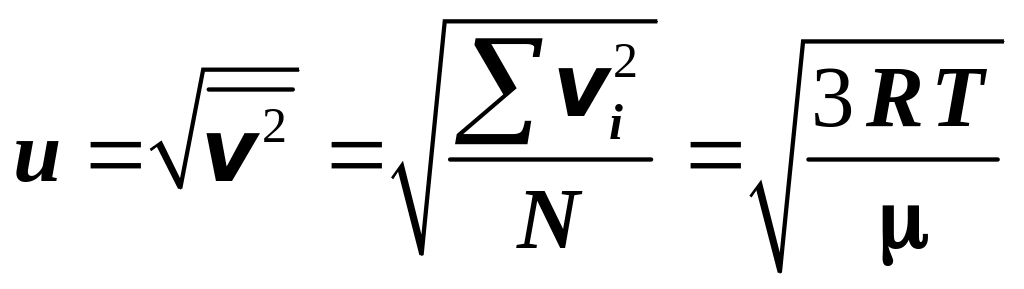
Максвелл
установил закон, определяющий число
молекул
![]() из общего числа молекул в единице объема
из общего числа молекул в единице объема
![]() (концентрация молекул), которые обладают
при данной температуре
скоростями поступательного движения
в интервале от
(концентрация молекул), которые обладают
при данной температуре
скоростями поступательного движения
в интервале от
![]() до
до
![]() :
:
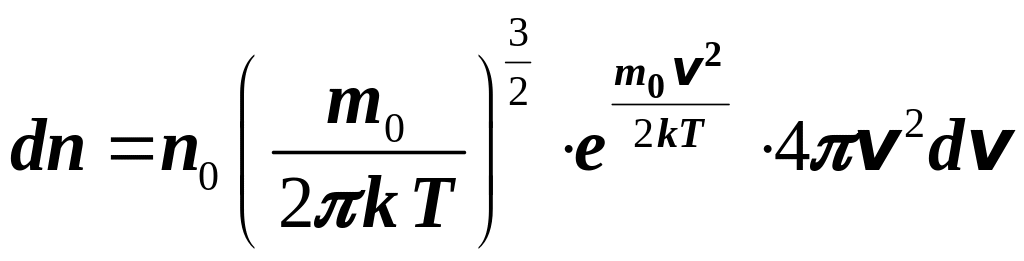 ,
где
,
где
— масса молекулы, — постоянная Больцмана.
Наиболее вероятная скорость молекул.
Из закона
распределения молекул по скоростям
можно
определить наиболее вероятную скорость
молекул
![]() .
Решая задачу на экстремум функции
.
Решая задачу на экстремум функции
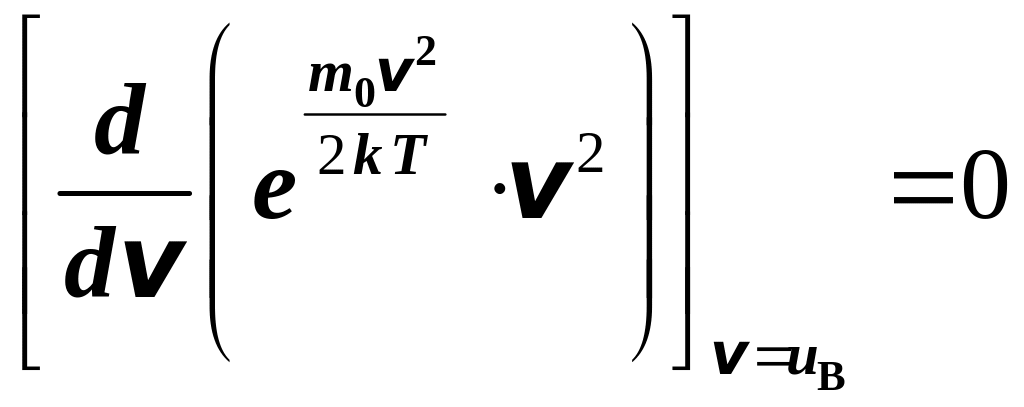 ,
,
получаем
 .
.
Таким образом наиболее вероятная скорость молекул зависит только от температуры и молярной массы молекул.
Закон максвелловского распределения молекул по скоростям может быть записан в виде:
 ,
,
где скорости
молекул
![]() рассматриваются в единицах наиболее
вероятной скорости
рассматриваются в единицах наиболее
вероятной скорости
![]() .
.
Рис.
7.4.2
Рис.
7.4.1

Число частиц
со скоростями в интервале от
до
![]() равно площади криволинейной трапеции.
Очевидно, что вся площадь, ограниченная
кривой
равно площади криволинейной трапеции.
Очевидно, что вся площадь, ограниченная
кривой
![]() равна концентрации молекул газа
.
С увеличением температуры газа максимум
кривой смещается в сторону больших
скоростей, а его высота уменьшается
(рис.7.4.2).
равна концентрации молекул газа
.
С увеличением температуры газа максимум
кривой смещается в сторону больших
скоростей, а его высота уменьшается
(рис.7.4.2).
Средняя арифметическая скорость молекул определяется интегралом

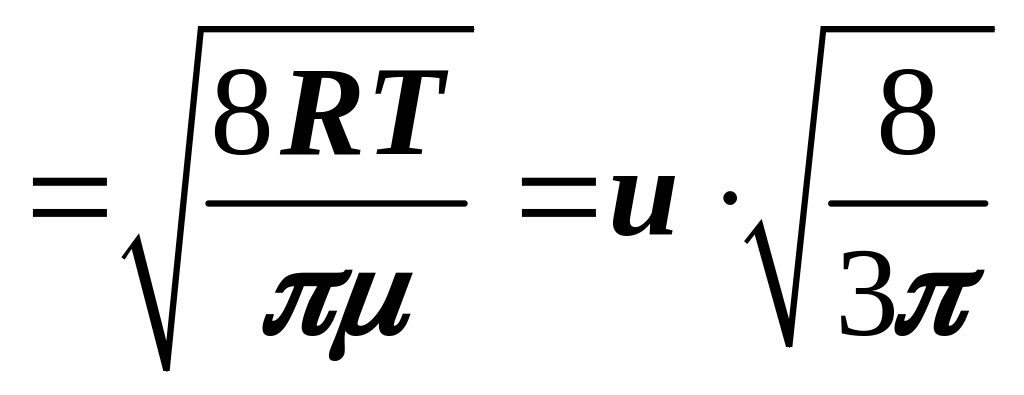 .
.
Таким образом, существуют три скорости, характеризующие состояние газа:
![]() — средняя
квадратичная скорость;
— средняя
квадратичная скорость;
![]()
![]() — средняя
арифметическая скорость;
— средняя
арифметическая скорость;
![]() — наиболее
вероятная скорость.
— наиболее
вероятная скорость.
7.5. Барометрическая формула #
Барометрическая формула. В реальных земных условиях на молекулы газ всегда действует сила тяжести. Тяготение и тепловое движение приводят к тому, что концентрация молекул и давление убывают с высотой.
Найдем закон
изменения давления газа с высотой. По
формуле Паскаля при увеличении высоты
на бесконечно малую величину
![]() ,
когда изменением плотности газа
,
когда изменением плотности газа
![]() можно пренебречь давление газа понизиться
на
можно пренебречь давление газа понизиться
на
![]() :
:
![]() .
.
Воспользуемся
уравнением состояния идеального газа
![]() и заменим плотность по формуле
и заменим плотность по формуле
![]() .
Тогда,
.
Тогда,
![]()
![]() .
.
Считая
![]() и интегрируя по высоте от
и интегрируя по высоте от
![]() до
до
![]() ,
получаем:
,
получаем:
![]() ,
или
,
или
![]() — барометрическая
формула.
— барометрическая
формула.
Здесь
![]() — давление газа на высотах
— давление газа на высотах
![]() .
.
Глава 8 основы термодинамики
8.1. Первый закон термодинамики
Внутренняя энергия (Дж) это кинетическая и потенциальная энергия атомов и молекул, из которых состоит тело. Для идеального газа это кинетическая энергия поступательного и вращательного движения его молекул.
Закон
равнораспределения
гласит:
на каждую степень свободы молекулы
приходится одинаковая энергия, равная
![]() ,
где
– постоянная Больцмана. Следовательно,
внутренняя
энергия
системы из
молекул, равна
,
где
– постоянная Больцмана. Следовательно,
внутренняя
энергия
системы из
молекул, равна
![]() или
или
![]() ,
где
,
где
– число степеней свободы молекулы,
– число молей газа,
– универсальная газовая постоянная,
– абсолютная температура.
Внутренняя энергия
является однозначной функцией
термодинамических параметров
![]() и
не зависит от предыстории состояния,
поэтому
и
не зависит от предыстории состояния,
поэтому
![]() является полным дифференциалом,
например, для идеального газа
является полным дифференциалом,
например, для идеального газа
![]() .
.
Количество
теплоты
![]() (Дж) – это энергия, передаваемая системе
путем теплообмена без
совершения механической работы.
Количество теплоты зависит от предыстории
состояния, например, как будет показано,
для изменения температуры системы на
один градус в различных процессах
требуется разное количество теплоты.
Количество теплоты не является полным
дифференциалом. Количество теплоты
можно определить, зная теплоемкость
процесса
(Дж) – это энергия, передаваемая системе
путем теплообмена без
совершения механической работы.
Количество теплоты зависит от предыстории
состояния, например, как будет показано,
для изменения температуры системы на
один градус в различных процессах
требуется разное количество теплоты.
Количество теплоты не является полным
дифференциалом. Количество теплоты
можно определить, зная теплоемкость
процесса
Теплоемкость (Дж/К) — это количество теплоты необходимое для изменения температуры системы на один кельвин.
![]()
Удельная теплоемкость это теплоемкость одного килограмма вещества. Зависит от строения вещества и температуры:
![]() .
.
Рис.
8.1.1
![]() (Дж),
совершаемая системой (газом) при
изменении объема
(Дж),
совершаемая системой (газом) при
изменении объема
![]() не является полным
дифференциалом и зависит от хода
термодинамического процесса
не является полным
дифференциалом и зависит от хода
термодинамического процесса
При расширении
газа (рис. 6.1.1) поршень площадью
под действием силы
![]() переместился на
.
Элементарная работа
переместился на
.
Элементарная работа
![]() .
Так как давление
.
Так как давление
![]() ,
то
,
то
![]() т.к.
т.к.
![]()
![]() .
.
Работа при конечном
изменении объема от
![]() до
до
![]() равна:
равна:
 .
.
Графически работа
определяется площадью криволинейной
трапеции на
![]() –
диаграмме (рис. 8.1.2):
–
диаграмме (рис. 8.1.2):


Рис. 8.1.2
На графиках стрелкой указаны направления процессов. При увеличении объема системы работа газа положительна, при уменьшении – отрицательна.
Первый закон термодинамики является законом сохранения энергии в термодинамических процессах.
Количество теплоты , сообщенное системе, идет на приращение ее внутренней энергии и на совершение системой работы :
![]() .
.
