
- •1. Расчетные химические задачи, их типы, овладение уч-ся по годам. Методические приемы формирования у уч-ся умения решать расчетные задачи по химии.
- •2. Растворы
- •4. Внеклассная работа по химии, её принципы, формы, направления.
- •7. Индивид. И дифференцир. Подходы к уч-ся в процессе обучения.
- •10. Методика формирования основ. Хим. Понятий. Этапы и пути. Развитие основн. Хим. Понятий.
- •11. Понятие о внутр. Энергии сис-мы и энтальпии. Теплота р-и, её термодинамические и термохимические обозначения. Закон Гесса и следствия из него.
- •13. Химический язык в школе. Структура. Значение формирования знаний химического языка.
- •14. Окислительно-восстановительные реакции.
- •17. Политехнизация знаний по химии.
- •18. Общая характеристика разбавленных р-ов неэлектролитов. Свойства р-ов. Роль осмоса в биологических процесса.
- •19. Производные карбоновых кислот: соли, галогенангидриды, ангидриды, эфиры, амиды и их взаимные переходы. Механизм реакции этерификации.
- •21. Формирование научного мировоззрения уч-ся при изучении химии в школе.
- •22. Химическая связь.
- •24. Методы обучения химии. Их клас-ция. Развив. Ф-ции.
- •25. Ионная связь.
- •26. Фенолы
- •Физические свойства
- •Химические свойства
- •26. Фенолы. Методы получения. Химические свойства: кислотность (влияние заместителей), реакции по гидроксильной группе и ароматическому кольцу.
- •27. Лекционно-семинарская система занятий по химии. Хар-ка структ. Эл-тов с-мы.
- •28. Общая характеристика и электронное строение атомов элементов V группы главной подгруппы. Аммиак, строение молекул, получение и свойства.
- •Аммиак (nh3)
- •29. Альдегиды, кетоны и карбоновые кислоты ароматического ряда. Способы получения и химические свойства.
- •30. Уроки обобщения знаний и умений уч-ся. Их особ-сти, класс-ция. Пути систематизации знаний.
- •31. Кислоты, основания, соли с точки зрения тэд.
- •33. Принципы обучения химии.
- •34. Обратимые и необратимые реакции.
- •36. Особенности урока химии как осн. Орг. Формы обучения. Типы, клас-ция уроков изучения новых знаний. Факторы, определяющие кач-во этих уроков.
- •37. Квантово-механическая модель строения атома.
- •39.Структура основных химических понятий, их формирование и развитие.
- •41. Ферменты
- •42. Наглядность в обучении химии. Виды и методы ее использования на уроках.
- •43. Металлы
- •44.Биосинтез белка. Этапы белкового синтеза. Строение рибосом и их роль в биосинтезе белка.
- •45. Химический кабинет в школе.
- •46. IV группа, гл. Подгруппа
- •Углерод
- •47. Рнк. Типы рнк. Структура рнк.Роль тРнк в биосинтезе белка.
- •48.Пути развития мышления учащихся при изучении химии в средней школе.
- •50. Одно – и многоатомные спирты
- •I. Реакции замещения
- •II. Реакции отщепления
- •III. Реакции окисления
- •II. Замещение гидроксильных групп
- •51.Демонстрационный эксперимент в обучении химии
30. Уроки обобщения знаний и умений уч-ся. Их особ-сти, класс-ция. Пути систематизации знаний.
Роль обобщения в химии: дает возм-сть привести знания в с-му, установить взаимосв. м/у разделами химии и др. учебн. предметами; позволяет сформулир. мировоззр. выводы; сделать выводы о значении данного мат-ла для человека; развить мышление. Виды обобщений: эмпирическое (на уровне индукции); теоретическое (на уровне дедукции). Основные требования к орг-ции обобщения: уч-ся должны быть готовы к обобщ. уроку; должна активироваться позноват. д-сть уч-ся. Орг-ся самост. работа; В задания для самост. работы включ-ся задания, дающие возм-сть применять знания из др. наук. Межпредм. связи; Должен присутствовать новый мат-л; Должны решаться проблемы, кот стоят перед наукой; Широко исп-ся тех. средства, наглядность, эксперимент; выводы следует делать на основе сост. и анализа системат. таблиц, схем. Клас-ция:
Вид урока |
Разновидность |
Лекция Лекция с демонстр. Доклады уч-ся
Беседа Работа с учебником Работа с раздаточным мат-лом Теле и кино-уроки Семинар. занятия |
Обобщ. Лекция Демонстр. Повтор. Опытов, опыты-задачи. Обзорные, с демостр. опытов и нагл. пособий Повторение, упражн., составл. обощ. схем, табл.
Воспризв., аналитико-синт. деят. Фронт. работа, работа по группам. |
31. Кислоты, основания, соли с точки зрения тэд.
Кислоты- это электролиты, распвдающиеся в водных растворах с образованием гидратированных ионов Н+.
HCl—→H2OH++Cl-
HCN↔H2OH++CN-
H2SO4↔H2OH++HSO3- HSO3-↔H2OH++SO3-
Основания-это электролиты, расп-ся в водных растворах с образ-м гидротиров-х гидроксид- ионов.
KOH→H2OK++OH-
NH3*H2O↔H2ONH4++OH-
Pb(OH)2↔H2OPbOH++OH-
PbOH↔+H2OPb2++OH-
Соли-это электролиты,расп-ся на катионы Мет.(илиNH4+) и анионы кислотных остатков.Соли: средние K2SO3→H2O2K++SO32- двойные: KAl(SO4)2→H2OK++Al3++2SO42-
кислые(гидросоли) NaHCO3→H2ONa++HCO3-
комплексные K3[Fe(CN)6]→H2O3K++[Fe(CN)6]3-
основные(гидроксосоли) Al(OH)2Cl→H2O[Al(OH)2]++Cl-
Кислотный, основный и амфотерный тип ионизации гидроксидов.
Тип ионизации опред-ся полярностью и поляризуемостью хим.связей. Кислотно-основные св-ва гидроксидов опр-ся природой центрального атома,т.е.его Мет.или неМет.св-ми,гидроксид будет вести себя как основание, если преобладают Мет.св-ва центр.атома; гидроксид будет вести себя как кислота, если преобладают неМет.св-ва центр.атома. Сила кислородсодержащих кислот зависит от строения молекул. (НО)nЭОm . Как установлено экпериментально сила к-т практически не зависит от n, но возрастает с увеличением m. Резкое возрастание силы в ряду кислот с увеличением m можно объяснить оттягиванием электронной плотности от связи Н-О, на связь Э=О.
(НО)nЭ-очень слабая кислота
(НО)n ЭО- слабая кислота
(НО)nЭО2- сильная кислота
(НО)nЭО3- очень сильная кислота
С увелич-м степени окисления центр.атома увелич-ся m, а значит и возрастает сила кислот.
HClO HClO2 HClO3 HClO4
Ст.ок. Cl ————————————→
m ————————————→
сила к-ты ———————————→
HNO2 HNO3
(HO)NO (HO)NO2
Ст.ок. —————————→
m —————————→
сила к-ты ————————→
Mn(OH)2 Mn(OH)3 Mn(OH)4 H2MnO4 HMnO4
осн. слаб.осн. амф. к-та очень
ст.ок. ————————————————————→
кисл.св-ва ————————————————————→
основн.св-ва ←———————————————————
Протонная теория кислот и оснований:или теория Бренстеда и Лоури.
Определение к-т и оснований с точки зрения ТЭД ограниченно только водными р-ми и только гидроксидсодержащими основаниями.Но ряд осн-й(NH3) не подходят под определение основания с точки зрения ТЭД.
Согласно этой теории, кислоты-это в-ва,отщепляющие при данной р-ции протоны,т.е.являющиеся донорами протонов. Основания- это в-ва , способные принимать протоны,т.е.явл-ся акцепторами протонов. Р-цию между кислотой и основанием, согласно теории, можно записать в виде протолитического равновесия.
Н-А+:В↔А-+ НВ+ HF+H2O↔F-+H3O+
к-та осн-е осн-е к-та к-та осн-е осн-е к-та
С2H5OH+: NH3↔C2H5O-+NH4+
к-та осн-е осн-е к-та
Еще более общее опред-е кислот и оснований было дано Льюисом, основанное на участии электронных пар.
Кислота Льюиса – это катионы, анионы или нейтральные молекулы, способные принять одну или несколько электронных пар, или это акцептор электр-х пар.
Основание Льюиса- это катионы, анионы или нейтральные молекулы,способные отдаватьэлектронные пары, или это доноры электр-х пар.
AlF3+: NH3= AlF3*NH3
к-та осн-е
Н++: ОН-=Н2О
к-та осн-е
32. Полисахариды. Высокомолекулярные несахароподобные углеводы, содержащие от 10 до сотен тысяч остатков моносахаридов, связанных гликозидными связями. Важнейшие представители: крахмал, целлюлоза, гликоген. Это природные полимеры (ВМС), мономером которых является глюкоза. Их общая формула (С6Н10О5)n Значение nцел >>nкр и достигает в некоторых видах до 40 тысяч, а молекулярная масса доходит до нескольких миллионов.
Крахмал. Аморфный порошок белокго цвета, без вкуса и запаха, плохо растворим в воде, в горячей воде образует коллоидный раствор. Макромолекулы крахмала построены из большого числа остатков α-глюкозы. Крахмал состоит из двух фракций: амилозы и амилопектина. Соотношение между ними в крахмалах разных растений различно. В среднем содержание амилозы – 20-30%, амилопектина – 70-80%..
Гликоген – это эквивалент крахмала, синтезируемый в животных орагнизмах,т.е.это тоже резервный полисахарид, молекулы которого построены из большого числа остатков α-глюкозы. Содержится гликоген главным образом в печени и мышцах. По своему строению он очень близок амилопектину.
Гликоген – белый аморфный порошок, хорошо растворимый даже в холодной воде, легко гидролизуется под действием кислот и ферментов, образуя в качестве промежуточных веществ декстрины, мальтозу и при полном гидролизе – глюкозу.
Молекулы целлюлозы имеют линейное (неразветвленное) строение, вследствие чего целлюлоза образует волокна.
Макромолекулы целлюлозы построены из остатков β-глюкозы. В этом заключается главное отличие целлюлозы от крахмала.
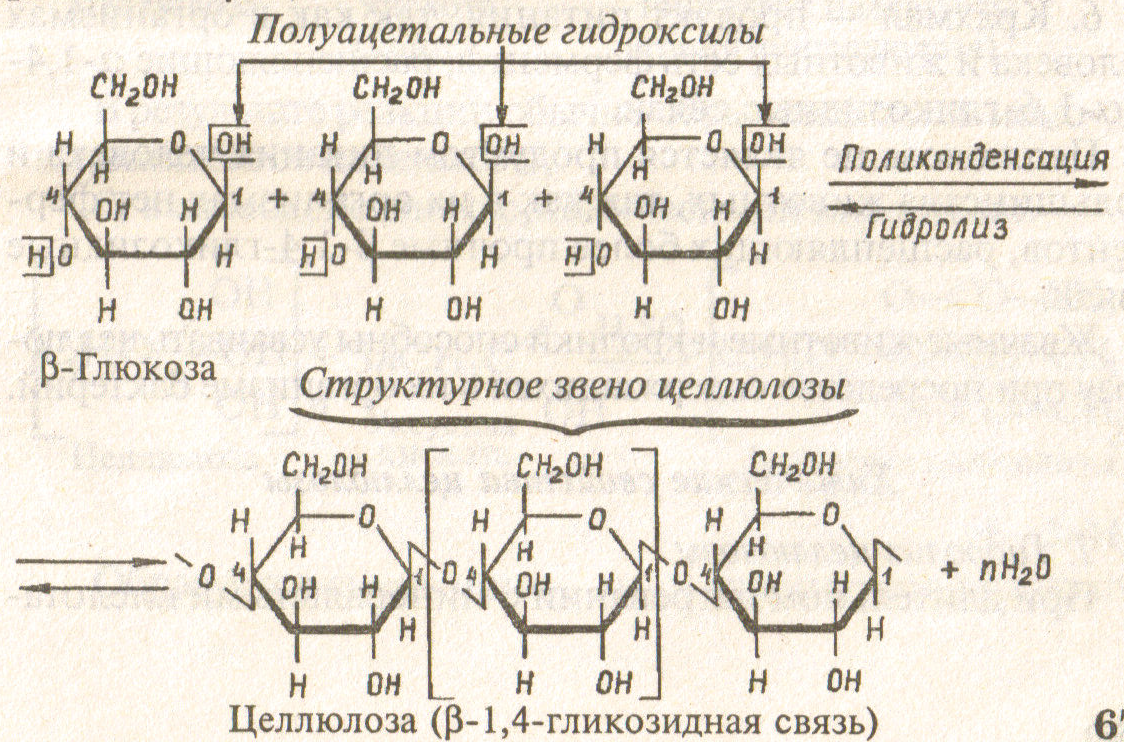
Следует особо отметить, что в молекуле целлюлозы каждое второе кольцо остатка глюкозы повернуто на 180° относительно первого. Это обеспечивает плотную упаковку макромолекул целлюлозы. Вы видите, что каждый остаток глюкозы содержит три гидроксильные группы. Поэтому между цепями макромолекул могут образовываться межмолекулярные водородные связи. Это увеличивает механическую прочность целлюлозы. Поэтому целлюлоза образует каркас растительной клетки.
Физические свойства:
Чистая целлюлоза – белое твердое вещество, нерастворимое в воде и обычных органических растворителях, но хорошо растворимое в аммиачном растворе гидроксида меди (II) – реактив Швейцера. Из этого раствора кислоты осаждают целлюлозу в виде волокон (гидрат целлюлозы).
Химические свойства:
Небольшие различия в строении молекул крахмала и целлюлозы обуславливают значительные различия в свойствах полимеров: целлюлоза не дает реакции серебряного зеркала (нет альдегидной группы), но с кислотами вступает в реакции этерификации. Это дает основание рассматривать каждое звено С6Н10О5 как остаток глюкозы, содержащий три гидроксильные группы:
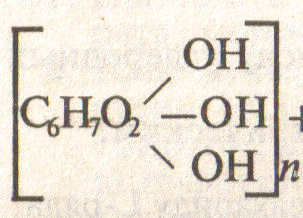 или [C6H7O2(OH)3]
или [C6H7O2(OH)3]
За счет них целлюлоза может образовывать простые и сложные эфиры.
При взаимодействии целлюлозы с концентрированной азотной кислотой в присутствии концентрированной серной в качестве водоотнимающего средства образуется сложный эфир – тринитрат целлюлозы
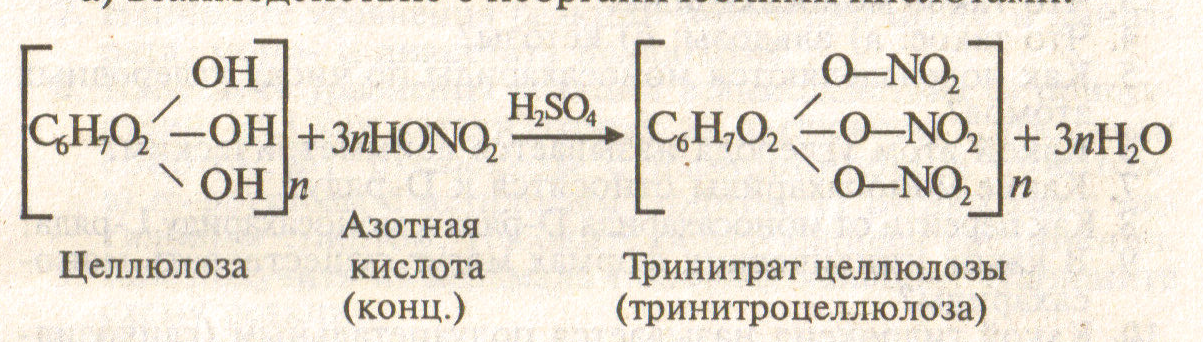
При обычной температуре целлюлоза взаимодействует только с концентрированными кислотами.
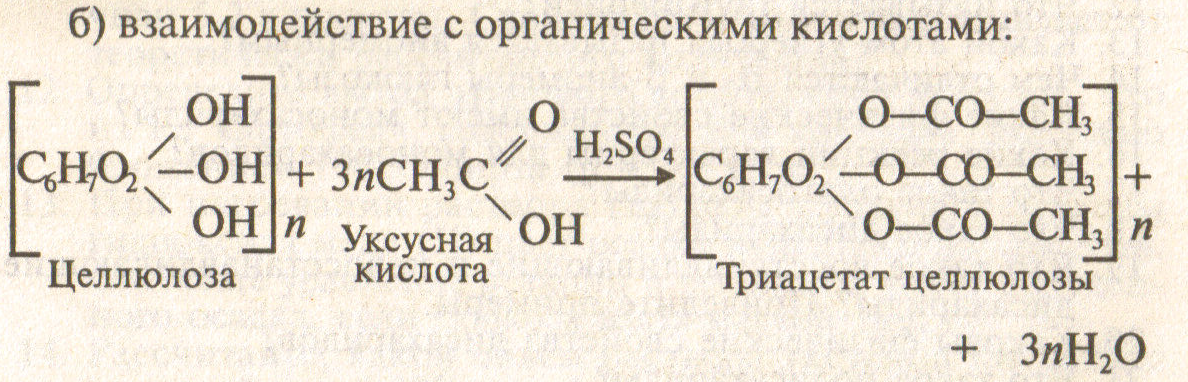
Подобно крахмалу, целлюлоза при нагревании с разбавленными кислотами подвергается гидролизу:
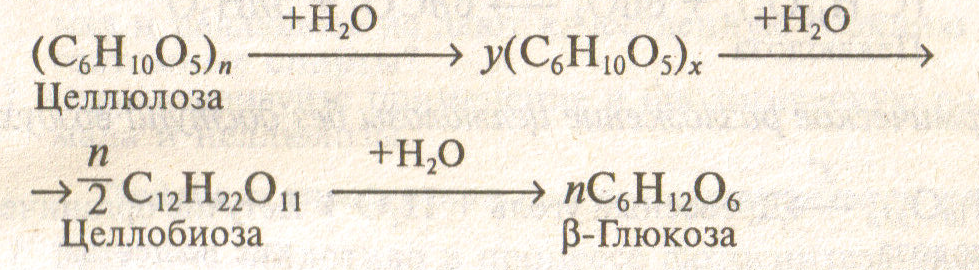
Гидролиз целлюлозы, иначе называется осахариванием, - очень важное свойство целлюлозы, он позволяет получить из древесных опилок и стружек глюкозу, а сбраживанием последних – этиловый спирт. Такой спирт называют гидролизным. На гидролизных заводах из 1 тонны древесины получают до 200 литров спирта.
Для целлюлозы характерно горение:
(С6Н10О5)n + 6nО2 → 6nСО2 + 5nН2О + Q
Без доступа воздуха – термическое разложение целлюлозы приводит к образованию СН3ОН, СН3СООН, (СН3)2СО и др.
Применение:
Сырая глюкоза, полученная из древесины, может служить кормом для скота.
Гидролизный спирт (см. выше)
Целлюлоза в виде хлопка, льна и пеньки идет на изготовление тканей – хлопчатобумажных и льняных.
Большое количество расходуется на производство бумаги. Дешевые сорта изготавливают из древесины хвойных пород, лучшие – из льняного и хлопчатобумажного тряпья.
Подвергая целлюлозу химической обработке, получают несколько видов искусственного шелка, пластмассы, кинопленку, бездымный порох (тринитроцеллюлоза), лаки и многое другое.
