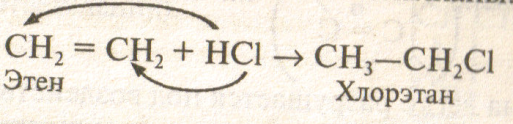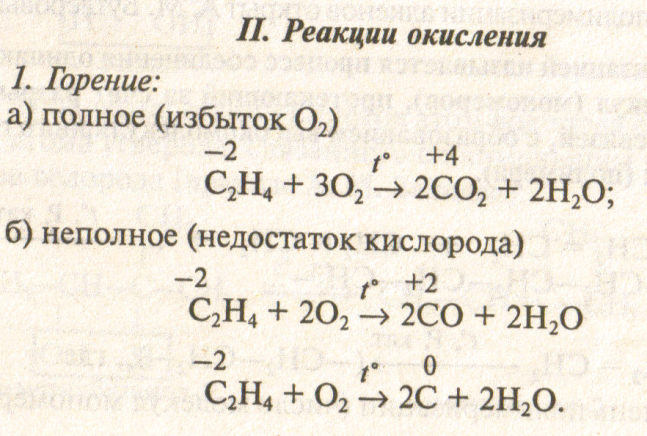- •53.Экспериментальные (качественные) задачи по химии.
- •54. Азотная кислота
- •55. Моносахариды
- •56.Подготовка учителя к уроку.Виды планирования.Рабочий плпн урока.
- •58. Дисахариды
- •Физические свойства
- •59. Массовая внеклассная работа по химии.
- •60. Растворы электролитов. Эл. Диссоциация.
- •61. Альдегиды, кетоны. Изомерия и номенклатура. Сравнительная реакционная способность альдегидов и кетонов. Способы получения и химические свойства.
- •62. Самостоятельная работа учащихся по химии.
- •65. Задачи курса химии средней школы.
- •66. Скорости хим. Р-й. Факторы, влияющие на скорость хим. Р-й. Классиф. Хим. Р-й. Молекулярность и порядок р-и. Энергия активации.
- •68. Технические средства обучения (тсо)
- •71. Лабороторные и практические занятия по химии.
- •72. Cерная кислота
- •73. Структура нуклеотидов и нуклеозидов. Динуклеотиды. Надф и фад.
- •7 4. Проверка знаний и умений по химии.
- •75. Основные химические понятия.
- •Основные законы химии
- •Способы получения
- •Физические свойства
62. Самостоятельная работа учащихся по химии.
Самостоятельная работа-работа,выполняемая по заданию учителя или в в специально отведенное время,в ходе которой учащиеся стремятся достигнуть цели,оформить результат выполняемой работы.
По форме организации подразделяют:
а) фронтальные
Повысить развивающую функцию фронтальных работ можно: разнообразием, дифференциацией работы. Дифференцированные задания для фронтальных самостоятельных работ как min состоят из 3 частей,расположенных в порядке нарастания сложности от 1 части к 3.Такие задания можно использовать не только для формирования знаний,но и для контроля уровня усвоения.
б) групповые
Выполняются группами школьников по разной степени сложности заданий и с различной дидактической целью.
Выделяют:
-гомогенные группы (по уровню усвоения знаний)
-гетерогееные группы (по уровню различного усвоения знаний)
в) индивидуальные
Наиболее значительные среди них-творческие задания.
Проблемное обучение — это такой тип организации работы на уроке, основой которого является развитие познавательной самостоятельности учащихся в поисковой исследовательской деятельности.
Сущность проблемного обучения — в создании проблемных ситуаций на уроке и их разрешении или самим учителем, или с частичным привлечением учащихся, или самостоятельно учащимися. Содержание курса химии дает возможность на многих уроках создавать проблемные ситуации. Они возможны тогда, когда ученики встречаются с каким-либо противоречием: между известными фактами и новыми, между теорией и опытом, между разными фактами, между теоретическими представлениями и фактами.
Проблемное обучение развивает творческие способности учащихся. Наибольший эффект достигается в том случае, когда учащиеся самостоятельно выдвигают проблемы и решают их.
64. Алкены. Это УВ, в молекулах которых два атома углерода находятся в состоянии sp2 - гибридизации и связаны друг с другом двойной связью.
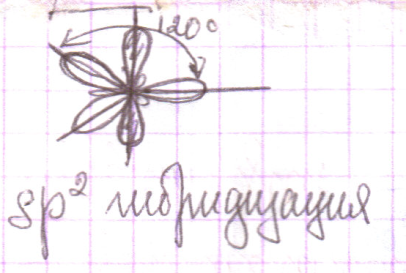
Длина связи С=С в алкенах равна 0,134нм. Каждый атом углерода у двойной связи соединен с двумя другими атомами и может присоединять еще один атом.
Изомерия и номенклатура
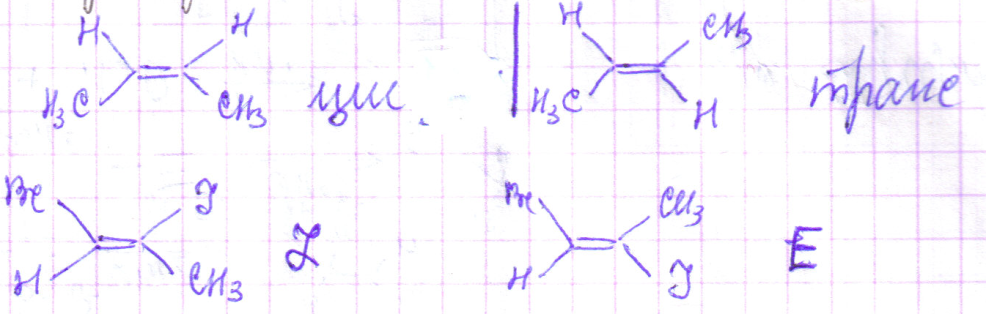
Для алкенов возможны три типа изомерии: изомерия углеродной цепи, изомерия положения двойной связи, изомерия углеродной цепи, пространственная изомерия
Синтез. В промышленности – крекигн алканов, дегидрирование алканов
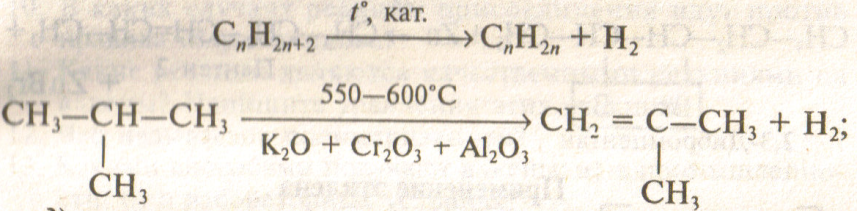
гидрирование алкинов

При дегидратации спиртов атом водорода отщепляется от атома углерода, связанного с наименьшим числом атомов водорода (правило А. М. Зайцева):
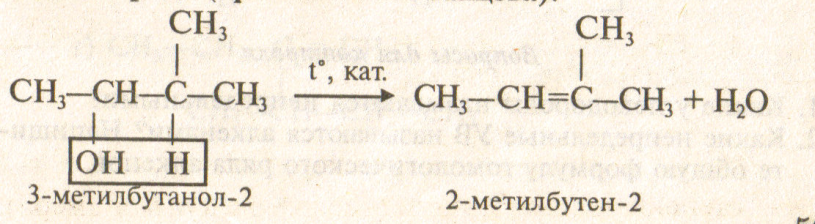
2) Дегидрогалогенирование моногалогеналканов (-ННа!) действием твердой щелочи или ее спиртового раствора. Происходит по правилу А. М. Зайцева:
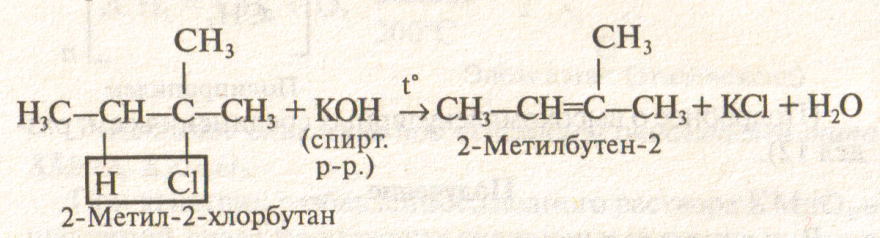
3) Дегалогенирование (-2На1) дигалогеналканов с атомами галогена у соседних атомов «С» действием 2п или М§:
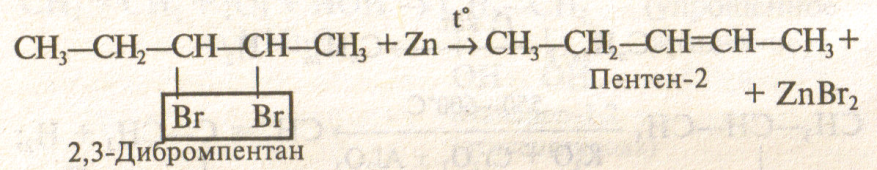
Химические свойства
Алкены обладают большей реакционной способностью, чем алканы. Это обусловлено наличием в их молекулах двойной связи π-связь менее прочная, чем σ-связь. Она легко разрушается под воздействием различных реагентов. Освободившиеся в результате разрыва п-связи валентности углеродных атомов используются для присоединения атомов или групп атомов молекулы реагента. Для алкенов характерны реакции присоединения.
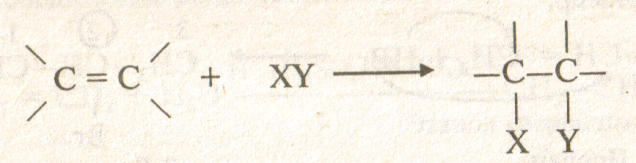
Присоединение водорода (+Н2) – гидрирование, образуются алканы:
![]()
Присоединение галогенов – галогенирование, образуются дигалогеналканы6
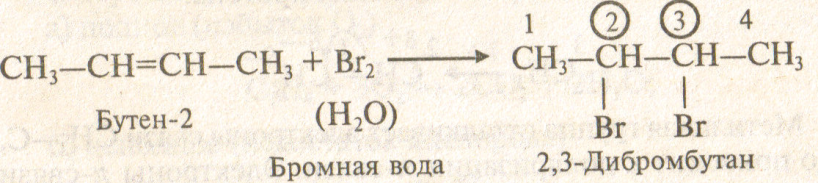
Бромная вода имеет желтый цвет. При взаимодействии с алкенами бромная вода обесцвечивается, поэтому реакция с бромной водой используется для идентификации алкенов.
Присоединение галогеноводородов