
- •1. Математическая модель и производная второй вариации энтропии
- •2. Изменение избытка энтропии за счёт теплообмена с окружающей средой
- •3. Изменение избытка энтропии за счёт массообмена с окружающей средой
- •4. Простая необратимая реакция
- •4.1. Вывод выражения для избыточного производства энтропии
- •4.2. Анализ устойчивости режима в реакторе
- •4. Простая необратимая реакция
- •4.3. Задача о тепловой устойчивости процесса
- •5. Автокаталитическая реакция
- •5.1. Вывод выражения для избыточного производства энтропии
- •5.2. Анализ устойчивости режима в реакторе
- •6. Простая реакционная схема
- •6.1. Вывод выражения для избыточного производства энтропии
- •6.2. Анализ устойчивости режима в реакторе с помощью критерия Сильвестра
- •7. Реакционные схемы БелоусоваЖаботинского и БриггсаРаушера
- •7.1. Выражения для производной второй вариации энтропии
- •7.2. Анализ причин осцилляций
- •8. Осцилляторы в реакторах с рециклами
- •8.1. Математическое описание реактора с рециклом
- •8.2. Анализ влияния рецикла на устойчивость режима в реакторе
- •9. Классификация колебательных процессов в химии
4. Простая необратимая реакция
4.3. Задача о тепловой устойчивости процесса
Анализ устойчивости химического процесса в проточном реакторе с мешалкой свидетельствует о том, что наличие прямых реакций приводит к стабилизации концентрационного режима, т.е. рассматриваемый реакционный механизм не может вызвать появление концентрационных пульсаций в реакторе. Однако в такой системе может возникнуть тепловая неустойчивость при высоких тепловых эффектах химических реакций и недостаточном теплоотводе. Зависимость константы скорости химической реакции от температуры приведёт к тому, что при возникновении в системе пульсаций по температуре могут возникнуть и концентрационные пульсации, что не позволит гарантировать стабильность свойств получаемого продукта. Таким образом, задаче о тепловой устойчивости химического процесса в реакторе следует уделить особое внимание. Рассмотрим подход к её решению на примере простой необратимой реакции в проточном реакторе с мешалкой.
Пусть для рассматриваемой системы гарантирована стабильность концентраций всех компонентов, как в самом реакторе, так и во входном потоке, т.е.
![]()
и допускаются
только пульсации по температуре
![]() .
Выражение для производной термодинамической
функции Ляпунова (второй вариации
энтропии системы) (6.5) при этом преобразуется
к виду:
.
Выражение для производной термодинамической
функции Ляпунова (второй вариации
энтропии системы) (6.5) при этом преобразуется
к виду:
![]()
Видно, что производная термодинамической функции Ляпунова положительна при условии:
![]()
Отсюда можно получить зависимость для управляющего параметра химического процесса – времени пребывания в реакторе, при котором тепловая устойчивость системы будет гарантирована:
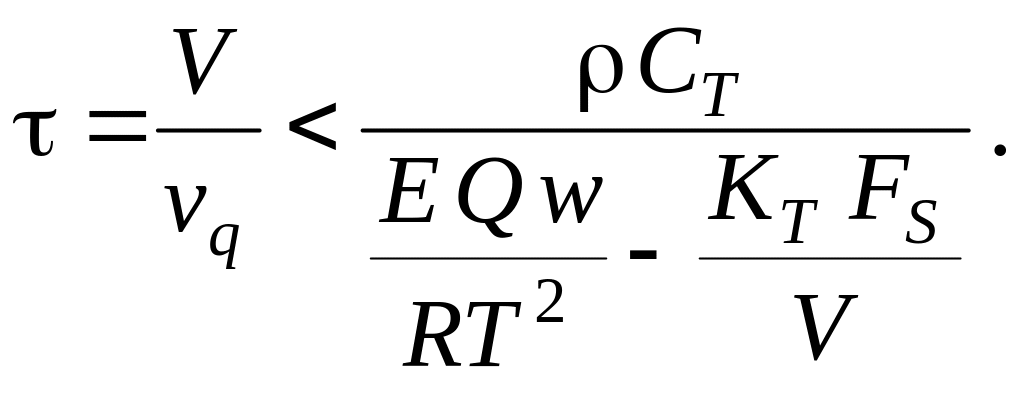
5. Автокаталитическая реакция
5.1. Вывод выражения для избыточного производства энтропии
Пусть в проточном реакторе с мешалкой протекает автокаталитическая реакция
![]()
Скорость и химическое сродство такой реакции имеют вид:
![]()
где х концентрация вещества Х; y концентрация вещества Y.
Получим вариацию от термодинамического потока процесса (скорости реакции):
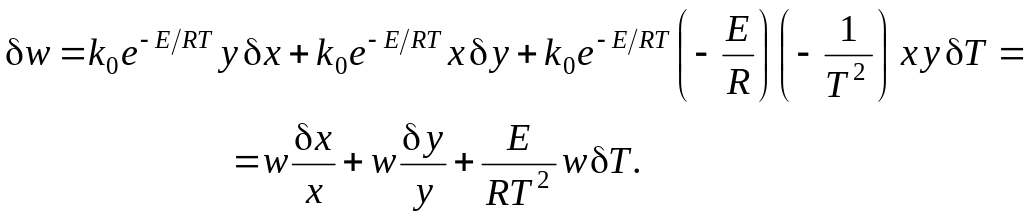
Получим вариацию от термодинамической движущей силы процесса (химического сродства, отнесённого к температуре реакционной смеси):
![]()
Таким образом, избыточное производство энтропии процесса имеет вид:
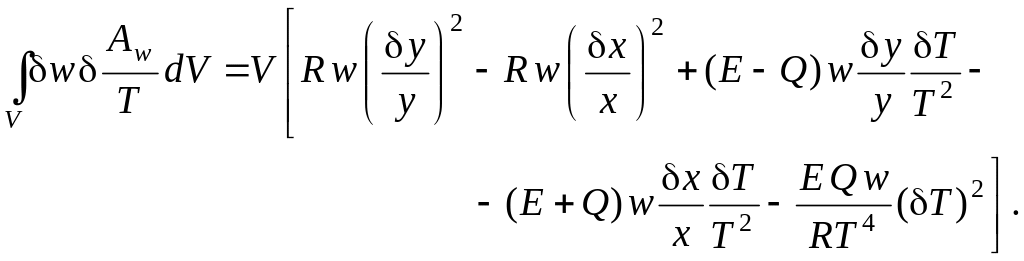 (6.6)
(6.6)
Подставляя выражения (6.2), (6.3а) и (6.6) в (6.1), получим в явном виде производную термодинамической функции Ляпунова (второй вариации энтропии) для проточного реактора с мешалкой, в котором протекает автокаталитическая реакция:
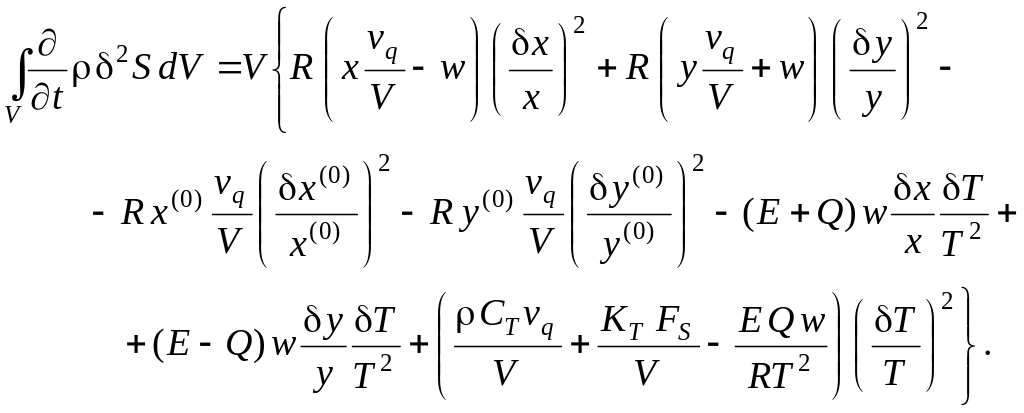 (6.7)
(6.7)
Напомним, что если выражение (6.7), являющееся квадратичной формой, положительно определено, то стационарное состояние системы устойчиво, если – отрицательно, то состояние – неустойчиво (согласно второму методу Ляпунова). Для определения знака квадратичной формы используется критерий Сильвестра.
5.2. Анализ устойчивости режима в реакторе
При анализе выражения (6.7) остановимся подробно только на тех эффектах, которые не рассматривались при анализе устойчивости химического процесса с простой необратимой реакцией. Так, член
![]()
характеризует непосредственно автокаталитический химический процесс. Очевидно, что он имеет отрицательный знак, что усиливает дестабилизацию системы.
Слагаемое
![]()
соответствует термокинетическому эффекту: если увеличение температуры (которое может произойти вследствие интенсивного тепловыделения в процессе реакции) способствует ускорению реакции, то в системе будет происходить накопление вещества X, т.е.
![]()
Следовательно, данное слагаемое будет иметь отрицательный знак, что также усиливает дестабилизацию системы.
Таким образом, наличие в системе автокаталитических химических реакций понижает устойчивость системы, дестабилизирует её как за счёт самого реакционного механизма, так и за счёт термокинетических связей. Если вклад этих эффектов начинает преобладать, то исследуемый режим становится неустойчивым и в системе возможно возникновение диссипативных структур.
