
- •1. Математическая модель и производная второй вариации энтропии
- •2. Изменение избытка энтропии за счёт теплообмена с окружающей средой
- •3. Изменение избытка энтропии за счёт массообмена с окружающей средой
- •4. Простая необратимая реакция
- •4.1. Вывод выражения для избыточного производства энтропии
- •4.2. Анализ устойчивости режима в реакторе
- •4. Простая необратимая реакция
- •4.3. Задача о тепловой устойчивости процесса
- •5. Автокаталитическая реакция
- •5.1. Вывод выражения для избыточного производства энтропии
- •5.2. Анализ устойчивости режима в реакторе
- •6. Простая реакционная схема
- •6.1. Вывод выражения для избыточного производства энтропии
- •6.2. Анализ устойчивости режима в реакторе с помощью критерия Сильвестра
- •7. Реакционные схемы БелоусоваЖаботинского и БриггсаРаушера
- •7.1. Выражения для производной второй вариации энтропии
- •7.2. Анализ причин осцилляций
- •8. Осцилляторы в реакторах с рециклами
- •8.1. Математическое описание реактора с рециклом
- •8.2. Анализ влияния рецикла на устойчивость режима в реакторе
- •9. Классификация колебательных процессов в химии
Химические осцилляторы
1. Математическая модель и производная второй вариации энтропии
2. Изменение избытка энтропии за счёт теплообмена с окружающей средой
3. Изменение избытка энтропии за счёт массообмена с окружающей средой
4. Простая необратимая реакция
4.1. Вывод выражения для избыточного производства энтропии
4.2. Анализ устойчивости режима в реакторе
4.3. Задача о тепловой устойчивости процесса
5. Автокаталитическая реакция
5.1. Вывод выражения для избыточного производства энтропии
5.2. Анализ устойчивости режима в реакторе
6. Простая реакционная схема
6.1. Вывод выражения для избыточного производства энтропии
6.2. Анализ устойчивости режима в реакторе с помощью критерия Сильвестра
7. Реакционные схемы БелоусоваЖаботинского и БриггсаРаушера
7.1. Выражения для производной второй вариации энтропии
7.2. Анализ причин осцилляций
8. Осцилляторы в реакторах с рециклами
8.1. Математическое описание реактора с рециклом
8.2. Анализ влияния рецикла на устойчивость режима в реакторе
9. Классификация колебательных процессов в химии
1. Математическая модель и производная второй вариации энтропии
Рассмотрим ёмкостной проточный реактор смешения с охлаждением через рубашку, в котором могут происходить реакции типа
![]()
Математическая модель проточного реактора смешения имеет вид:
![]()
![]()
где
![]() – концентрация k-го компонента;
– концентрация k-го компонента;
![]() – объёмный расход поступающего раствора;
w скорость
химической реакции; Q
тепловой эффект реакции;
– объёмный расход поступающего раствора;
w скорость
химической реакции; Q
тепловой эффект реакции;
![]() – коэффициент теплопередачи; V
рабочий объём реактора;
– коэффициент теплопередачи; V
рабочий объём реактора;
![]() – поверхность реактора;
– поверхность реактора;
![]() – теплоёмкость, плотность и температура
смеси в реакторе;
– теплоёмкость, плотность и температура
смеси в реакторе;
![]() – температура хладагента в рубашке;
индекс (0) означает значение параметра
на входе в реактор.
– температура хладагента в рубашке;
индекс (0) означает значение параметра
на входе в реактор.
Поскольку реакции протекают в ёмкостном реакторе с мешалкой, в качестве необратимых процессов следует рассматривать только непосредственно химические превращения. Соотношение для производной второй вариации энтропии (5.7) при этом преобразуется к виду:
![]() (6.1)
(6.1)
где
![]() – сродство химической реакции;
– сродство химической реакции;
![]() – тепловой поток через единицу поверхности
реактора;
– тепловой поток через единицу поверхности
реактора;
![]() – скорость движения реакционной смеси;
– скорость движения реакционной смеси;
![]() – химический потенциал k-го компонента;
индекс n означает
проекцию вектора на нормаль к поверхности
реактора FS
.
– химический потенциал k-го компонента;
индекс n означает
проекцию вектора на нормаль к поверхности
реактора FS
.
Первое и второе слагаемые в правой части выражения (6.1) характеризуют изменение избытка энтропии за счёт тепло- и массообмена системы с окружающей средой, т.е. за счёт наличия протока через реактор и теплообмена через поверхность реактора с хладагентом в рубашке; таким образом, эти слагаемые определяются только конструкционными особенностями реактора. Последнее слагаемое является избыточным производством энтропии; оно зависит от типа химических превращений, протекающих в реакторе.
Напомним, что вторая вариация энтропии является термодинамической функцией Ляпунова для систем, удалённых от равновесия, и согласно второму методу Ляпунова производная этой функции должна быть положительной, чтобы стационарное состояние системы было устойчивым. Однако даже при отсутствии возможности рассчитать величину в выражении (6.1) простой анализ знаков отдельных слагаемых позволяет сделать важные выводы о том, какие процессы дестабилизируют систему (описывающие их члены в выражении (6.1) будут всегда отрицательны), а какие, наоборот, – повышают её устойчивость (описывающие их члены – всегда положительны), и как необходимо изменить условия протекания процесса, чтобы ослабить влияние первых и усилить влияние вторых.
2. Изменение избытка энтропии за счёт теплообмена с окружающей средой
Получим выражение для изменения избытка энтропии проточного реактора с мешалкой за счёт обмена энергией с окружающей средой:
![]()
Вариация от величины, обратной температуре в реакторе, определяется согласно правилам дифференцирования:
![]()
Тепловой поток из реактора в окружающую среду, отнесённый к единице поверхности реактора, определяется по формуле:
![]()
Первое слагаемое в правой части этого уравнения характеризует отвод тепла через поверхность реактора за счёт теплообмена с хладагентом в рубашке; второе слагаемое – изменение теплоты реакционной смеси за счёт наличия протока через реактор.
Допуская,
что температура питательного раствора
и температура хладагента в рубашке –
величины постоянные, получим вариацию
от теплового потока
![]() :
:
![]()
Подставим полученные выражения для вариаций в исходную формулу:
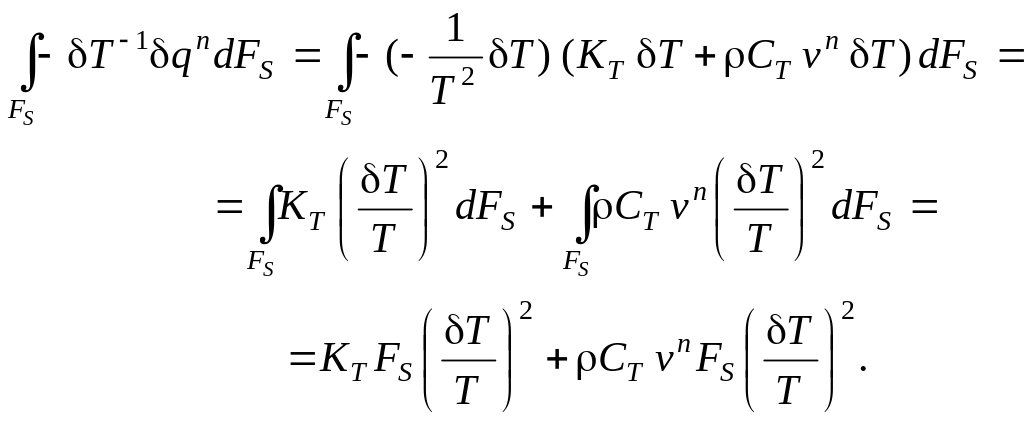
Учитывая, что
![]()
получим итоговое выражение для изменения избытка энтропии проточного реактора с мешалкой за счёт обмена энергией с окружающей средой:
![]() (6.2)
(6.2)
Отметим, что выражение (6.2) определяется только типом реактора и не зависит от того, какие химические превращения в нём протекают, что позволяет его применять для любой реакционной схемы.
