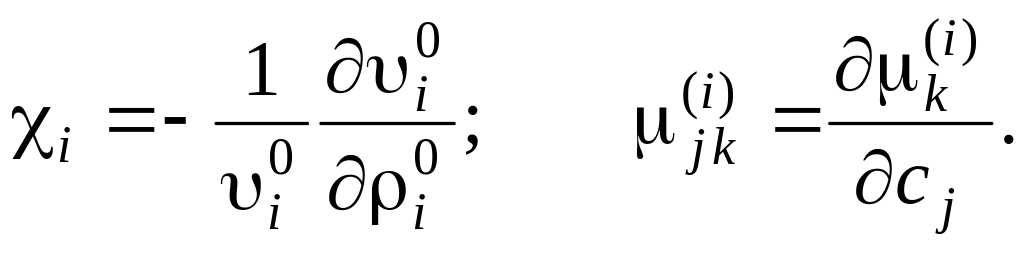- •1. Проблемы исследования нелинейных систем
- •2. Вторая вариация энтропии многофазной гетерогенной среды
- •3. Исследование знака второй вариации энтропии
- •4. Производная второй вариации энтропии. Термодинамический анализ
- •5. Осцилляторы при кристаллизации малорастворимых веществ
- •5.1. Представления Оствальда об образовании периодических структур
- •5.2. Кристаллизация малорастворимых веществ
- •5.3. Механизм кристаллизации малорастворимых веществ
- •5.4. Примеры образования диссипативных структур при кристаллизации
- •5.5. Выражение для избыточного производства энтропии
- •5.6. Анализ причин образования диссипативных структур
Термодинамика нелинейных систем
1. Проблемы исследования нелинейных систем
2. Вторая вариация энтропии многофазной гетерогенной среды
3. Исследование знака второй вариации энтропии
4. Производная второй вариации энтропии. Термодинамический анализ
5. Осцилляторы при кристаллизации малорастворимых веществ
5.1. Представления Оствальда об образовании периодических структур
5.2. Кристаллизация малорастворимых веществ
5.3. Механизм кристаллизации малорастворимых веществ
5.4. Примеры образования диссипативных структур при кристаллизации
5.5. Выражение для избыточного производства энтропии
5.6. Анализ причин образования диссипативных структур
1. Проблемы исследования нелинейных систем
Линейная неравновесная термодинамика описывает стабильное, предсказуемое поведение систем, стремящихся к минимальной активности в соответствии с питающими их внешними потоками. Из того, что линейная термодинамика допускает описание с помощью потенциала (а именно, производства энтропии), следует: при эволюции к равновесию или к стационарному состоянию система “забывает” начальные условия. Каковы бы ни были начальные условия, система рано или поздно перейдёт в состояние, определяемое граничными условиями. В результате реакция такой системы на любое изменение граничных условий становится предсказуемой.
Таким образом, в линейной области (т.е. в области применимости соотношений Онзагера) ситуация остаётся такой же, как и в равновесной. В нелинейной области (при достаточном удалении от равновесия), т.е. когда термодинамические потоки уже более не являются линейными функциями термодинамических сил, ситуация коренным образом меняется. Несмотря на все попытки обобщение теоремы о минимуме производства энтропии на нелинейные системы оказалось невозможным [4]. Вдали от равновесия система по-прежнему может эволюционировать к некоторому стационарному состоянию, но это состояние уже не определяется с помощью надлежаще выбранного потенциала.
В связи с этим возникает вопрос: что можно сказать относительно устойчивости состояний, к которым эволюционирует нелинейная система? До тех пор пока состояние определяется минимумом потенциала (производства энтропии), его устойчивость гарантирована. Флуктуации могут вывести систему из этого минимума, но второе начало термодинамики вынудит её вернуться обратно. Таким образом, существование термодинамического потенциала делает систему невосприимчивой к флуктуациям. Располагая потенциалом, мы описываем стабильный мир, в котором системы, эволюционируя, переходят в статичное состояние, установленное для них раз и навсегда. Но когда термодинамические силы, действуя на систему, становятся достаточно большими и вынуждают её покинуть линейную область, гарантировать устойчивость стационарного состояния или его независимость от флуктуаций невозможно. За пределами линейной области устойчивость уже не является следствием общих законов физики. Необходимо специально изучать, каким образом стационарное состояние реагирует на различные типы флуктуаций, создаваемых системой или окружающей средой.
Неравновесная термодинамика не даёт ответа на вопрос, каким образом происходит потеря устойчивости прежнего состояния и переход к новому, но она позволяет выяснить, какие причины побуждают систему к этому переходу.
2. Вторая вариация энтропии многофазной гетерогенной среды
Согласно второму началу термодинамики (1.1) состояние равновесия изолированной системы устойчиво, если оно соответствует максимуму энтропии. Энтропию системы, находящейся вблизи равновесного состояния, можно представить в виде:
![]() (5.1)
(5.1)
Здесь
![]() – значение энтропии в состоянии
равновесия;
– значение энтропии в состоянии
равновесия;
![]() и
и
![]() – первая и вторая вариации энтропии
системы. Под вариацией какого-либо
параметра Y понимают
отклонение величины этого параметра
от его стационарного или равновесного
значения
– первая и вторая вариации энтропии
системы. Под вариацией какого-либо
параметра Y понимают
отклонение величины этого параметра
от его стационарного или равновесного
значения
![]() под воздействием внешних возмущений:
под воздействием внешних возмущений:
![]()
Поскольку является максимальным значением энтропии, член первого порядка обращается в нуль, и следовательно, устойчивость состояния системы, находящейся вблизи равновесия, определяется знаком члена второго порядка . Таким образом, в области, близкой к равновесию, играет роль функции Ляпунова.
Для многофазной гетерогенной среды, в которой могут происходить химические и фазовые превращения, вторая вариация энтропии имеет вид:
![]()
Здесь
![]() – удельная энтропия i-й фазы (i = 1,2);
– удельная энтропия i-й фазы (i = 1,2);
![]() – средняя плотность i-й фазы;
– средняя плотность i-й фазы;
![]() – энтропия и средняя плотность j-го
компонента в i-й фазе.
– энтропия и средняя плотность j-го
компонента в i-й фазе.
С помощью ряда преобразований [6], это выражение можно представить в виде квадратичной формы:
 (5.2)
(5.2)
Здесь
![]() – удельный объём, теплоёмкость, истинная
плотность, температура и коэффициент
сжимаемости i-й фазы (i = 1,2),
соответственно;
– удельный объём, теплоёмкость, истинная
плотность, температура и коэффициент
сжимаемости i-й фазы (i = 1,2),
соответственно;
![]() – химический потенциал k-го компонента
в i-й фазе;
– химический потенциал k-го компонента
в i-й фазе;