
- •«Аналитическая химия и физико-химические методы анализа»
- •Способы проведения аналитических реакций в растворе
- •Лабораторная работа №2. Реакции и анализ первой аналитической группы катионов
- •Реакции и анализ третьей аналитической группы катионов
- •1. Общая характеристика катионов третьей группы
- •3. Опыт 2 . Обнаружение иона
- •1. Предварительные испытания
- •2. Отделение катионов I аналитической группы от II:
- •6. Обнаружение ионов
- •7. Обнаружение иона стронция
- •3. Стандартизация раствора хлороводородной кислоты по тетраборату натрия.
- •4. Определение содержания щёлочи в растворе
- •Контрольные вопросы :
- •Задачи для самостоятельного решения
- •1. Приготовление раствора титранта кМnO4
- •2. Приготовление раствора первичного стандарта
- •3. Стандартизация раствора титранта кМnO4
- •4. Вычисления
- •5) Определение железа (II)
- •Определение концентрации ионов меди в растворе
- •4. Определение меди в исследуемом растворе
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«УФИМСКАЯ ГОСУДАРСТВЕННАЯ АКАДЕМИЯ ЭКОНОМИКИ И СЕРВИСА»
Кафедра «Общая химия»
Методические указания к выполнению лабораторных работ по дисциплине
«Аналитическая химия и физико-химические методы анализа»
Уфа 2011
Составитель: О. Г. Горлевских.
УДК 543(076.5)
Методические указания к выполнению лабораторных работ по дисциплине «Аналитическая химия и физико-химические методы анализа» / Сост.: О.Г. Горлевских.- Уфа: Уфимская государственная академия экономики и сервиса, 2011.- 44 с.
В данном издании приведены методические указания к выполнению лабораторных работ по дисциплине «Аналитическая химия и физико-химические методы анализа». К каждой лабораторной работе дано краткое изложение теоретических основ. В конце каждой темы представлен перечень вопросов и заданий для подготовки студентов.
Методические указания предназначены для студентов специальности 280201.65 Охрана окружающей среды и рациональное использование природных ресурсов
.
Рецензент: Гаделева Х. К., канд. хим. наук, доцент кафедры «Специальная химическая технология».
Библиогр: 4 назв.
ВВЕДЕНИЕ
Аналитическая химия — это наука, разрабатывающая теоретические основы, методы и средства химического анализа, определение химического состава исследуемого вещества и его строение. Химический анализ широко используется для контроля производства и качества продукции ряда отраслей народного хозяйства химической, нефтеперерабатывающей, пищевой, фармацевтической и др.Создание и совершенствование методов, средств и методик анализа – это основы аналитической химии.
Методы -это универсальные и теоретически обоснованные способы определения состава безотносительно к определенному компоненту и к анализируемому обьекту.
Средства – приборы, реактивы , стандартные образцы , программы для компьютеров и т.д.
Методика анализа – это подробное описание анализа данного обьекта с использованием выбранного метода.
В аналитической химии наряду с другими анализами можно выделить качественный и количественный анализы.
Качественный анализ решает вопрос о том, какие компоненты включает анализируемый обьект. Количественный анализ дает сведения о количественном содержании всех или отдельных компонентов.
Методы определения можно классифицировать по характеру измеряемого состава или по способу регистрации составляющего сигнала. Методы определения можно условно разделить : на химические, физические и биологические.
Химические методы базируются на химических ( в том числе электрохимических) реакциях. Физические методы основаны на физических явлениях и процессах, биологические – на явлении жизни. Основные требования к методам аналитической химии: правильность и хорошая воспроизводимость результатов, избирательность, экспрессность,простота анализа,возможность его автоматиз
Лабораторная работа № 1
Способы проведения аналитических реакций в растворе
Содержание работы
Целью работы является знакомство с основными методами качественного анализа, овладение навыками проведения аналитических реакций.
Ход работы
Задание 1. Пробирочные реакции
Опыт 1. Реакция взаимодействия ионов меди с раствором аммиака.
Аммиак дает с ионом Сu2+ зеленоватый осадок гидроксосульфата меди:
2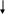
 СиS04
+ 2NН4ОН
(CuОН)2
+ (NН4)2S04
СиS04
+ 2NН4ОН
(CuОН)2
+ (NН4)2S04
В избытке аммиака осадок растворяется с образованием тетраамминокупро (II )сульфата, сообщающего раствору интенсивно синий цвет:
( Cu0Н)2S04 + (NН4)2S04 + 6NH4ОН 2[Cu(NH3)4]S04 + 8Н20
Выполнение реакции. К 2-3 каплям раствора соли CuS04 добавлять по каплям раствор аммиака до появления интенсивно синей окраски.
Опыт 2. Реакция взаимодействия ионов кальция с оксалатом аммония.
Оксалат аммония (NН4)2С2O4 осаждает из раствора солей Са2+ белый мелкокристаллический оксалат кальция:
С а2+ + С2042- СаС204
Выполнение реакции. .К 1-2 каплям раствора соли кальция прибавить столько же оксалата аммония. Осадок растворим в минеральных кислотах, но не растворяется в уксусной. Нагревание способствует быстрому осаждению оксалата кальция.
Задание 2. Капельные реакции
Опыт 3. Реакция ионов алюминия с ализарином.
Выполнение реакции . На фильтровальную бумагу нанесите каплю раствора соли А13 и 1-2 минуты подержите над открытой склянкой с концентрированным аммиаком. Получившееся водянистое пятно гидроксида алюминия смочите каплей спиртового раствора ализарина и снова обработайте аммиаком. Красноватая окраска алюминиевого лака, т.е. ализарата алюминия А1(0Н)зС4Н5O2(0Н)2S03Na , становится более отчетливой после подсушивания бумаги. Последнее необходимо также для удаления избытка аммиака, который сам дает с ализарином фиолетовое окрашивание.
Опыт 4. Реакция обнаружения ионов никеля.
. Ni2+ - ионы в аммиачной среде образуют с диметилглиоксимом (реактив Чугаева) красный осадок внутрикомплексной соли диметилглиоксимата никеля:
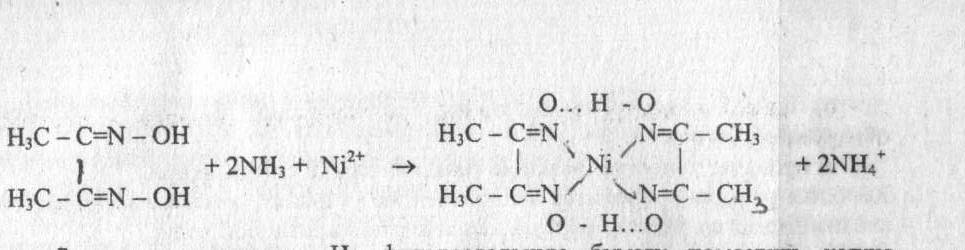
Выполнение реакции. На фильтровальную бумагу поместить каплю раствора Nа2НР04 (подстилка), затем в центр пятна нанести каплю исследуемого раствора и опять каплю Nа2НР04. После этого по периферии обвести пятно раствором диметилглиоксима и выдержать над раствором аммиака. В присутствии ионов №2+ образуется розовое кольцо.
Задание 3. Микрокристаллоскопические реакции
Опыт 5. Реакция обнаружения ионов кальция.
Выполнение реакции. К капле раствора соли кальция на предметном стекле прибавьте каплю 2н. Н2S04 и упарьте до появления каймы по краю капли. Рассмотрите игольчатые кристаллы гипса СаS04 *2Н20, собранные в пучки. Обнаруживаемый минимум - 0,04 мкг Ca.
Задание 4 .Реакции в «газовой камере».
Опыт 6.Реакция обнаружения ионов аммония.
Выполнение реакции.. Обнаружение ионов NH4+ проводят в газовой камере (чашка Петри) следующим образом: для проведения реакции берут чашку Петри. В нижнюю часть чашки Петри наносят 1-2 капли раствора соли аммония и 1-2 капли раствора NaОН. На верхнюю часть чашки Петри наносят каплю реактива Несслера или смоченную водой бумажку универсального индикатора. Накрывают нижнюю часть чашки Петри верхней частью. Через некоторое время на верхнем стекле с реактивом Несслера образуется осадок, а универсальный индикатор синеет вследствие образования гидроксильных ионов .
