
- •Черепкова и. А.. Химико-технологические системы
- •Содержание
- •Введение
- •Тема 1. Химико-технологические процессы и химико-технологические системы
- •1. 1. Классификация химических веществ.
- •Номенклатура химических соединений
- •1. 1. Основные классы неорганических соединений
- •1. 1. 2. Основы номенклатуры неорганических веществ
- •1. 1. 2. 1. Общие положения
- •1. 1. 2. 2. Номенклатура простых веществ
- •1. 1. 2. 3. Номенклатура сложных веществ
- •1. 1. 2. 3. 1. Бинарные соединения
- •1. 1. 2. 3. 2. Многоэлементные соединения
- •1. 1. 2. 4. Тривиальные названия веществ и смесей
- •Тривиальные названия индивидуальных веществ
- •Тривиальные названия смесей и растворов
- •Тема 2. Химическая термодинамика
- •2. 1. Расчет тепловых эффектов химических реакций с использованием стандартных термодинамических функций.
- •2. 2. Расчет изменения энтропии и энергии Гиббса в химических процессах
- •3. Термодинамический анализ возможности протекания химического процесса
- •Тема 3. Химическое равновесие
- •3. 1. Расчет термодинамических и практических констант равновесия
- •2. Расчет глубины и степени превращения исходных веществ, выхода продукта и равновесного состава.
- •3. 3. Влияние концентрации реагентов, внешнего давления и температуры на химическое равновесие.
- •Тема 4. Фазовые равновесия
- •4. 1. Построение и анализ диаграмм температура – состав
- •4. 1. 1. Метод физико-химического анализа. Диаграммы состав – свойство
- •4. 1. 2. Диаграммы температура – состав для идеальных и растворов
- •4. 1. 3. Диаграммы температура – состав для неидеальных растворов
- •4. 1. 4. Правило рычага
- •4. 1.5. Разделение бинарных растворов
- •5. Многовариантные расчетные задания
- •Библиографический список
Тема 3. Химическое равновесие
3. 1. Расчет термодинамических и практических констант равновесия
Термодинамическая константа равновесия может быть выражена как через активности веществ, участвующих в реакции, Ka , так и через фугитивности Kf:
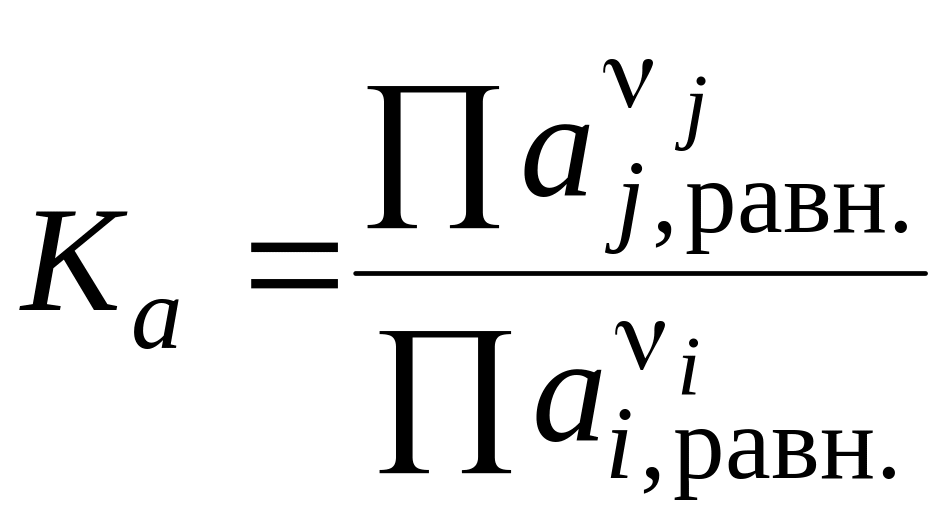
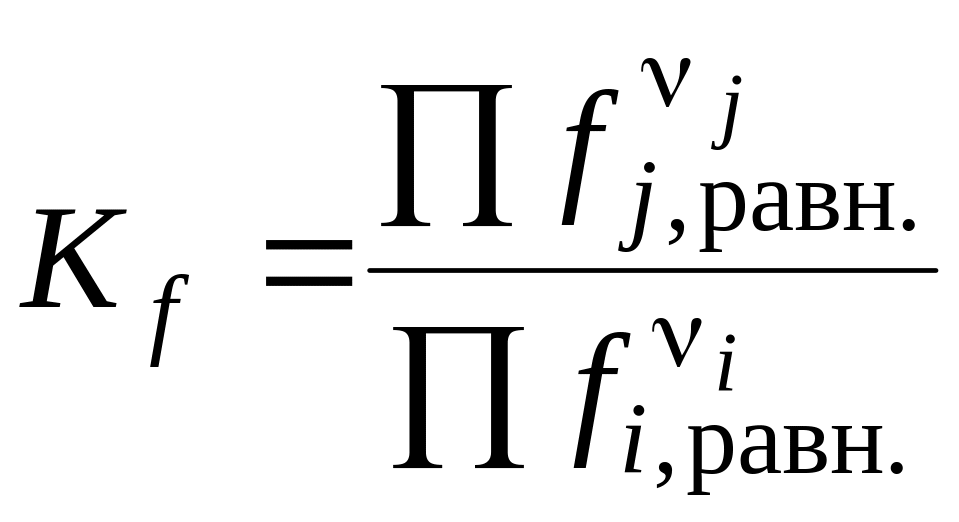 ,
,
Термодинамические константы равновесия являются безразмерными величинами.
Константа равновесия может быть рассчитана по частному уравнению изотермы химической реакции:
![]() ,
,
если
известно значение изменения стандартной
энергии Гиббса при данной температуре.
Тогда термодинамическая константа
равновесия
![]() рассчитывается как экспонента:
рассчитывается как экспонента:
![]()
Термодинамическая константа равновесия зависит от природы реагирующих веществ и температуры, но не зависит от давления, поскольку изменение стандартной энергии Гиббса не зависит от давления по определению.
Величина
константы равновесия может принимать
значения от нуля до бесконечности:
![]()
Пример 7: Рассчитаем термодинамическую константу равновесия реакции синтеза метанола при температурах 298 и 1000 К и давлении 101,013 кПа.
Решение:
Рассчитаем изменение стандартной
энергии Гиббса при температуре 298 К,
используя рассчитанные в примерах 1 и
3 значения
![]() и
и
![]() :
:
![]() =
– 90,47∙103
– 298( – 218,83) = = – 25258,66 Дж
=
– 90,47∙103
– 298( – 218,83) = = – 25258,66 Дж
По частному уравнению изотермы химической реакции
![]()
Для
расчета константы равновесия при 1000 К
воспользуемся рассчитанным в примере
5 значением стандартной энергии Гиббса
при температуре 1000 К для реакции синтеза
метанола
![]() .
.
По частному уравнению изотермы химической реакции
![]()
Если
химическая реакция протекает при
давлениях меньше ≤ 50 атм), то константа
равновесия, выраженная через приведенные
давления (![]() )
)
![]() ,
равна термодинамической константе
равновесия Ka
и
является безразмерной величиной
,
равна термодинамической константе
равновесия Ka
и
является безразмерной величиной
Кроме термодинамических констант равновесие могут характеризовать практические константы равновесия. Практические константы равновесия могут быть рассчитаны, если при равновесии определить количества или концентрации веществ, участвующих в реакции тем или иным методом химического или физико-химического анализа. Они могут быть выражены
– через числа молей веществ ni,j в равновесии:
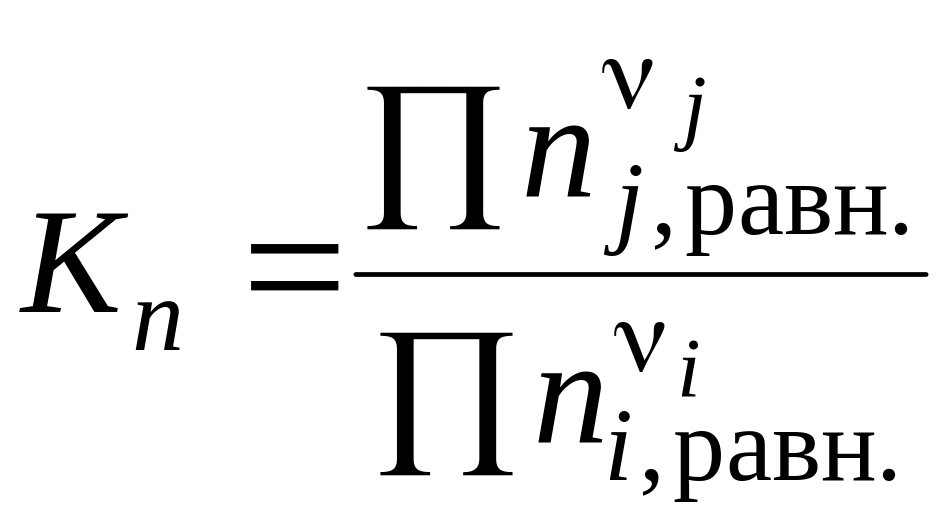 ;
;
– через молярные концентрации веществ Ci,j в равновесии:
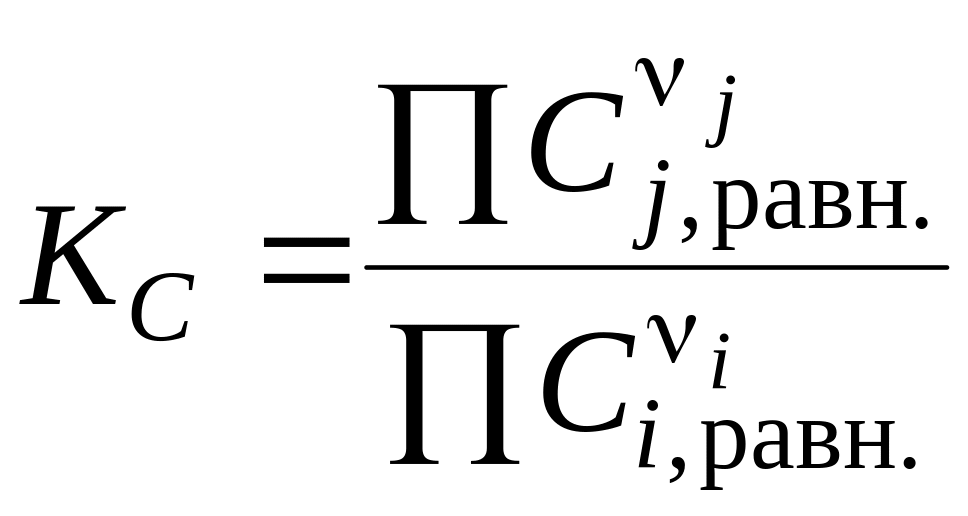 ;
;
– через мольные доли веществ Ni,j в равновесии:
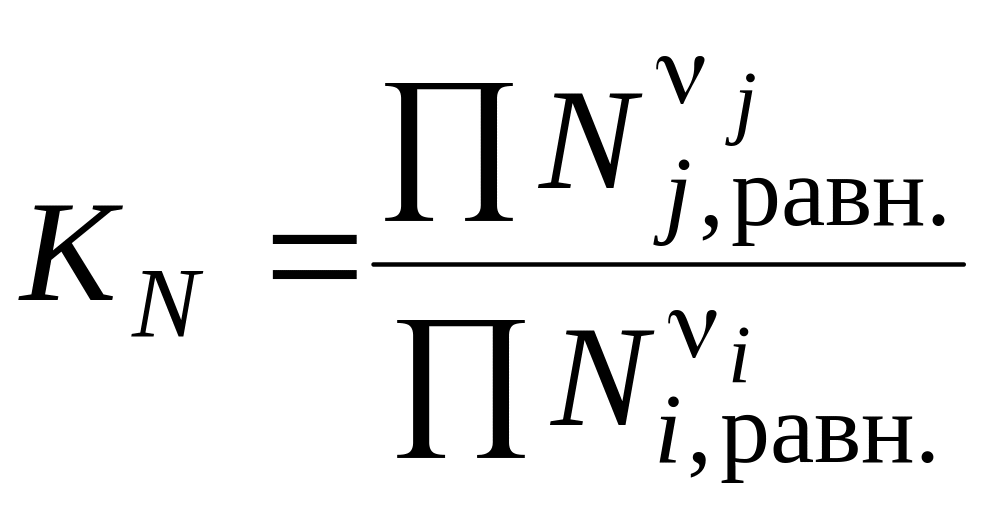 ;
;
– через парциальные давления веществ Pi,j в равновесии:
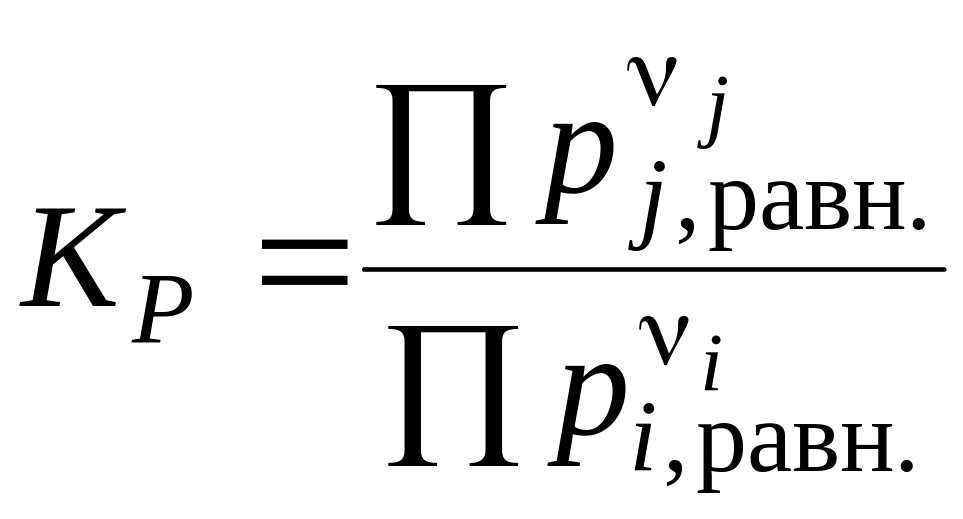
В отличие от термодинамических констант равновесия, практические константы являются размерными величинами.
Между термодинамическими и практическими константами равновесия существует определенная математическая связь. Например, константа , которая является термодинамической константой равновесия при давлениях меньше 50 атм., связана с практической константой равновесия, выраженной через моли Kn, следующим соотношением
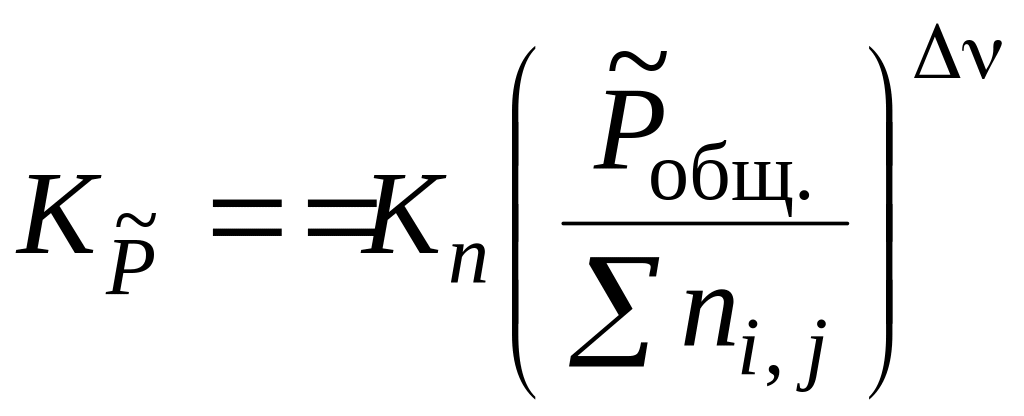
2. Расчет глубины и степени превращения исходных веществ, выхода продукта и равновесного состава.
Для расчета равновесного состава была введена универсальная величина – химическая переменная или глубина превращения ξ (кси), равная отношению изменения количества вещества данного реагента или продукта реакции к его стехиометрическому коэффициенту в уравнении химической реакции:
![]() ,
,
где знак “+” используется для продуктов реакции, а знак “ – “ для исходных веществ.
Равновесное количество вещества для каждого участника реакции выразим через глубину превращения:
![]()
Подставив полученное выражение в уравнение, связывающее термодинамическую Ka = и практическую Kn константы равновесия, получим
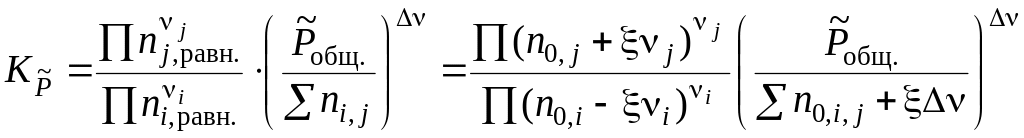
Решив это уравнение относительно химической переменной ξ, можно рассчитать: равновесные количества вещества каждого участника реакции, равновесные концентрации реагентов, степень превращения исходных веществ и выход продуктов реакции.
Пример
8:
Определим равновесную глубину превращения
ξ в реакции 2CO
+ S2
= 2COS
при температуре
500 К и давлении 101,013 кПа., при
условии, что исходные вещества взяты в
стехиометрических количествах.
Термодинамическая
константа равновесия
![]() =
3,56·1011
=
3,56·1011
Решение: Выразим равновесный состав через химическую переменную ξ и найдем область допустимых значений (ОДЗ) ξ из условия, число молей вещества всегда положительная величина:
|
2CO |
+ S2 = |
2COS |
исх. состав n |
2 |
1 |
0 |
равн. состав n |
2–2 ξ |
1– ξ |
2 ξ |
ОДЗ ξ: |
|
|
2–2ξ > 0 |
|
|
1–ξ > 0 |
=> 0 < ξ < 1 |
|
2ξ > 0 |
|
Выразим практическую константу Kn через глубину превращения ξ:
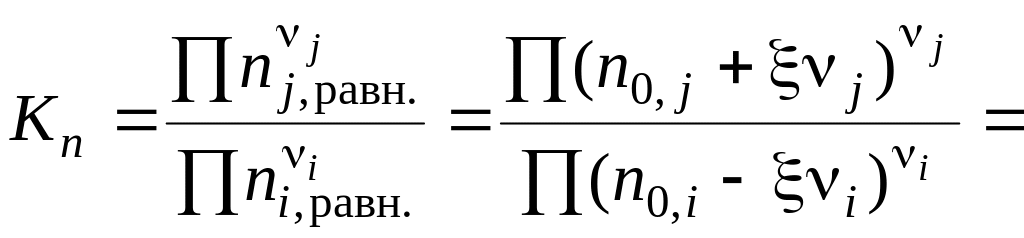
![]()
Выразим сумму молей газообразных веществ в равновесии через глубину превращения ξ:
![]()
Найдем разность стехиометрических коэффициентов в уравнении реакции:
![]()
Подставим
Kn,
![]() и
и
![]() в
уравнение, связывающее термодинамическую
константу
с практической константой Kn
в
уравнение, связывающее термодинамическую
константу
с практической константой Kn
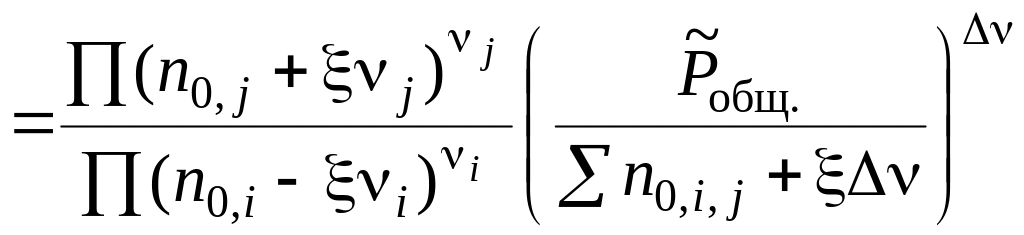 =
=
=
![]() =
=
![]()
Полученное кубическое уравнение
=
решаем точно, отбирая корни в соответствии с областью допустимых значений ξ, или приближенно (методом подбора или графически), что для практических расчетов вполне допустимо. Используя метод приближенных вычислений, получим, что при
= 3,56·1011
![]() = 0,9998.
= 0,9998.
Пример 9: Определим равновесную глубину превращения ξ в реакции 2CO + S2 = 2COS при температуре 500 К и давлении 101,013 кПа., при условии, что исходный состав содержал 0,2 моля СО и 2 моля газообразной серы. Термодинамическая константа равновесия = 3,56·1011
Решение: Выразим равновесный состав через химическую переменную ξ и найдем область допустимых значений (ОДЗ) ξ:
|
2CO |
+ S2 = |
2COS |
исх. состав n , моль |
0,2 |
2 |
0 |
равн. состав n , моль |
0,2–2 ξ |
2– ξ |
2 ξ |
ОДЗ ξ: |
|
|
0,2–2 ξ > 0 |
|
|
2– ξ > 0 |
=> 0 < ξ < 0,1 |
|
2 ξ > 0 |
|
Выразим практическую константу Kn через глубину превращения ξ:
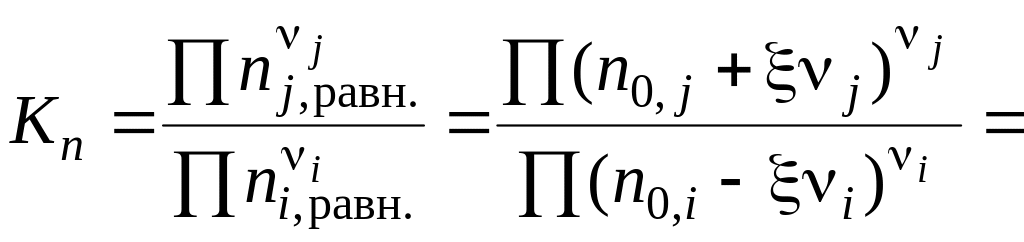
![]()
Выразим сумму молей газообразных веществ в равновесии через глубину превращения ξ:
![]()
Найдем разность стехиометрических коэффициентов в уравнении реакции:
Подставим Kn, и в уравнение, связывающее термодинамическую константу с практической константой Kn
=
=
![]() =
=
![]()
Полученное кубическое уравнение
=
решаем приближенно и получаем, что при
= 3,56·1011 ξ = 0,0999997.
Пример 10: Определим степень превращения исходных веществ в реакции 2CO + S2 = 2COS при условиях примеров 8 и 9.
Решение:
Степень превращения Xi – это отношение количества прореагировавшего вещества к его начальному количеству:
Xi
=
![]() =
=![]()
При условии примера 8 = 0,9998
Х![]() = 99,98 %
= 99,98 %
Х![]() =99,98
%
=99,98
%
При условии примера 9 = 0,0999997
Х![]() 000
= 50,00 %
000
= 50,00 %
Х![]() 00
= 5,00 %
00
= 5,00 %
Пример 11: Определим состав равновесной смеси в % (мол.) для реакции 2CO + S2 = 2COS при условиях примеров 8 и 9.
Решение:
Мольная доля вещества в смеси равна:
![]() ,
,
или в % (мол):
100
При условии примера 8 = 0,9998
![]() (мол.)
(мол.)
![]() (мол.)
(мол.)
![]() (мол.)
(мол.)
При условии примера 9 = 0,0999997
![]() (мол.)
(мол.)
![]() (мол.)
(мол.)
![]() (мол.)
(мол.)


