
- •Раздел I. Оптические методы анализа.
- •Тема 1. Фотометрические методы анализа.
- •1 Оптические методы анализа.
- •2 Электрохимический метод анализа.
- •Условия подчинения растворов закону б-л-б.
- •Тема 2. Нефелометрический и турбодиметрический методы анализа.
- •Тема 3. Люминесцентный метод анализа.
- •Закон Стокса – Ломмеля
- •Правило Левшина
- •Концентрационное тушение.
- •Температурное тушение.
- •Тушение посторонними примесями.
- •Сортовой анализ.
- •Люминесцентная микроскопия.
- •Химический люминесцентный анализ.
- •Качественный анализ одного вещества.
- •3.2.Прямой метод.
- •3.3.Метод добавок.
- •Тема 4. Поляриметрический метод анализа.
- •Зачернение
- •Канадский
- •Исландский шпат
- •2.1.Поляриметры с бикварцевыми пластинками.
- •2.2.Поляриметры с 1 и 2 дополнительными Николями.
- •Тема 5. Рефрактометрический метод анализа.
- •0 Среда 1 Среда 2
- •2 Среда 2
Закон Стокса – Ломмеля
Спектр люминесценции и его максимум всегда сдвинуты относительно спектра возбуждения и его максимума в сторону длинных волн (сравнить схему 1 и схему 2).
W Стоксово смещение СХЕМА 2
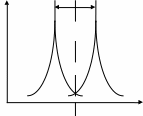 λ
(нм)
λ
(нм)
Рис. 1.3.2.
Вещества, поглощающие ультрафиолетовый свет, могут светиться любым светом. Вещества, свечение которых вызывается синим светом, могут светиться только тем светом, который лежит в более длинноволновой части спектра (зеленым, желтым, красным.)
Расстояние между максимумом спектра возбуждения и максимумом спектра люминесценции называется стоксовым смещением.
Чем больше стоксово смещение, тем более точно определяется вещество люминесцентным методом.
Правило Левшина
Спектры возбуждения и излучения зеркально подобны.
Это правило справедливо для сложных молекул и непригодны для простых молекул.
№5
Полнота преобразования возбуждающей энергии при люминесценции характеризуется энергетическим выходом Вэ и квантовым выходом Вк
Энергетический выход:
Вэ = Ел/Ев
Ел – энергия люминесценции.
Ев – поглощенная энергия возбуждения.
Квантовый выход:
Вк = Nл/Nв
Nл – число квантов люминесценции.
Nв – число квантов поглощенных при возбуждении.
Е кванта = h*v = h*c/λ
Ел = h*vл*Nл Ев = h*vв*Nв
Вэ
= Ел/Ев
= h*vл*Nл
/ h*vв*Nв
= Вк*vл
/
vв
= Вк*λв/λл
Зависимость между энергетическим и квантовым выходом описывается уравнением:
Вэ = Вк* λв/λл
Ученый Вавилов установил зависимость между энергетическим выходом люминесценции и длиной волны возбуждающего света. Зависимость выражается графически.
В э
I
III
II
 λв
λв
Рис. 1.3.3.
При возбуждении люминесценции коротковолновой частью спектра величина энергетического выхода растет пропорционально длине волны возбуждающего света.
Затем на некотором спектральном интервале выход не изменяет своей величины при увеличении длины волны возбуждающего света.
После чего в области наложения спектров поглощения и излучения происходит резкое падение выхода люминесценции.
1 участок описывается уравнением:
Вэ = а* λв а – постоянная.
Вэ = Вк* λв/λл = а* λв
Вк= а* λл
λл = const – каждое вещество испускает свет своей определенной длины волны, поэтому Вк= const.
Квантовый выход люминесценции остается постоянным при увеличении длины волны возбуждающего света, до некоторого значения λn и спектр люминесценции не зависит от того, каким участком спектра возбуждается люминесценция данного вещества.
В практике для получения люминесценции используют ультрафиолетовые лучи света, т.е. свет с самой короткой длиной волны, хотя это менее выгодно энергетически, но более просто в техническом исполнении.
3 участок характеризует тушение люминесценции.
№6
Тушение люминесценции бывает нескольких видов.
Концентрационное тушение.
Вэ
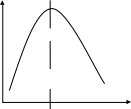 с
с
концентрационный барьер
(10-4 ÷ 10-3)М
Рис. 1.3.4.
При малых концентрациях энергетический выход пропорционален концентрации. Эта зависимость используется при количественном люминесцентном анализе.
При достижении концентрации (10-4 ÷ 10-3) М начинается резкое тушение люминесценции. Тушение возникает в результате усилившихся взаимодействий между молекулами, в результате которых возникают безизлучательные переходы.
Концентрационное тушение обратимо, т.е. при разбавлении растворы светятся вновь.
