
- •Оглавление
- •Часть первая. Физическая химия
- •1 Агрегатные состояния вещества
- •1.1 Межмолекулярные взаимодействия
- •1.2 Твердое состояние
- •1.3 Жидкое состояние
- •1.4 Газообразное состояние
- •2 Химическая термодинамика
- •2.1 Основные понятия химической термодинамики
- •2.2 Первое начало термодинамики
- •2.2.1 Термохимия
- •2.3 Второе начало термодинамики
- •2.3.1 Направление химических реакций
- •2.4 Третье начало термодинамики
- •3 Химическая кинетика и катализ
- •3.1 Основные понятия химической кинетики
- •3.2 Влияние концентрации реагентов на скорость химических реакций
- •3.3 Влияние температуры на скорость химических реакций
- •3.4 Катализ в химических реакциях
- •3.5 Особенности ферментативного катализа
- •4. Химическое равновесие
- •5 Фотохимические реакции
- •6 Свойства растворов
- •6.1 Общие сведения
- •6.2 Свойства растворов неэлектролитов
- •6.3 Электролитическая диссоциация
- •6.4 Ионное произведение воды. Понятие рН
- •6.5 Буферные растворы
- •7 Электрохимия растворов
- •7.1 Общие сведения
- •7.2 Электропроводность растворов
- •7.3 Электродные потенциалы и электродвижущие силы
- •7.4 Электрохимическая коррозия металлов
- •8 Адсорбция
- •8.1 Общие свойства поверхностей
- •8.2 Особенности сорбционных процессов
- •8.3 Адсорбция на границе раздела газ-жидкость
- •8.4 Адсорбция на границе газ-твердое тело
- •8.5 Адсорбция на границе жидкость-твердое тело
- •8.6 Значение адсорбционных процессов
- •Часть вторая.
- •9 Коллоидная химия
- •9.1 Классификация дисперсных систем
- •9.2 Общая характеристика коллоидных систем
- •9.3 Получение коллоидных систем
- •9.4 Методы очистки коллоидных систем
- •9.5 Молекулярно-кинетические свойства коллоидных систем
- •9.5.1 Броуновское движение
- •9.5.2 Диффузия
- •9.5.3 Осмотическое давление
- •9.5.4 Мембранное равновесие доннана
- •9.6 Оптические свойства коллоидных систем
- •9.7 Электрические свойства коллоидных систем
- •9.7.1 Мицеллярная теория стоения частиц лиофобного золя
- •9.7.2 Молекулярная теория строения частиц растворов вмс
- •9.7.3 Электрокинетические явления
- •9.8 Нарушение устойчивости коллоидов
- •9.8.1 Агрегативная и кинетическая устойчивость коллоидов
- •9.8.2 Нарушение устойчивости лиофобных золей
- •9.8.3 Нарушение устойчивости растворов вмс
- •10 Гели и студни
- •11 Почвеные коллоиды
- •11.1 Состав почвенных коллоидов
- •11.2 Строение и заряд частиц почвенных коллоидов
- •11.3 Адсорбция ионов почвенными коллоидами
- •11.4 Влияние состава обменных катионов на свойства почв
9.7.3 Электрокинетические явления
Электрокинетические явления – это эффекты, связанные с относительным движением двух фаз под действием электрического поля, а также возникновением разности потенциалов при вынужденном относительном движении двух фаз, на границе между которыми существует двойной электрический слой (рисунок 11а).
В мицеллах лиофобных
золей двойной электрический слой
образуется за счет противоположно
заряженных ионов адсорбционного и
диффузного слоев. На рисунке 11б
показан график изменения потенциала
при удалении от поверхности ядра к
внешней границе мицеллы. Потенциал
![]() о
называется термодинамическим
потенциалом. Величина
его зависит от количества потенциалопределяющих
ионов, адсорбированных на поверхности
ядра и не поддается экспериментальному
определению.
о
называется термодинамическим
потенциалом. Величина
его зависит от количества потенциалопределяющих
ионов, адсорбированных на поверхности
ядра и не поддается экспериментальному
определению.
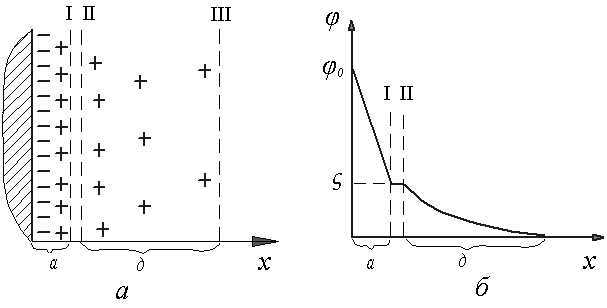
Рисунок 11 Строение двойного электрического слоя (а) и график изменения потенциала в двойном электрическом слое (б) мицеллы
На границе между
адсорбционным и диффузным слоями
возникает разность потенциалов, которая
называется электрокинетичес-ким
потенциалом. Этот
потенциал обычно обозначают греческой
буквой
![]() (дзета)
и потому называют дзета-потенциалом
(
-потенциал).
По-другому, его можно рассматривать как
заряд гранулы (рисунок 11б).
-потенциал
является важной характеристикой
коллоидных систем, определяющей их
свойства и устойчивость.
(дзета)
и потому называют дзета-потенциалом
(
-потенциал).
По-другому, его можно рассматривать как
заряд гранулы (рисунок 11б).
-потенциал
является важной характеристикой
коллоидных систем, определяющей их
свойства и устойчивость.
П
В электрокинетических явлениях обычно происходит отрыв ионов диффузного слоя от гранулы.
Электрофорез. Электрофорез – это движение частиц дисперсной фазы в электрическом поле к противоположно заряженному электроду.
В лиофобных золях гранула движется к одному из электродов, а ионы диффузного слоя – к другому. Существуют различные методы определения скорости движения частиц при электрофорезе. Зная их скорость, вычисляют величину -потенциала частиц цилиндрической формы по формуле:
![]() ,
,
где – электрокинетический потенциал, В; – динамическая вязкость растворителя, Пз (пуаз); и – скорость движения частицы, см/с; l – расстояние между электродами, см; – диэлектрическая проницаемость дисперсионной среды; Е – приложенная к электродам разность потенциалов, В; 300 – коэффициент перевода электростатической единицы в вольты.
Электрофорез также наблюдается в растворах ВМС. Однако до сих пор какая-либо теория электрофореза для свернутых в клубок макромолекул отсутствует.
Электрофорез находит применение при нанесении тонких слоев коллоидных частиц на поверхность проводящего материала, очистке веществ от примесей, при получении новых материалов и в медицинской практике.
Электроосмос. Электроосмос – это явление переноса жидкости через пористые диафрагмы и мембраны, а также через слои высококонцентрированных коллоидных частиц под действием внешнего электрического поля.
На поверхности стенок капилляров диафрагм и мембран также образуется двойной электрический слой. Поэтому при наличии внешнего электрического поля ионы диффузного слоя начинают двигаться к противоположно заряженному электроду, увлекая за собой сольватную оболочку и близлежащие слои жидкости за счет внутреннего трения – вязкости. Так происходит перенос жидкости к одному из электродов при электроосмосе.
Метод электроосмоса используют также при определении ς-по-тенциала коллоидных частиц. Для этого измеряют объем перене-сенной жидкости в единицу времени при определенной силе тока и вычисляют по формуле величину -потенциала:
=
![]() ,
,
где
![]() и 300 – имеют тот же смысл, что и в уравнении
электрофоре-за;
– электрокинетический потенциал, В;
– удельная электропро-водность жидкости,
Ом–1 см–1;
v
– объем жидкости, перенесенный за
секунду, см3/с;
I
– сила тока,
А (ампер).
и 300 – имеют тот же смысл, что и в уравнении
электрофоре-за;
– электрокинетический потенциал, В;
– удельная электропро-водность жидкости,
Ом–1 см–1;
v
– объем жидкости, перенесенный за
секунду, см3/с;
I
– сила тока,
А (ампер).
Электроосмос также находит применение в различных процессах. Например, им пользуются при обезвоживании пористых материалов: грунта, строительных материалов, продуктов питания, сырья для пищевой промышленности и другие. При этом обезвоживаемый предмет помещают между двумя электродами и вода, в зависимости от строения двойного электрического слоя, двигается к одному из них и собирается в специальных емкостях.
Потенциал протекания (эффект Квинке). Потенциал протекания – это эффект, обратный электроосмосу – возникноение разности потенциалов между концами капилляра, а также между противоположными поверхностями диафрагмы, мембраны или другой пористой среды при продавливании через них жидкости. Движущаяся по капиллярам жидкость уносит с собой ионы диффузного слоя. Тот конец капилляра, куда двигаются ионы диффузного слоя, приобретает заряд, одинаковый по знаку зарядам ионов диффузного слоя, а другой конец – противоположный по знаку заряд.
Потенциал седиментации (эффект Дорна). Потенциал седиментации – это эффект, обратный электрофорезу – возникновение разности потенциалов в жидкости вследствие движения частиц, вызванного силами неэлектрического характера (например, при оседании частиц в поле тяжести, при движении в ультразвуковом или центробежном поле). При принудительном движении частиц дисперсной фазы в жидкости ионы диффузного слоя несколько отстают от частиц дисперсной фазы. В результате та сторона жидкости, откуда уходит дисперсная фаза, приобретает заряд, одинаковый по знаку с зарядом ионов диффузного слоя, а другая сторона – противоположный по знаку заряд.
