
- •Сафу им. М.В.Ломоносова, иИиКт
- •10 Июня 2011 г.
- •Вопрос 1. Механическое движение. Система отсчёта. Путь, перемещение, траектория. Расчёт пути при равноускоренном движении.
- •Вопрос 2. Кинематика поступательного движения. Скорость мгновенная, средняя. Модуль скорости. Ускорение и его составляющие.
- •Вопрос 3. Кинематика вращательного движения. Элементарный угол поворота, угловая скорость, угловое ускорение. Связь линейных и угловых величин. Псевдовекторы.
- •Вопрос 4. Масса, свойство массы. Сила. Инерция. Первый закон Ньютона.
- •Вопрос 5. Сила. Импульс тела. Второй закон Ньютона. Принцип независимости сил. Третий закон Ньютона.
- •Вопрос 6. Импульс механической системы. Внешние силы. Замкнутая система. Закон сохранения импульса. Центр масс.
- •Вопрос 7. Работа силы в механике. Работа силы тяжести, работа силы упругости.
- •Вопрос 8. Кинетическая энергия – функция состояния системы. Теорема о кинетической энергии.
- •Вопрос 9. Силовое поле. Консервативные силы и диссипативные силы. Работа консервативных сил. Потенциальная энергия. Связь потенциальной энергии и консервативной силы.
- •Вопрос 10. Силовое поле. Потенциальное поле. Полная механическая энергия. Закон сохранения энергии.
- •Вопрос 11. Момент инерции материальной точки, твёрдого тела. Теорема Штейнера. Кинетическая энергия вращающегося тела.
- •Вопрос 12. Момент силы материальной точки относительно точки, момент силы материальной точки относительно оси. Основное уравнение динамики вращательного движения.
- •Вопрос 13. Момент импульса материальной точки относительно точки, момент импульса материальной точки относительно оси.
- •Вопрос 14. Момент импульса твердого тела. Закон сохранения момента импульса.
- •Вопрос 15. Параметры состояния. Термодинамическое равновесие. Модель идеального газа. Уравнение состояния идеального газа. Изопроцессы идеального газа.
- •Вопрос 16. Основное уравнение молекулярно-кинетической теории идеальных газов. Молекулярно-кинетическое толкование температуры. Средняя квадратичная скорость.
- •Вопрос 17. Закон Максвелла для распределения молекул идеального газа по скоростям. Анализ функции распределения.
- •Вопрос 18. Закон Максвелла для распределения молекул идеального газа по скоростям. Наиболее вероятная скорость.
- •Вопрос 19. Барометрическая формула. Распределение Больцмана.
- •Вопрос 20. Степени свободы молекул. Закон равномерного распределения энергии по степеням свободы. Внутренняя энергия газа – функция состояния.
- •Вопрос 21. Первое начало термодинамики. Работа газа в адиабатном и изопроцессах.
- •Вопрос 22. Молекулярно-кинетическая теория теплоемкости идеальных газов. Недостатки классической теории теплоемкости идеальных газов.
- •Вопрос 23. Адиабатный и политропный процессы. Уравнение Пуассона.
- •Вопрос 24. Обратимые и необратимые процессы. Круговой процесс (цикл). Термический кпд цикла. Цикл Карно. Кпд цикла Карно.
- •Вопрос 25. Энтропия, её статистическое толкование и связь с термодинамической вероятностью. Расчет энтропии в процессах идеального газа.
- •Вопрос 26. Второе начало термодинамики. Второе начало термодинамики для необратимых процессов. Теорема Нернста.
- •Вопрос 27. Реальные газы. Уравнение Ван-дер-Ваальса и его анализ. Внутренняя энергия реального газа.
- •Вопрос 28. Постулаты Эйнштейна. Релятивистский импульс. Закон взаимосвязи массы и энергии.
- •Основные формулы.
- •1. Кинематика поступательного движения.
- •2. Кинематика поступательного и вращательного движения.
- •3. Динамика. Работа, энергия. Законы сохранения.
- •4. Динамика вращательного движения.
- •5. Динамика вращательного движения. Работа, энергия.
- •6. Теория относительности.
- •Молекулярная физика. Термодинамика Молекулярно-кинетическая теория
- •2. Распределение газовых молекул по скоростям
- •3. Элементы физической кинетики
- •4. Первое начало термодинамики. Внутренняя энергии. Работа и теплота
- •6. Второе начало термодинамики
Вопрос 24. Обратимые и необратимые процессы. Круговой процесс (цикл). Термический кпд цикла. Цикл Карно. Кпд цикла Карно.
Обратимые процессы – это идеализация реальных процессов. Термодинамический процесс наз-ся обратимым, если он может происходить как в прямом, так и в обратном направлении и при этом в окружающей среде и самой системе не происходит никаких изменений. Любой процесс неудовлетворяющий этим условиям является необратимым.
Большое значение для применения термодинамики имеют круговые процессы, которые лежат в основе действия всех тепловых машин: холодильников, двигателей, паровых турбин. Тело, совершающее круговой процесс и обменивающееся энергией с др. телами называется рабочим телом. Если тепловая машина преобразовывает теплоту в работу, то это тепловой двигатель, а если посредством работы отнимается теплота у системы, то это холодильник. Круговые процессы изображаются в диаграммах P-V, P-T, V-T в виде замкнутых кривых. Круговой процесс – цикл, потому что за цикл система возвращается в исходное состояние. Если тело получает количество теплоты и совершает работу, то это прямой цикл, а если наоборот, то обратимый.
Чтобы тепловая машина имела возможность совершать работу необходимо наличие холодильника, т.е. тела, которому рабочее тело будет отдавать кол-во теплоты.
а) Q >0 A>0 б) A<0 Q<0
Особое место среди круговых процессов занимает цикл Карно.
Термический КПД – величина, равная отношению работы, совершённой рабочим телом в прямом обратимом цикле, к количеству теплоты, сообщённой в этом процессе нагревателем.
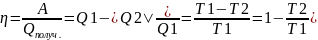
Тепловая машина при данных значениях температуры нагревателя и холодильника не может иметь большего КПД, чем машина, работающая по обратному циклу Карно при тех же значениях температур нагревателя и холодильника.
Цикл Карно является единственным круговым процессом, который, в принципе, можно осуществить обратимым образом.
Вопрос 25. Энтропия, её статистическое толкование и связь с термодинамической вероятностью. Расчет энтропии в процессах идеального газа.
Обратимые процессы – это идеализация реальных процессов. Термодинамический процесс называетсяся обратимым, если он может происходить как в прямом, так и в обратном направлении и при этом в окружающей среде и самой системе не происходит никаких изменений. Любой процесс неудовлетворяющий этим условиям является необратимым.
Энтропия
– функция состояния, которая связана
с полученной термодинамической системой
теплотой. Пусть с рабочим телом совершили
круговой цикл. Он получил количество
теплоты
 при
при
 и отдает при
и отдает при
 .
.

Отношение полученной теплоты к температуре, при которой происходит это получение, называется приведённая теплота.

ΔS=0 - для обратимых процессов, ΔS>0 – для обратимых; S-энтропия. В замкнутой системе энтропия либо возрастает, либо остаётся постоянной.
В различных изопроцессах:

Из
уравнения состояния:





V p=const
p=const

Энтропия и термодинамическая вероятность:
Термодинамическая вероятность системы - число всевозможных распределений частиц по координатам и скоростям, соответствующих данному термодинамическому состоянию систем.
Термодинамическая
вероятность – это число микросостояний,
которым осуществляется макросостояние.

Чем больше микросостояний, которыми осуществляется макросостояния, тем наиболее вероятно число способов его реализации.
Больцман связал энтропию с термодинамической вероятностью:

Энтропия
пропорциональна термодинамической
вероятности p. Т.к. p
заведомо большое число, поэтому берётся
 -
коэффициент пропорциональности,
рассчитанный Больцманом:
-
коэффициент пропорциональности,
рассчитанный Больцманом:


