
- •4.Константа электролитической диссоциации слабых электролитов. Закон разведения Оствальда.
- •5. Константа диссоциации воды. Ионное произведение воды. Водородный показатель рН.
- •6. Активность и коэффициент активности электролита. Средние ионные активности и коэффициенты активности. Средняя ионная моляльность, средний стехиометрический коэффициент.
- •7.Зависимость среднего ионного коэффнциента активности электролита от концентрации раствора и валентности ионов электролита. Ионная сила. Закон ионной силы.
- •8.Электролитическая теория сильных электролитов Дебая-Гюккеля, ионная атмосфера. Предельный закон Дебая-Гюккеля.
- •9.Удельная э/п р-ра,ее экс.Определение по сопротивл. Р-ра.Ед.Измер.В си.
- •12. Подвижность ионов.Ур-ние,связ. Подвижность(э/п)ионов при бескон.Разб.С пред.Эквив.Э/п р-ра(з-н Кольрауша).Опред.Степени дис.Слаб.Электрол.По э/п р-ра.
- •15.Кондуктометрия(кондукт.Титрование),опред.Растворимости и пр труднораствор.Соед,опред.РН р-ра.
- •16.Понятие о межфазной разности потенц.И строение двойного электр.Слоя на границе Ме-р-р.Нулевой р-р,потенц.Нулевого заряда.
- •17.Электр.Потенциал.Станд.Вод.Электрод.Зав-ть велич.Электр.Потенц.От прир.Электр.И от акт.Потенц.-опред.Ионов.Ур-ние Нернста.
- •18.Гальванический элемент. Процессы, протекающие на отрицательных и положительных электродах элемента. Правила записи гальванического элемента и электродных реакций.
- •31.Кинетика необратимых реакций третьего порядка
- •32.Кинетика Необратимые реакции n-ого порядка
- •34.Методы определения порядка реакции
- •37.Кинетика параллельных реакций первого порядка
- •1.Предмет электрохимии. Проводники первого и второго рода. Определение понятия электролит.
- •2.Основные положения теории электролитической диссоциации.Причины электролитической диссоциации электролитов при их растворении.
- •3.Сильные и слабые электролиты. Степень диссоциации, изотонический коэффициент.Уравнение связывающее степень диссоц. С изотон. Коэф.
- •46. Гетерогенный катализ
- •47.Мультиплетная теория гетерогенного катализа.
- •49.Цепные реакции.
17.Электр.Потенциал.Станд.Вод.Электрод.Зав-ть велич.Электр.Потенц.От прир.Электр.И от акт.Потенц.-опред.Ионов.Ур-ние Нернста.
Электр.потенц._ЭДС
гальв.эл-та,сост.из станд Вод.эл-та,запис.в
схеме слева и исследуемого
электрода.Потенциал станд.вод.электр.при
всех Т=0.
Станд.электр.потенц-потенц.электрода
при активности всех участников
электр.проц=1.Станд.электрод-электрод,у
кот.активность всех участников проц=1,а
потенц=станд. В качестве условно-нулевого
потенциала выбран потенциал
стандартного водородного электрода: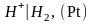 ,в
котором давление продуваемого водорода
равно 1 атм, а активность ионов
водорода в растворе равна единице (рис.
1). При любых температурах
,в
котором давление продуваемого водорода
равно 1 атм, а активность ионов
водорода в растворе равна единице (рис.
1). При любых температурах
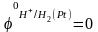 .Электродная
реакция для водородного электрода
записывается в следующем виде:
.Электродная
реакция для водородного электрода
записывается в следующем виде: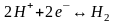 .
Стандартный
потенциал представляет собой величину,
характерную для данного электродного
процесса. Он зависит от температуры и
природы электрода. Тогда для электрода
типа MeZ+/Me:
.
Стандартный
потенциал представляет собой величину,
характерную для данного электродного
процесса. Он зависит от температуры и
природы электрода. Тогда для электрода
типа MeZ+/Me: Скачок
потенциала возникает и на границе
раздела двух растворов, это диффузионный
потенциал
Скачок
потенциала возникает и на границе
раздела двух растворов, это диффузионный
потенциал
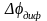 .
в
общем виде (для любого типа электродов):
.
в
общем виде (для любого типа электродов):
14.Основные положения теории электрической проводимости сильных электролитов. Коэффициент электрической проводимости. Электрофоретический и релаксационный эффекты, их влияние на электрическую проводимость. Уравнение Дебая-Онзагера для эквивалентной электропроводности разбавленного раствора сильного электролита.
Для
сильных электролитов, диссоциирующих
полностью, рассчитывают коэффициент
электропроводности:

который учитывает влияние электростатического взаимодействия ионов на скорость их движения.
С позиций теории Дебая-Гюккеля уменьшение подвижности ионов с ростом концентрации обусловлено двумя эффектами торможения движения ионов за счёт электростатического взаимодействия между ионом и ионной атмосферой (рис.5,6.)
1 )
Эффект
электрофоретического торможения
обусловлен торможением движения
центрального иона встречным движением
ионной атмосферы и имеет гидродинамическую
природу. Поскольку ионы гидратированы,
то движение центрального иона происходит
не в неподвижной среде, а в среде,
перемещающейся ему навстречу. Движущийся
ион находится под влиянием дополнительной
тормозящей силы (силы электрофоретического
торможения), что приводит к снижению
скорости его движения. (рис.5.)
)
Эффект
электрофоретического торможения
обусловлен торможением движения
центрального иона встречным движением
ионной атмосферы и имеет гидродинамическую
природу. Поскольку ионы гидратированы,
то движение центрального иона происходит
не в неподвижной среде, а в среде,
перемещающейся ему навстречу. Движущийся
ион находится под влиянием дополнительной
тормозящей силы (силы электрофоретического
торможения), что приводит к снижению
скорости его движения. (рис.5.)
2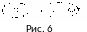 )
Эффект
релаксационного торможения.
Ионная атмосфера обладает сферической
симметрией до тех пор, пока отсутствует
внешнее электрическое поле. Как только
центральный ион начинает движение под
действием электрического поля, симметрия
ионной атмосферы нарушается. Перемещение
иона сопровождается разрушением ионной
атмосферы в одном положении иона и
формированием ее в другом, новом. Этот
процесс происходит с конечной скоростью
в течение некоторого времени, называемого
временем
релаксации.
В результате ионная атмосфера теряет
центральную симметрию и позади
движущегося иона всегда будет находиться
некоторый избыток заряда противоположного
знака, что и вызывает уменьшение его
скорости движения. (рис.6.)
)
Эффект
релаксационного торможения.
Ионная атмосфера обладает сферической
симметрией до тех пор, пока отсутствует
внешнее электрическое поле. Как только
центральный ион начинает движение под
действием электрического поля, симметрия
ионной атмосферы нарушается. Перемещение
иона сопровождается разрушением ионной
атмосферы в одном положении иона и
формированием ее в другом, новом. Этот
процесс происходит с конечной скоростью
в течение некоторого времени, называемого
временем
релаксации.
В результате ионная атмосфера теряет
центральную симметрию и позади
движущегося иона всегда будет находиться
некоторый избыток заряда противоположного
знака, что и вызывает уменьшение его
скорости движения. (рис.6.)
Уравнение Дебая-Онзагера для эквивалентной электропроводности разбавленного раствора сильного электролита:

в
котором постоянные (В1·λ∞)
и В2
характеризуют влияние релаксационного
и электрофоретического эффектов
соответственно. Если концентрация в
растворе стремиться к нулю С → 0
эти эффекты практически не проявляются
и
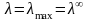 .
.
