
- •43. Гомогенный катализ в растворах.
- •33. Внешняя масса передачи.
- •34. Внутренняя масса передачи.
- •42. Катализ.
- •35. Кинетика фазовых превращений.
- •16. 3 Закон термодинамики.
- •44. Гетерогенный катализ
- •19. Изменение энтропии при изотермическом расширении или сжатии.
- •17. Применение третьего закона термодинамики для расчета равновесий.
- •13. Изменение свободной энергии при изотермическом расширении и сжатии
- •18. Изменение энтропии при изобарном нагревании или охлаждении.
- •37. Скорость образования зародыша концентрации.
- •23. Закон распределения энергии по степеням свободы.
- •25. Флуктуации плотности.
- •3. Основные условия существования термодинамического равновесия.
- •1. Первый закон тд. Тд координаты, обобщенные силы.
- •4.Химический потенциал.
- •2. Второй закон термодинамики. Общее понятие энтропии.
- •5.Основные термодинамические потенциалы (тдп).
- •8. Распределение в-ва м/у 2 фазами.
- •6.Механические и калорические ур-ия состояния.
- •7. Тдп идеального газа.
- •9.Фазовые превращения. Уравнения Клаузиуса – Клапейрона и Кирхгофа.
- •10. Хим. Равновесие в гом-ых сис-х.
- •15. Равновесие в гетеро-х системах.
- •12. Изменение энергии Гиббса при изменении температуры.
- •11. Изменение свободной энергии при химических реакциях.
- •41. Влияние температуры на скорость химических реакций
- •32.Кинетика гетерогенных реакций.
- •20. Энтропия и вероятность. Теорема Больцмана-Планка.
- •21. Распределение молекул газа в потенциальном поле.
- •28. Статистический расчет химического равновесия.
- •29. Формальная кинетика химических реакций.
- •31.Теория переходного состояния при химической реакции.
- •14. Зависимость константы равновесия от температуры.
- •38. Порядок реакции и молекулярность.
- •30.Теория активных столкновений Аррениуса.
- •22. Распределение молекул по импульсам.
- •24. Статистика Гиббса.
- •36. Работа образования зародыша конденсации.
41. Влияние температуры на скорость химических реакций
Скорость большинства реакций увеличивается с ростом температуры, т.к. при этом возрастает энергия сталкивающихся частиц и повышается вероятность того, что при столкновении произойдет химическое превращение. Для количественного описания температурных эффектов в химической кинетике используют два основных соотношения - правило Вант-Гоффа и уравнение Аррениуса.
Правило Вант-Гоффа заключается в том, что при нагревании на
10
°С скорость большинства химических
реакций увеличивается в 2 - 4 раза.
Математически это означает, что скорость
реакции зависит от температуры степенным
образом:
![]() где
у - температурный коэффициент скорости
где
у - температурный коэффициент скорости
![]() .
.
Правило
Вант-Гоффа довольно грубо описывает
экспериментальные данные и применимо
только в очень ограниченном интервале
температур. Гораздо более точным
является уравнение Аррениуса , описывающее
температурную зависимость константы
скорости:
![]() где
R-универсальная газовая постоянная.
где
R-универсальная газовая постоянная.
Это уравнение содержит два параметра, характеризующих химическую реакцию: А - предэкспоненциальный множитель, который не зависит от температуры, а определяется только видом реакции; ЕА - энергия активации, которую можно охарактеризовать как некоторую пороговую энергию, характеризующую высоту энергетического барьера на пути реакции. Энергия активации также не зависит от температуры. Для большинства реакций в растворе энергия активации
составляет 50-100 кДж/моль.
Экспоненциальный
множитель в уравнении Аррениуса можно
интерпретировать, как долю молекул,
энергия которых превышает ЕА при
температуре Т. В самом деле, если
рассмотреть больцмановскую функцию
распределения по энергии:
![]() ,
то доля молекул с Е > ЕА
дается выражением:
,
то доля молекул с Е > ЕА
дается выражением:
![]() .
.
32.Кинетика гетерогенных реакций.
ГЕТЕРОГЕННЫЕ РЕАКЦИИ - хим. р-ции с участием в-в, находящихся в разл. фазах и составляющих в совокупности гетерог. систему
3 стадии:
Перенос реагирующих вещ.-в с поверхности раздела фаз;
Собственно гетерогенной реакции
Отвод продуктов под реакционные
Т.к. скорости процессов во всех стадиях пропорциональна величине поверхности (граница раздела фаз), то скорость гетерогенной реакции должны зависеть от отношения м.у. величиной поверхности и объема. Стадии, опред. процесс яв.-ся более медленными. Если первая или третья стадия , то кинетика суммарного процесса будет диффузионной, если в хим. или физ. превращении, в самой реак., то процесс лежит в кинетич, области. При сравнимых скоростях всех 3 стадий имеет промежут. области. Это справедливо для сложн. процессов, сост. из неск. послед. стадий. Если процесс сост.из ряда паралл. протекающих процессов, то определяющей является самой быстрой.
20. Энтропия и вероятность. Теорема Больцмана-Планка.
Энтропия
– функция состояния, то есть любому
состоянию можно сопоставить вполне
определенное значение энергии.
Для
одной молекулы вероятность равна
 ,
а для N молекул –
,
а для N молекул –
 .
Общая вероятность – общий результат
произведения вероятностей на каждый
элемент. Равновесному состоянию
соответствует максимальная вероятность.
Следовательно, вероятность данного
состояния является критерием, который
определяет направление процесса и
позволяет найти равновесие. В
статистической термодинамике используется
термодинамическая
вероятность ω —
число способов, которыми может быть
реализовано состояние физической
системы. Термодинамическая вероятность
является числом математической
вероятности и всегда много больше 1. ω
– является функцией состояния и
максимальна при равновесии. Пусть 2
системы в термодинамическом равновесии
с ω1
и
ω2
образуют
сложную систему. ω1+2=
ω1
ω2.
(1) Это свойство мультипликативность
делает эту функцию неудобную для
непосредственных расчетов, так как она
не аддитативна. Она не связана с
термодинамическими характеристиками
системы и следовательно, найти такую
функцию вероятности которая была бы
связана с тепловыми характеристиками
и обладало бы аддитативностью. Введем
новую функцию
.
Общая вероятность – общий результат
произведения вероятностей на каждый
элемент. Равновесному состоянию
соответствует максимальная вероятность.
Следовательно, вероятность данного
состояния является критерием, который
определяет направление процесса и
позволяет найти равновесие. В
статистической термодинамике используется
термодинамическая
вероятность ω —
число способов, которыми может быть
реализовано состояние физической
системы. Термодинамическая вероятность
является числом математической
вероятности и всегда много больше 1. ω
– является функцией состояния и
максимальна при равновесии. Пусть 2
системы в термодинамическом равновесии
с ω1
и
ω2
образуют
сложную систему. ω1+2=
ω1
ω2.
(1) Это свойство мультипликативность
делает эту функцию неудобную для
непосредственных расчетов, так как она
не аддитативна. Она не связана с
термодинамическими характеристиками
системы и следовательно, найти такую
функцию вероятности которая была бы
связана с тепловыми характеристиками
и обладало бы аддитативностью. Введем
новую функцию
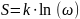 (*) Так как система состоит из 2 частей,
то
(*) Так как система состоит из 2 частей,
то
 (2) Графически положение молекул можно
изобразить в виде точек так называемом
в фазовом пространстве, осями которой
выделяются все координаты и импульсы.
При этом каждая опишется отображающей
точкой в фазовом пространстве. Для
полного механического описания моля
одноатомного газа необходимо 6N чисел.
Нет необходимости точно задавать число
атомов, можно задавать с некоторой
точностью координаты и импульсы ∆x,
∆y, ∆z, ∆Px,
∆Py,
∆Pz.
Это точность зависит от характера
задачи. Распределение должно описать,
сколько находится в разных областях
фазового пространства. Можно разделить
фазовое пространство на области с
одинаковыми объемами. Распределение
опишется совокупностью Ni
указывающих число молекул в каждой
области. Так как каждому способу
осуществления распределения молекулы
в одной области отвечает все способы
распределения в других областях, то
общее число способов и размещения
молекул в каждой области равно
(2) Графически положение молекул можно
изобразить в виде точек так называемом
в фазовом пространстве, осями которой
выделяются все координаты и импульсы.
При этом каждая опишется отображающей
точкой в фазовом пространстве. Для
полного механического описания моля
одноатомного газа необходимо 6N чисел.
Нет необходимости точно задавать число
атомов, можно задавать с некоторой
точностью координаты и импульсы ∆x,
∆y, ∆z, ∆Px,
∆Py,
∆Pz.
Это точность зависит от характера
задачи. Распределение должно описать,
сколько находится в разных областях
фазового пространства. Можно разделить
фазовое пространство на области с
одинаковыми объемами. Распределение
опишется совокупностью Ni
указывающих число молекул в каждой
области. Так как каждому способу
осуществления распределения молекулы
в одной области отвечает все способы
распределения в других областях, то
общее число способов и размещения
молекул в каждой области равно
 где g – число ячеек. Для того чтобы
найти равновесное распределение следует
искать максимальную термодинамическую
вероятность при учете что число молекул
постоянно и общая энергия системы равна
где g – число ячеек. Для того чтобы
найти равновесное распределение следует
искать максимальную термодинамическую
вероятность при учете что число молекул
постоянно и общая энергия системы равна
 где i – номер ячейки, а
где i – номер ячейки, а
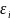 - энергия молекулы в -той области. Вместо
ωmax
можно искать Smax.
Необходимо
- энергия молекулы в -той области. Вместо
ωmax
можно искать Smax.
Необходимо найти
значение
найти
значение
 отвечающему максимуму величины S.
отвечающему максимуму величины S.
 .
Имеются дополнительные условия
постоянства частиц и энергии. Воспользуемся
формулой Стирлинга:
.
Имеются дополнительные условия
постоянства частиц и энергии. Воспользуемся
формулой Стирлинга:

 (3) Воспользуемся неопределенным
множителем Лагранжа.
(3) Воспользуемся неопределенным
множителем Лагранжа.
 Продифференцируем, приравняем нулю и
решим и получится
Продифференцируем, приравняем нулю и
решим и получится



 (4) так как B1=1/kT,
то
(4) так как B1=1/kT,
то
 (5) – это уравнение Больцмана.
(5) – это уравнение Больцмана.
