
- •2. Химическая технология и защита окружающей среды
- •3. Основные направления в развитии химической промышленности.
- •4. Хтп и их классификация
- •5. Уровни анализа, описания и расчета хтп.
- •6. Основные показатели хтп: степень превращения, выход продукта
- •7. Расходные коэф-ты. Избирательность хтп (φ)
- •Скорость хтп. Способы увеличения скорости
- •9. Материальный баланс процесса.
- •10. Тепловой баланс процесса.
- •11. Задачи термодинамического анализа
- •12. Равновесие Принцип Ле-Шателье и его применение в хт. Равновесная степень превращения
- •13.Константа равновесия и способы ее выражения
- •14. Влияние температуры на константу равновесия, ее расчет
- •15.Общая характеристика гомогенных хтп
- •16. Влияние концентраций реагентов на скорость гомогенных процессов и степень превращения
- •Основное кинетическое уравнение:
- •17. Влияние концентрации реагентов на избирательность гомогенных хтп.
- •18. Температура как фактор повышения скорости процесса и управления выходом продукта реакции (необратимые, обратимые, экзо- и эндотермические реакции)
- •19. Влияние температуры на скорость, избирательность процесса и выход продукта при протекании сложных реакций
- •20. Влияние давления на скорость газофазных реакций
- •1 Влияние давления на скорость необратимых процессов
- •2 Влияние давления на скорость обратимых процессов
- •21. Характер изменения основных параметров хтп во времени
- •22. Принципы расчета оптимальных параметров проведения процессов
- •23. Применение катализаторов в гомогенных системах (гомогенный катализ)
- •24. Общая характеристика гетерогенных хтп.
- •25. Процессы протекающие во внешнедиффузионной области.
- •26. Внутредиффузионная область протекания процессов.
- •27. Кинетическая область протекания процессов.
- •28. Основные методы изготовления и требования к катализаторам.
- •29. Особенности протекания каталитических процессов. Гетерогенные каталитические процессы.
- •Области протекания гетерогенных каталитических процессов.
- •Влияние этих торможений на избирательность Кт.
- •Влияние внутридиффузионных торможений на кинетику процесса.
- •30. Переходные области протекания гетерогенного хтп.
- •31. Моделирование хтп. Общие понятия.
- •37. Основные характеристики потоков и их влияние на хтп
- •38. Протекание хтп в потоке идеального вытеснения (ив)
- •39. Температурные режимы протекания хтп.
- •40. Протекание хтп в потоке полного (идеального) смешения.
- •4 0.1. Технологические расчеты.
- •40.2. Закономерность хтп без теплообмена.
- •41. Теплообмен с окружающей средой как фактор интенсификации хтп в потоке.
- •42. Секционирование реакционной зоны потока смешения.
- •42.1. Методы расчета каскада реакционных зон.
- •43. Сопоставление протекания хтп в различных идеальных потоках.
- •43.1. Процессы без тепловых эффектов ( при изотермическом температурном режиме).
- •43.2. Процессы с большими тепловыми эффектами.
- •43.3. Сравнение по избирательности.
- •44. Протекание хтп в неидеальных потоках.
- •45. Химические реакторы
- •45.1. Классификация
- •46. Основные требования к промышленным реакторам:
- •47. Отклонения реальных реакторов от идеализированных моделей
- •48. Реакторы для гомогенных процессов
- •49. Реакторы для проведения гетерогенных процессов в системе г — ж
- •50. Химико-технологические системы (хтс). Основные определение.
- •51. Моделирование химика-технологической системы
- •52. Организация химико-технологического процесса. Выбор схемы процесса
- •53. Основные условные обозначения технолог.Операторов. Основные способы отражения структуры хтс.
- •54. Технологическая схема хтс. Схемы с открытой цепью и циклические
- •55. Элементы анализа и синтеза хтс.
- •56. Основные типы связей.
- •59. Задачи, решаемые при исследовании хтс.
- •60. Сырьё в химической технологии. Комплексное использование сырья.
- •61. Методы очистки воды для производственных процессов. Очистка сточных вод. Замкнутые водооборотные циклы.
- •62. Очистка газообразных промышленных выбросов.
- •63. Обработка твердых отходов
- •64. Виды энергии, применяемые в химической промышленности. Использование тепла отходящих газов: регенераторы, рекуператоры, котлы-утилизаторы.
- •65. Методы обогащения твёрдых, жидких материалов и газов.
2 Влияние давления на скорость обратимых процессов
Для обратимых реакций, рассматривая влияние давления на скорость необходимо учитывать термодинамические и кинетические факторы. При протекании обратимых реакций давление сказывается на концентрации реагирующих веществ и на состоянии равновесия (принцип Ле-Шателье). В этом случае при рассмотрении вопроса «Влияние давления на скорость обратимых процессов» необходимо рассмотреть 2 случая:
реакции, идущие с уменьшением объёма
реакции, идущие с увеличением объёма
I. Реакции, идущие с уменьшением объёма
В этом случае одновременно с увеличением концентрации реагирующих веществ происходит смещение равновесия по принципу Ле-Шателье в сторону увеличения выхода целевых продуктов.
![]()
![]() ,
с = n/V
– число моль в ед. объема.
,
с = n/V
– число моль в ед. объема.

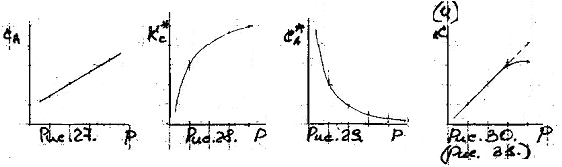
С увеличением давления будет расти по затухающей кривой => график U = f(P) такой же.
Вывод: для обратимых реакций, идущих с уменьшением объема стремятся увеличивать давление и ограничение роста давления чисто экономически.
II. Реакции, идущие с увеличением объема.
Применяя к этому случаю те же рассуждения и ту же последовательность, что и в случае (I) можно показать, что в данном случае Δс и U проходят через максимум.
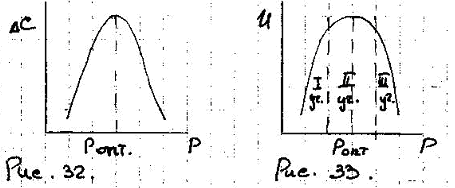
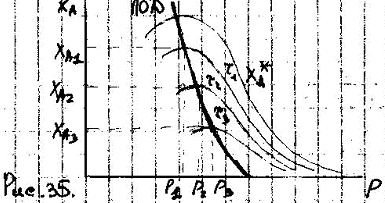
График на Рис. 33. имеет чисто теоретический хар-р, т.к. ХА = const во всем диапазоне изменения давления. Но на практике такого не может быть.
Разбиваем график на 3 участка.
Объяснение хода кривой (Рис. 33):
I – рост U р-ции связан с увеличением конц-ции реагирующих в-в.
II – уменьшение равновесных конц-ций продуктов р-ции компенсируется увеличением текущих конц-ций.
III – играют большую роль т/д-ое ограничение (р-ция уменьшается => сдвиг равновесия влево).
Л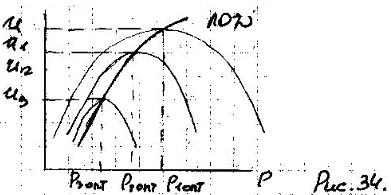 ОД
– линия оптимальных давлений.
ОД
– линия оптимальных давлений.
Р3 ОПТ < Р2 ОПТ < Р1 ОПТ
х1 < х2 < х3
Для
объяснения графика
![]() .
.
Из физ-ого смысла: с понижением давления, ХА – растет (в соотв-ии с принципом Ле-Шателье), для р-ций, идущих с увеличением объема => х3 – самая большая.
Из матем-ого смысла: см. формулу.
Технолога больше интересует, как влияет давление на Х для р-ции, идущей с увеличением объема.
Р1 < Р2 < Р3
![]()
Исходя из принципа Ле-Шателье, ХА увеличивается с увеличением давления.
Выводы:
Положение линии оптимальных давлений (ЛОД) в координатах ХА, Р показывает, что по мере увеличения Х необходимо уменьшать или Робщ. или Рпарц. реагентов. Для этого на практике реакционная смесь по мере увеличения Х разбавляется или инертным газом или паром.
Для р-ций, идущих с уменьшением объема, надо увеличивать давление, пока позволяют экономические соображения.
При проведении сложных (парал-ных, послед-ных) р-ций влияние Р эквивалентно изменениию конц-ции реагирующих в-в. Напр., увеличение Р увеличивает во всех случаях U образования целевых и побочных продуктов, но если порядок основной р-ции выше порядка побочной, то при этом увеличивается выход целевого продукта и избирательность пр-са.
Для гомогенных пр-сов в жидкой фазе влияние Р сказывается на константе скорости р-ции, но это проявляется при Р порядка сотен и тысяч атмосфер. дущей с увеличением объема.и.ление на Х для р-ции.величением текущих конц-ций.
ае ичение роста давления чисто экономически.
