
- •Внутренняя энергия
- •Фазовые переходы
- •Теплоёмкость
- •Свободная частица.
- •Квантовый гармонический осциллятор.
- •С татистический метод исследования
- •Внутренняя энергия идеального газа
- •Явление переноса:
- •М олекулярно-кинетическая теория диффузии:
- •М олекулярно-кинетическая теория теплопроводности:
- •М олекулярно-кинетическая теория вязкости:
- •П ервое начало термодинамики:
- •П рименение первого начала термодинамики к изопроцессам и адиабатическому процессу в ид. Газе.
- •О братимые и необратимые процессы:
- •В торое начало термодинамики:
- •Г армоническме колебания
- •Э нергия колебаний
- •Фигуры Лиссажу
- •Вынужденные колебания
- •Волновой процесс
- •М еханическое движение
- •У гловая скорость и ускорение
- •Масса тела
- •И мпульс материальной точки
- •Э нергия,работа.Мощность.
- •К онсервативные силы
- •Закон сохранения энергии
- •Абсолютно упругий удар
- •Релятивистский закон сложения скоростей:
- •Энергия гармонических колебаний:
М олекулярно-кинетическая теория вязкости:
Явлением внутреннего трения (вязкости) называется появление сил трения между слоями газа или жидкости, движущимися друг относительно друга параллельно и с разными по величине скоростями. Слой, движущийся быстрее, действует с ускоряющей силой на более медленно движущийся слой и наоборот. Силы внутреннего трения, которые возникают при этом, направлены по касательной к поверхности соприкосновения слоёв. Причиной вязкости является наложение упорядоченного движения слоёв газа с различными скоростями v и теплового хаотического движения молекул со скоростями, зависящими от температуры.
Явление
внутреннего трения описывается законом
Ньютона:
![]() ,
,
![]() -
напряжение трения, т.е. физ. в-на, численно
равная силе внутреннего трения,
действующая на единицу площади поверхности
слоя,
-
напряжение трения, т.е. физ. в-на, численно
равная силе внутреннего трения,
действующая на единицу площади поверхности
слоя,
![]() -
градиент скорости – изменение скорости
движения слоёв на единицу длины в
направлении внутренней нормали n
к поверхности слоя. Величина
-
градиент скорости – изменение скорости
движения слоёв на единицу длины в
направлении внутренней нормали n
к поверхности слоя. Величина
![]() -
называется коэффициентом внутреннего
трения или динамическим коэффициентом
вязкости. Коэффициент внутреннего
трения численно равен напряжению трения
или градиенте скорости, равном единице.
-
называется коэффициентом внутреннего
трения или динамическим коэффициентом
вязкости. Коэффициент внутреннего
трения численно равен напряжению трения
или градиенте скорости, равном единице.
Кинематическим
коэффициентом вязкости называется
величина
![]() ,
где
-
плотность вещества.
,
где
-
плотность вещества.
Коэффициент
внутреннего трения:![]()
![]() ,
где
,
где
![]() -
средняя арифметическая скорость
теплового движения,
-
средняя длина свободного пробега.
Коэффициент внутреннего трения не
зависит от давления (или плотности)
газа, поскольку
~
-
средняя арифметическая скорость
теплового движения,
-
средняя длина свободного пробега.
Коэффициент внутреннего трения не
зависит от давления (или плотности)
газа, поскольку
~
![]() .
.
П ервое начало термодинамики:
Изменение
внутренней энергии
![]() закрытой
системы, которое происходит в равновесном
процессе перехода системы из состояния
1 в состояние 2, равно сумме работы
закрытой
системы, которое происходит в равновесном
процессе перехода системы из состояния
1 в состояние 2, равно сумме работы
![]() ,
совершённой над системой внешними
силами, и количества теплоты
,
совершённой над системой внешними
силами, и количества теплоты
![]() ,
сообщённого системе:
,
сообщённого системе:![]() ,
где
,
где
![]() ,
где
,
где
![]() есть работа совершённая системой над
внешними силами в процессе
есть работа совершённая системой над
внешними силами в процессе
![]() .
.
Температура: Температура равновесной системы является мерой интенсивности теплового движения её молекул (атомов, ионов). Для равновесной системы частиц, подчиняющихся законам классической статистической физики, средняя кинетическая энергия теплового движения частиц прямо пропорциональна термодинамической температуре системы. В международной стоградусной шкале температура изменяется в С0. В термодинамической шкале температура изменяется в кельвинах (К)и обозначается: Т=273,15+t.
Работа
при изменение объёма идеального газа
:Элементарная
работа расширения
![]() ,
совершаемая системой при равновесном
процессе, измеряется площадью криволинейной
трапеции, заштрихованной на рис. Работа
системы в процессе С1С2,
равная
,
совершаемая системой при равновесном
процессе, измеряется площадью криволинейной
трапеции, заштрихованной на рис. Работа
системы в процессе С1С2,
равная
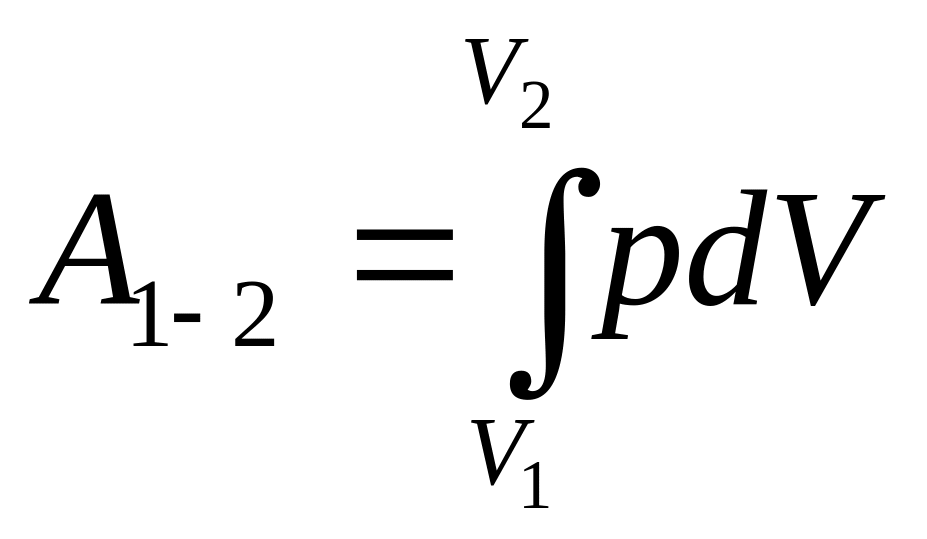 ,
измеряется площадью.
,
измеряется площадью.
Теплоемкость:
Теплоемкостью С тела, называется
физическая величина, численно равная
отношению количества теплоты
![]() ,
сообщаемого телу, к изменению dT
температуры тела в рассматриваемом
термодинамическом процессе:
,
сообщаемого телу, к изменению dT
температуры тела в рассматриваемом
термодинамическом процессе:
![]() .
Значение С зависит от массы тела, его
химического состава, термодинамического
состояния и процесса, в котором сообщается
теплота
.
.
Значение С зависит от массы тела, его
химического состава, термодинамического
состояния и процесса, в котором сообщается
теплота
.
П рименение первого начала термодинамики к изопроцессам и адиабатическому процессу в ид. Газе.
Если какой-либо из внешних параметров системы изменяется, то происходит изменение состояния термодинамической системы, называемое термодинамическим: Изопроцессами называют термодинамические процессы, происходящие в системе с постоянной массой при каком-либо одном постоянном параметре состояния. Изотермический процесс происходит при постоянной температуре (T=const). Изохорический процесс происходит при постоянном объёме (V-const). Изобарический процесс протекает при постоянном давлении (p=const). Адиабатическим процессом называется термодинамический процесс, который происходит в системе без теплообмена с внешними телами.
Зависимость теплоёмкость ид. газа от вида процесса:
Изохорический
Изобарический
Изотермический
Адиабатический
![]()
![]()
![]()
![]()
![]() -число
молей газа, содержащихся в массе М,
-число
молей газа, содержащихся в массе М,
К-показатель адиабаты, R-универсальная газовая постоянная.
