
- •37 Амфотерные гидроксиды. Характеристика химических свойств с точки зрения теории электролитической диссоциации.
- •38 Фосфор. Оксиды фосфора. Ортофосфорная кислота. Получение, свойства и применение. Качественная реакция на фосфат-анион.
- •Получение
- •Физические свойства
- •Белый фосфор
- •Жёлтый фосфор
- •Красный фосфор
- •Чёрный фосфор
- •Металлический фосфор
- •Химические свойства
- •Взаимодействие с простыми веществами
- •40 Дисперсные системы.
- •43 Истинные растворы. Гидратная теория растворов д. И. Менделеева.
- •49 Теория электролитической диссоциации с. Аррениуса.
- •50 Водородные соединения галогенов, особенности строения и свойств. Получение и применение. Качественные реакции на хлорид, бромид и йодид-анионы.
- •Свойства галогеноводородов
- •52 Гидролиз солей. Факторы, усиливающие или ослабляющие гидролиз.
- •55 Скорость химической реакции. Факторы, влияющие на скорость химической реакции.
- •58 Классификация химических реакций.
- •1. Реакции соединения
- •2. Реакции разложения
- •3. Реакции замещения
- •4. Реакции обмена
- •1. Протолитические реакции.
- •2. Окислительно-восстановительные реакции.
- •3. Лиганднообменные реакции.
- •4. Реакции атомно-молекулярного обмена.
- •61 Обратимые химические реакции. Химическое равновесие. Условия смещения химического равновесия. Принцип Ле-Шателье.
- •64 Окислительно-восстановительные реакции. Окислители и восстановители.
- •Описание
- •Окисление
- •Восстановление
- •Виды окислительно-восстановительных реакций
- •Химические свойства
- •73 Реакции ионного обмена. Условия протекания реакций ионного обмена до конца.
- •Введение, правило Бертолле
- •Изображение реакций ионного обмена
- •Правила написания реакций двойного обмена
- •Условия, при которых реакции ионного обмена протекают до конца
- •1. Если в результате реакции выделяется малодиссоциирующее вещество – вода.
- •2. Если в результате реакции выделяется нерастворимое в воде вещество.
- •3. Если в результате реакции выделяется газообразное вещество.
- •76 Понятие об аллотропии. Аллотропные видоизменения кислорода, водорода, углерода.
- •77 Соединения цинка. Особенности строения, свойства, получения. Применение соединений цинка в медицине. Качественная реакция на катион цинка.
- •79 Электролиз расплавов и растворов солей.
- •80 Соединения хрома. Физические и химические свойства, получение, применение. Превращение хроматов в дихроматы и наоборот.
- •Окись хрома (III)(Зеленый крон, хромовая зелень)
- •Бихромат аммония
- •Хромоаммониевые квасцы
- •Хлорид хрома (III)
- •Гексакарбонил хрома
- •86 Соединения марганца. Физические и химические свойства, получение и применение. Участие соединений марганца в окислительно-восстановительных реакциях.
- •Перманганат калия (Калий марганцовокислый)
- •Стеарат-пальмитат марганца
- •Циклопентадиенилтрикарбонил марганца(цтм)
- •Метилциклопентадиенилтрикарбонил марганца (Метил-цтм)
- •88 Электролиз растворов солей.
- •89 Кислородсодержащие соединения хлора, имеющие наибольшее практическое значение.
1. Протолитические реакции.
К протолитическим реакциям относят химические процессы, суть которых заключается в переносе протона от одних реагирующих веществ к другим.
В основе этой классификации лежит протолитическая теория кислот и оснований, в соответствии с которой кислотой считают любое вещество, отдающее протон, а основанием - вещество, способное присоединять протон, например:
|
CH3COOH |
+ H2O = |
CH3COO- + |
H3O+ |
|
кислотаI |
основаниеI |
основаниеI |
кислотаII |
|
NH3 + |
H2O = |
NH4+ + |
OH- |
|
основаниеI |
кислотаII |
кислотаII |
основаниеII |
К протолитическим реакциям относят реакции нейтрализации и гидролиза.
2. Окислительно-восстановительные реакции.
К таковым относят реакции, в которых реагирующие вещества обмениваются электронами, изменяя при этом степени окисления атомов элементов, входящих в состав реагирующих веществ. Например:
Zn + 2H+ → Zn2+ + H2↑,
FeS2 + 8HNO3(конц) = Fe(NO3)3 + 5NO↑ + 2H2SO4 + 2H2O,
Подавляющее большинство химических реакций относятся к окислительно-восстановительным, они играют исключительно важную роль.
3. Лиганднообменные реакции.
К таковым относят реакции, в ходе которых происходит перенос электронной пары с образованием ковалентной связи по донорно-акцепторному механизму. Например:
Cu(NO3)2 + 4NH3 = [Cu(NH3)4](NO3)2,
Fe + 5CO = [Fe(CO)5],
Al(OH)3 + NaOH = [NaAl(OH)4].
Характерной особенностью лиганднообменных реакций является то, что образование новых соединений, называемых комплексными, происходит без изменения степени окисления.
4. Реакции атомно-молекулярного обмена.
К данному типу реакций относятся многие из изучаемых в органической химии реакций замещения, протекающие по радикальному, электрофильному или нуклеофильному механизму.
Обратимые и необратимые химические реакции
Обратимыми называют такие химические процессы, продукты которых способны реагировать друг с другом в тех же условиях, в которых они получены, с образованием исходных веществ.
Для обратимых реакций уравнение принято записывать следующим образом:
А + В АВ.
Две противоположно направленные стрелки указывают на то, что при одних и тех же условиях одновременно протекает как прямая, так и обратная реакция, например:
СН3СООН + С2Н5ОН СН3СООС2Н5 + Н2О.
Необратимыми называют такие химические процессы, продукты которых не способны реагировать друг с другом с образованием исходных веществ. Примерами необратимых реакций может служить разложение бертолетовой соли при нагревании:
2КСlО3 → 2КСl + ЗО2↑,
или окисление глюкозы кислородом воздуха:
С6Н12О6 + 6О2 → 6СО2 + 6Н2О.
61 Обратимые химические реакции. Химическое равновесие. Условия смещения химического равновесия. Принцип Ле-Шателье.
Обратимые реакции — химические реакции, протекающие одновременно в двух противоположных направлениях (прямом и обратном), например:
3H2 + N2 ⇌ 2NH3.
Направление обратимых реакций зависит от концентраций веществ — участников реакции. Так в приведённой реакции, при малой концентрации аммиака в газовой смеси и больших концентрациях азота и водорода происходит образование аммиака; напротив, при большой концентрации аммиака он разлагается, реакция идёт в обратном направлении. По завершении обратимой реакции, т. е. при достижении химического равновесия, система содержит как исходные вещества, так и продукты реакции.
Простая (одностадийная) обратимая реакция состоит из двух происходящих одновременно элементарных реакций, которые отличаются одна от другой лишь направлением химического превращения. Направление доступной непосредственному наблюдению итоговой реакции определяется тем, какая из этих взаимно-обратных реакций имеет большую скорость. Например, простая реакция
N2O4 ⇌ 2NO2
складывается из элементарных реакций
N2O4 ⇌ 2NO2 и 2NO2 ⇌ N2O4.
Для обратимости сложной (многостадийной) реакции, например уже упоминавшейся реакции синтеза аммиака, необходимо, чтобы были обратимы все составляющие её стадии.
Химические реакции, которые протекают со сравнимыми скоростями в обоих направлениях, называются обратимыми. В таких реакциях образуются равновесные смеси реагентов и продуктов, состав которых далее уже не меняется со временем. Например, при нагревании происходят следующие превращения:
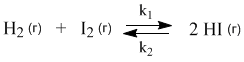
У этой равновесной системы есть замечательное свойство: ее состав не зависит от способа получения. Можно нагревать смесь газообразных водорода и йода, а можно взять для опыта чистый HI – результат будет одним и тем же: образуется равновесная смесь трех веществ (H2, I2, HI) одного и того же состава. Для внешнего наблюдателя в такой системе химические превращения не происходят, но на самом деле здесь постоянно идут прямая и обратная реакции. Рассмотрим эту систему с точки зрения химической кинетики.
Допустим, для опыта взяли газообразные водород и йод. В первый момент времени еще нет HI, поэтому идет только прямая реакция, скорость которой (vпр) выражается кинетическим уравнением:
vпр = k1[H2][I2]
Здесь k1 – константа скорости прямой реакции. Постепенно в смеси накапливается продукт реакции HI. Но в этих же условиях йодистый водород с заметной скоростью разлагается на исходные вещества: H2 и I2. Скорость обратной реакции (vобр) выражается кинетическим уравнением с константой скорости k2:
vобр = k2[HI]2
Когда йодистого водорода образуется уже достаточно много (т.е. когда его концентрация достигнет определенной величины), скорости прямой и обратной реакции выравниваются:
vпр = vобр
В этом случае говорят, что наступило химическое равновесие. Количество содержащихся в равновесной системе веществ H2, I2 и HI теперь не меняется со временем, если нет внешних воздействий на систему.
Химическим равновесием называется такое состояние химической системы, при котором количества исходных веществ и продуктов не меняются со временем.
Химическое равновесие носит динамический характер. Например, в приведенной реакции HI постоянно образуется и расходуется. Если добавить в такую равновесную смесь радиоактивный йод, то он быстро распределяется между молекулами I2 и HI. Это говорит о постоянном переходе атомов йода из исходного вещества в продукт реакции и обратно.
Можно ли изменить состояние химического равновесия? Иными словами – можно ли сдвинуть равновесие в сторону образования продуктов или в сторону образования исходных веществ?
Ответ на этот вопрос подсказывают кинетические уравнения прямой и обратной реакций. Если добавлять в равновесную систему извне «лишний» водород, то возрастет величина молярной концентрации [H2] в кинетическом уравнении прямой реакции. Следовательно, увеличится скорость прямой реакции vпр, а скорость обратной реакции vобр останется неизменной. В итоге израсходуется какая-то часть добавленного водорода, а равновесие сместится вправо, т.е. в сторону образования продукта реакции. Такой же эффект даст и введение в систему дополнительных порций I2.
Напротив, добавление HI приведет к сдвигу равновесия влево. Это подтверждает кинетическое уравнение обратной реакции (vобр): она получит преимущество, поскольку возрастет величина [HI]2.
Мы можем заметить важную закономерность: при попытке воздействовать на равновесную систему она «сопротивляется» такому воздействию. Действительно, добавление в равновесную систему H2 или I2 приводит к увеличению их расходования в прямой реакции. В итоге H2 или I2 в системе окажется меньше, чем было добавлено, зато возрастет количество HI. Наоборот, добавление HI приводит к более быстрому его расходованию в обратной реакции. Такая способность равновесных систем «сопротивляться» внешним воздействиям носит общий характер и известна под названием принципа Ле Шателье:
Если на равновесную систему воздействовать извне, изменяя какой-нибудь из факторов, определяющих положение равновесия, то в системе усилится то направление процесса, которое ослабляет это воздействие
